下列说法中正确的是( )
| A.NaHSO4在熔融状态下电离与在水中电离时,破坏的化学键完全相同 |
| B.H2O比H2S分子稳定,是因为H2O分子间能形成氢键 |
| C.NaCl和HCl气化时,克服的作用力不相同,故沸点不同 |
| D.碘沸点低、易升华,是因为分子中的 I﹣I键能较小 |
更新时间:2018-06-15 17:33:33
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】下列说法正确的是
| A.CO2溶于水和干冰气化克服的作用力相同 |
| B.H2O分子比H2S分子稳定的原因是H2O分子间存在氢键 |
| C.Na2O和Na2O2的化学键类型相同,其中阴、阳离子的个数比也相同 |
| D.二氧化碳分子中碳原子和氧原子最外电子层都具有8电子的稳定结构 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列说法不正确的是
| A.石英是由硅原子和氧原子构成的原子晶体,每个原子的最外层都具有8电子稳定结构 |
| B.Na2O是离子晶体,其溶于水生成NaOH的过程中既有离子键的断裂又有共价键的形成 |
| C.现代科技已经能够拍到氢键的“照片”,直观地证实了水分子间的氢键是一个水分子中的氢原子与另一个水分子中的氧原子间形成的化学键 |
| D.NH5的所有原子的最外层都符合相应的稀有气体原子的最外层电子结构,是既具有离子键又具有共价键的离子化合物 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列物质性质的变化规律,与共价键的键能大小有关的是( )
| A.F2、Cl2、Br2、I2的熔点、沸点逐渐升高 |
| B.HF、HCl、HBr、HI的热稳定性依次增强 |
| C.金刚石的硬度、熔点、沸点都高于晶体硅 |
| D.NaF、NaCl、NaBr、NaI的熔点依次降低 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列气体分子中不含共价键的是
| A.NH3 | B.O2 | C.Ar | D.HCl |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列说法错误的是
| A.因H-Br键能大于H-Cl键能,故HBr的沸点高于HCl |
B.配离子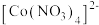 中各元素第一电离能: 中各元素第一电离能: |
C.N与N的π键比P与P的强,可推断 的稳定性比 的稳定性比 的高 的高 |
D. 中 中 的键角大于 的键角大于 中 中 的键角 的键角 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】电影《泰坦尼克号》讲述了一个凄婉的爱情故事,导致这一爱情悲剧的罪魁祸首就是冰山。以下对冰的描述中不正确的是
| A.冰形成后,密度小于水,故冰山浮在水面上 |
| B.水在4℃时达到最大密度,4℃后水的密度变小 |
| C.范德华力与氢键可同时存在于分子之间 |
| D.在冰中含有的作用力只有共价键和氢键 |
您最近一年使用:0次