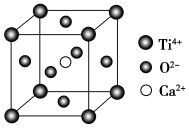
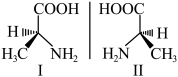下列说法不正确的是( )
| A.干冰升华和液氧气化时,都只需克服分子间作用力 |
| B.N2和Cl2O两种分子中,每个原子的最外层都具有8电子稳定结构 |
| C.HF、HCl、HBr、HI的热稳定性和水溶液的酸性均依次减弱 |
| D.石墨转化金刚石,既有化学键的断裂,又有化学键的形成 |
更新时间:2018-08-28 17:19:23
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】下列有关碱金属单质的性质的说法错误的是( )
| A.锂与水反应不如钠与水反应剧烈 |
| B.Rb比Na活泼,故Rb可以从NaCl溶液中置换出Na |
| C.熔、沸点:Li>Na>K>Cs |
| D.碱性:LiOH<NaOH<KOH<CsOH |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列叙述中,A的金属性肯定比B的金属性强的是
| A.A原子的最外层电子数比B原子的最外层电子数少 |
| B.A的氢氧化物为两性氧化物,B的氢氧化物为弱碱 |
| C.1molA从酸中置换出来的H+生成的H2比1molB从酸中置换出来的H+生成的H2多 |
| D.A元素的电负性比B元素的电负性小 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】X、Y、Z、W、M、Q为原子序数依次增大的短周期元素,X元素最外层电子数是次外层电子数的一半,W和Q同主族。下列说法错误的是


| A.Y是形成化合物种类最多的元素 |
| B.Q最高价氧化物对应的水化物为强酸 |
| C.电负性由大到小:M>W>Z |
| D.X单质和W的单质在空气中加热生成X2W2 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】X、Y、Z、R、W为原子序数依次增大的短周期元素,Z、W为同族元素,R是短周期中原子半径最大的主族元素。其中,X、Y、Z、W形成的化合物可表示为[YX4]+[XWZ4]-。下列说法不正确的是
| A.R与X、Y、Z、W均可形成离子化合物 |
| B.简单气态氢化物的稳定性:Z>Y |
| C.X、Y、Z三种元素形成物质的水溶液只能呈酸性 |
| D.[YX4]+为正四面体构型 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
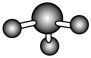
【推荐1】下列示意图正确的是
。
|
|
|
|
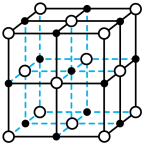
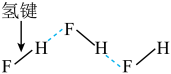
A. 的VSEPR模型 的VSEPR模型 | B.氯化铯的晶胞结构图 | C. 分子间的氢键 分子间的氢键 | D.丙氨酸的手性异构体 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列说法正确的是
| A.由非金属元素组成的化合物一定是共价化合物 |
| B.某物质在熔融态时能导电,该物质一定是离子化合物 |
| C.离子化合物中可能含有共价键,共价化合物中一定不含有离子键 |
| D.一般来说,对于组成和结构相似的分子,相对分子质量越大,分子间作用力越大,熔沸点越高,所以HF、HCl、HBr、HI的沸点依次升高 |
您最近一年使用:0次
【推荐1】下列说法正确的是
| A.BF3和NCl3中,每个原子的最外层都具有8电子稳定结构 |
| B.金刚石和石英晶体的熔点差别大的主要原因是共价键键长不同 |
| C.NaOH熔化的过程中,既破坏了离子键又破坏了共价键 |
| D.常温常压下,H2O是液态,H2S是气态,说明H2O的热稳定性更好 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列说法正确的是
| A.分子晶体的熔点一定比金属晶体的熔点低 |
| B.晶体在受热熔化过程中一定存在化学键的断裂 |
| C.DNA呈双螺旋结构是由于两条链间形成氢键所致 |
| D.1molNH4BF4中含有的配位键数目为1NA |
您最近一年使用:0次