【变式探究】(1)1.204×1024个氯化氢分子溶于水配成1 L溶液,则溶液的物质的量浓度为________ ;
(2)0.3 L 2 mol·L-1的硫酸铝溶液中SO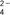 的物质的量为
的物质的量为
(3)2 mol·L-1 Mg(NO3)2溶液中含有0.4 mol NO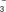 ,则溶液的体积为
,则溶液的体积为
(4)若20 g密度为ρ g·cm-3的Ca(NO3)2溶液中含有2 g Ca(NO3)2,则溶液中NO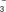 的物质的量浓度为
的物质的量浓度为
(5)V L Fe2(SO4)3溶液中含有a g SO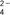 ,取此溶液0.5V L,用水稀释至2V L,则稀释后溶液中Fe3+的物质的量浓度为
,取此溶液0.5V L,用水稀释至2V L,则稀释后溶液中Fe3+的物质的量浓度为
2019高三·全国·专题练习 查看更多[1]
(已下线)2019高考备考一轮复习精品资料 第一章 从实验学化学 第2讲 物质的量浓度及一定物质的量浓度溶液的配制
更新时间:2018/09/12 13:54:10
|
相似题推荐
计算题
|
适中
(0.65)
【推荐1】将等物质的量的N2、H2混合于2L的固定体积的密闭容器中,在一定条件下反应合成氨,经5min后达到平衡,其中c(N2):c(H2) =3:1;若将混合气体中氨气分离,恰好能与250mL 2mol/L的稀硫酸溶液反应生成正盐;求:
(1)NH3的化学反应速率是多少?_____
(2)原容器中N2的物质的量是多少?_____
(3)5min后容器中H2的物质的量浓度是多少?_____
(4)N2的转化率是多少?_____
(要求书写计算过程)
(1)NH3的化学反应速率是多少?
(2)原容器中N2的物质的量是多少?
(3)5min后容器中H2的物质的量浓度是多少?
(4)N2的转化率是多少?
(要求书写计算过程)
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】试回答下列问题:
(1)0.5 mol的CH4气体中:①质量为_______ g,②约含_______ 个氢原子,③_______ mol电子;
(2)含2.3 g Na+的Na3PO4溶液100 mL,取出10 mL,Na+的物质的量浓度为_______ mol/L。
(3)已知AR3-电子数为18,则R的中子数为_______ 。
(1)0.5 mol的CH4气体中:①质量为
(2)含2.3 g Na+的Na3PO4溶液100 mL,取出10 mL,Na+的物质的量浓度为
(3)已知AR3-电子数为18,则R的中子数为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐3】(1)9.03×1024个H2O分子的物质的量为___________ ,在标准状况下4.48 LSO2的质量为___________ 。
(2)在标准状况下,22.4L由氮气和氧气组成的混合气体,其质量为30g,则其中氧气的质量为___________ g。
(3)某金属氯化物MClx的摩尔质量为133.5g/mol,取该金属氯化物26.7g配成水溶液,与足量AgNO3溶液完全反应,生成86.1g白色沉淀。则金属M的摩尔质量___________ 。
(4) 溶液分别恰好使相同体积的硫酸铁、硫酸铜两种溶液中的
溶液分别恰好使相同体积的硫酸铁、硫酸铜两种溶液中的 完全转化成沉淀,则硫酸铁、硫酸铜两种溶液的物质的量浓度之比是
完全转化成沉淀,则硫酸铁、硫酸铜两种溶液的物质的量浓度之比是___________ 。
(2)在标准状况下,22.4L由氮气和氧气组成的混合气体,其质量为30g,则其中氧气的质量为
(3)某金属氯化物MClx的摩尔质量为133.5g/mol,取该金属氯化物26.7g配成水溶液,与足量AgNO3溶液完全反应,生成86.1g白色沉淀。则金属M的摩尔质量
(4)
 溶液分别恰好使相同体积的硫酸铁、硫酸铜两种溶液中的
溶液分别恰好使相同体积的硫酸铁、硫酸铜两种溶液中的 完全转化成沉淀,则硫酸铁、硫酸铜两种溶液的物质的量浓度之比是
完全转化成沉淀,则硫酸铁、硫酸铜两种溶液的物质的量浓度之比是
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】在25 ℃时,将a mol·L-1的氨水溶液与0.02 mol·L-1HCl溶液等体积混合后溶液恰好呈中性(忽略溶液混合后体积的变化),用含a的表达式表示25 ℃时NH3·H2O的电离常数Kb=___________ 。用质量分数为17%、密度为0.93 g·cm-3的氨水,配制200 mL a mol·L-1的氨水,所需原氨水的体积V=___________ mL
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐2】(1)3.6gH2O的物质的量是____ mol,含有___ 个水分子,含有__ molH。
(2)标准状况下44.8LHCl气体的物质的量是____ mol,全部溶于水形成1L盐酸溶液,此盐酸的物质的量浓度是____ mol•L-1。
(3)3.01×1022个OH-的物质的量为___ mol,质量为___ g,含有质子的物质的量为___ mol,含有电子的物质的量为____ mol,这些OH-与____ molNH3的质量相同。
(4)用20gNaOH配成250mL溶液,它的物质的量浓度为___ mol•L-1。取出5mL该溶液,它的物质的量浓度为__ mol•L-1,再加水稀释至100mL,则稀释后溶液的物质的量浓度为___ mol•L-1。
(5)18.6gNa2R含0.6molNa+,则Na2R的摩尔质量为___ ,R的相对原子质量为___ 。
(2)标准状况下44.8LHCl气体的物质的量是
(3)3.01×1022个OH-的物质的量为
(4)用20gNaOH配成250mL溶液,它的物质的量浓度为
(5)18.6gNa2R含0.6molNa+,则Na2R的摩尔质量为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐3】物质的量是高中化学常用的物理量,请完成以下有关计算。
(1)含0.4mol 的
的 中所含的
中所含的 的物质的量是
的物质的量是___________ 。
(2)___________ mol 所含原子数与0.2mol
所含原子数与0.2mol 所含原子数相等。
所含原子数相等。
(3)同温同压下,同体积的甲烷 和
和 质量之比为
质量之比为___________ ,质子数之比___________ ;
(4)VL 溶液中含
溶液中含 amol,该
amol,该 溶液的物质的量浓度为
溶液的物质的量浓度为___________ ,取出V/2L再加入水稀释到4VL,则稀释后溶液中 的物质的量浓度是
的物质的量浓度是___________ 。
(1)含0.4mol
 的
的 中所含的
中所含的 的物质的量是
的物质的量是(2)
 所含原子数与0.2mol
所含原子数与0.2mol 所含原子数相等。
所含原子数相等。(3)同温同压下,同体积的甲烷
 和
和 质量之比为
质量之比为(4)VL
 溶液中含
溶液中含 amol,该
amol,该 溶液的物质的量浓度为
溶液的物质的量浓度为 的物质的量浓度是
的物质的量浓度是
您最近一年使用:0次



