下图为元素周期表的一部分,根据元素a~j在周期表中的位置,按要求回答下列问题。
(1)在a ~j中,化学性质最不活泼的元素是___________ (填元素符号)。
(2)f、g、h的单质分别与水反应,最剧烈的是___________ (填元素符号)。
(3)c、i的氢化物稳定性较强的是____________ (填化学式)。
(4)c、f可形成既含离子键又含非极性键的化合物,该化合物的电子式为__________ 。
(5)d、f、g的离子半径最大的是_______________ (填离子符号)。
(6)f的最高价氧化物的水化物与h的最高价氧化物的水化物反应的离子方程式为:___________________________________ 。
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | a | |||||||
| 2 | b | c | d | e | ||||
| 3 | f | g | h | i | j | |||
(1)在a ~j中,化学性质最不活泼的元素是
(2)f、g、h的单质分别与水反应,最剧烈的是
(3)c、i的氢化物稳定性较强的是
(4)c、f可形成既含离子键又含非极性键的化合物,该化合物的电子式为
(5)d、f、g的离子半径最大的是
(6)f的最高价氧化物的水化物与h的最高价氧化物的水化物反应的离子方程式为:
更新时间:2018-10-08 19:12:50
|
相似题推荐
填空题
|
较易
(0.85)
解题方法
【推荐1】1808年科学家戴维通过电解生石灰和汞的混合物制得了银白色的金属钙。请回答:
(1)钙的原子结构示意图为_______ ,它在元素周期表中的位置是_______
(2)原子半径:Ca_______ (填“>”或“<”,下同)Mg;氧化性:Ca2+_______ Mg2+
(3)科学家经分析后提出了有关推断,其中正确的是_______ (填选项序号)。
①自然界可能存在钙的单质②钙的金属性强于铝③钙与氧气不能反应
(4)钙的金属性_______ (填“强于”或“弱于”)镁,可以通过_______ (填实验方法)加以验证。
(1)钙的原子结构示意图为
(2)原子半径:Ca
(3)科学家经分析后提出了有关推断,其中正确的是
①自然界可能存在钙的单质②钙的金属性强于铝③钙与氧气不能反应
(4)钙的金属性
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】在1—18号元素中,选择合适的选项回答下列问题
1.写出①和②的非金属性较强的是( )
2.写出④的最高价氧化物化学式( )
3.写出③和⑤的最高价氧化物对应水化物反应的离子方程式( )
4.③和④两种元素的最高价氧化物对应水化物中碱性较强的是
5.写出③的单质在②单质中燃烧的现象()
6.①元素在周期表中的位置是( )
7.②和⑤两种元素中原子半径较大的是( )
8.下列化学用语表达不正确 的是( )
9.⑤和⑥形成的气态氢化物最稳定的是( )
10.④的氧化物类型为 ( )
| ① | ② | ||||||||||||||
| ③ | ④ | ⑤ | ⑥ |
| A.前者大 | B.后者大 | C.相等 | D.无法比较 |
| A.RO | B.R2O | C.R2O3 | D.RO2 |
| A.2NaOH+H2SO4=Na2SO4+2H2O | B.H+ +OH- =H2O |
| C.NaOH+H2SO4=Na2SO4+H2O | D.2OH- +H2SO4=SO42- +2H2O |
| A.前者大 | B.后者大 | C.相等 | D.无法比较 |
| A.白色固体 | B.淡黄色固体 | C.浅紫色火焰 | D.苍白色火焰 |
| A.第二周期第四主族 | B.第二周期第IV主族 |
| C.第二周期第IVA族 | D.第二周期第VA族 |
| A.前者大 | B.后者大 | C.相等 | D.无法比较 |
A.氟离子的结构示意图: | B.水分子的电子式: |
| C.二氧化碳的结构式:O=C=O | D.硫酸钠的电离方程式:Na2SO4=2Na++SO42- |
| A.前者大 | B.后者大 | C.相等 | D.无法比较 |
| A.酸性氧化物,非金属氧化物 | B.两性氧化物,金属氧化物 |
| C.碱性氧化物,金属氧化物 | D.酸性氧化物,金属氧化物 |
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】下表是元素周期表的一部分,除标出的元素外,表中的每个编号表示一种元素,请根据要求回答下列问题。
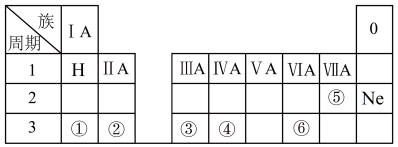
(1)元素④的符号是_______ ;②的最高价氧化物对应水化物的化学式为_______ ;⑤和⑥两种元素原子半径的大小关系:⑤_____ ⑥(填“>”或“<”);
(2)①和②两种元素金属性强弱关系:①_____ ②(填“>”或“<”);
(3)①的最高价氧化物的水化物与元素③的单质反应的化学方程式为:___________ 。

(1)元素④的符号是
(2)①和②两种元素金属性强弱关系:①
(3)①的最高价氧化物的水化物与元素③的单质反应的化学方程式为:
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】下列是部分短周期中第二、第三周期元素的原子半径及主要化合价。
回答下列问题:
(1)⑧在元素周期表中的位置是(周期、族)____________________ 。
(2)8个元素的最高价氧化物的水化物中,酸性最强的是___________________ (填化学式)。
(3)①元素和⑥元素形成化合物的电子式 是 ___________________________ 。
(4)写出④最高价氧化物对应水化物与⑥的氢化物水溶液反应的离子方程式:_______________________________________________ 。
(5)下列叙述正确的是______________ (填字母)。
A.③、④处于不同周期
B.②的阳离子与⑧的阴离子的核外电子数相等
C.⑥在同主族元素中非金属性最强
D.⑤元素与⑦元素两者核电荷数之差是8
E.①与⑧形成的化合物具有两性
| 元素代号 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ |
| 原子半径(nm) | 0.186 | 0.160 | 0.152 | 0.143 | 0.110 | 0.099 | 0.075 | 0.074 |
| 主要化合价 | +1 | +2 | +1 | +3 | +5、-3 | +7、-1 | +5、-3 | -2 |
回答下列问题:
(1)⑧在元素周期表中的位置是(周期、族)
(2)8个元素的最高价氧化物的水化物中,酸性最强的是
(3)①元素和⑥元素形成化合物的
(4)写出④最高价氧化物对应水化物与⑥的氢化物水溶液反应的离子方程式:
(5)下列叙述正确的是
A.③、④处于不同周期
B.②的阳离子与⑧的阴离子的核外电子数相等
C.⑥在同主族元素中非金属性最强
D.⑤元素与⑦元素两者核电荷数之差是8
E.①与⑧形成的化合物具有两性
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】短周期元素中,某些不同族元素的单质及其化合物有相似的化学性质,如铍和铝都能与氢氧化钠溶液反应;下图是元素周期表的一部分,编号为③的元素最外层与最内层电子数相等。
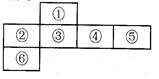
(1)编号为⑤的元素的符号为______ ,其在周期表中位于_______________________ 。
(2)写出Be与NaOH溶液反应生成Na2BeO2的离子方程式:_____________________ 。
(3)已知AlCl3的熔点为190℃(2.5×105Pa),沸点为182.7℃,试推测:
①BeCl2是______ 化合物(填“离子”或“共价”),
②Be(OH)2的碱性比LiOH__________ 。
(4)根据Mg在空气中的燃烧情况,Li在空气中燃烧生成的产物为______ (用化学式表示)。

(1)编号为⑤的元素的符号为
(2)写出Be与NaOH溶液反应生成Na2BeO2的离子方程式:
(3)已知AlCl3的熔点为190℃(2.5×105Pa),沸点为182.7℃,试推测:
①BeCl2是
②Be(OH)2的碱性比LiOH
(4)根据Mg在空气中的燃烧情况,Li在空气中燃烧生成的产物为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】联合国大会将2019年定为“化学元素周期表国际年”,高度体现了元素周期表的重要性,图中表示了元素周期表短周期的一部分,①~⑦代表7种短周期元素。
(1)写出七种元素中化学性质最不活泼的元素形成的单质的化学式_______ 。
(2)元素②的最低价阴离子的离子结构示意图是_______ 。
(3)②、⑤两种元素的最简单氢化物中稳定性较强的是_______ (填化学式)。
(4)⑤、⑥两种元素的最高价氧化物对应的水化物中,酸性较弱的是_______ (填化学式)。
(5)元素③最高价氧化物对应水化物与元素④的单质反应的离子方程式为:_______ 。
| ① | ② | |||||||
| ③ | ④ | ⑤ | ⑥ | ⑦ |
(1)写出七种元素中化学性质最不活泼的元素形成的单质的化学式
(2)元素②的最低价阴离子的离子结构示意图是
(3)②、⑤两种元素的最简单氢化物中稳定性较强的是
(4)⑤、⑥两种元素的最高价氧化物对应的水化物中,酸性较弱的是
(5)元素③最高价氧化物对应水化物与元素④的单质反应的离子方程式为:
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】2019年是元素周期表发表150周年,期间科学家为完善周期表做出了不懈努力。中国科学院院士张青莲教授曾主持测定了铟(49In)等9种元素相对原子质量的新值,被采用为国际新标准。
(1)In在周期表中的位置是______ 。
(2)In的最高价氧化物对应的水化物的碱性______ Ba(OH)2的碱性。(填“>”或“<”)
(3)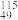 In的中子数与电子数的差值为
In的中子数与电子数的差值为______ 。
(1)In在周期表中的位置是
(2)In的最高价氧化物对应的水化物的碱性
(3)
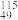 In的中子数与电子数的差值为
In的中子数与电子数的差值为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】下表是元素周期表的一部分,回答下列有关问题:
(1)写出①原子结构示意图_______________
(2)在这些元素中,金属性最强的元素是_______ ,(填元素符号)元素⑦与元素⑧相比,非金属性较强的是 _____________ (填元素符号)
(3)⑤的最高价氧化物对应水化物与⑧的最高价氧化物对应水化物反应的离子方程式为:________________
(4)⑤的单质与③的最高价氧化物对应水化物反应的离子方程式为___________________________
(5)已知某元素原子最外层电子数是其次外层电子数的2倍,该元素可以与⑦形成一种AB2型的化合物,请用电子式表示其形成过程:_____________________________ 。
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
2 | ① | ② | ||||||
3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |
4 | ⑩ | ⑪ | ⑫ |
(1)写出①原子结构示意图
(2)在这些元素中,金属性最强的元素是
(3)⑤的最高价氧化物对应水化物与⑧的最高价氧化物对应水化物反应的离子方程式为:
(4)⑤的单质与③的最高价氧化物对应水化物反应的离子方程式为
(5)已知某元素原子最外层电子数是其次外层电子数的2倍,该元素可以与⑦形成一种AB2型的化合物,请用电子式表示其形成过程:
您最近一年使用:0次



