已知H+(aq)+OH-(ag)=H2O(l)△H=-57.3kJ/mol,其中aq代表稀溶液,以下四个反应方程式中,反应热△H=-57.3kJ/mol的是
| A.H2SO4(aq)+2NaOH(ag)=Na2SO4(aq)+2H2O(l) |
| B.1/2H2SO4(aq)+1/2Ba(OH)2(ag)=1/2BaSO4(s)+H2O(l) |
| C.HCl(aq)+NaOH(ag)=NaCl(aq)+H2O(l) |
| D.HCl(aq)+NH3·H2O(ag)=NH4Cl(aq)+H2O(l) |
更新时间:2018-10-05 20:22:18
|
相似题推荐
单选题
|
较易
(0.85)
【推荐1】利用下列实验装置(夹持装置略),能达到实验目的的是
| 选项 | A | B | C | D |
| 目的 | 分离苯和三溴苯酚 | 验证锌与硫酸铜溶液反应有电子转移 | 证明相同温度时 ; ; | 测定中和热 |
| 实验方案 | 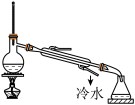 |  |  |  |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐2】如图为两种制备硫酸的途径(反应条件略)。下列说法不正确的是
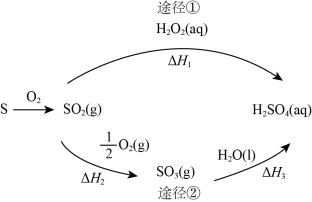

| A.途径②增大O2浓度可提高SO2的反应速率 |
| B.含1molH2SO4的浓溶液与足量NaOH反应,放出的热量即为中和热 |
| C.途径②中SO2和SO3均属于酸性氧化物 |
| D.若△H1<△H2+△H3,则2H2O2(aq)=2H2O(l)+O2(g)为放热反应 |
您最近半年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】中和反应的反应热测定实验中,下列操作一定会降低实验准确性的是
| A.实验过程中应使用同一个温度计测量温度 |
| B.使用18.4 mol⋅L-1 的硫酸溶液代替盐酸溶液做实验 |
| C.反应后读取温度计的最高温度 |
| D.测量HCl溶液的温度计用水洗净后才用来测NaOH溶液的温度 |
您最近半年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】利用如图所示装置测定中和热的实验步骤如下:

①用量筒量取50mL0.50mol·L-1盐酸倒入小烧杯中,测出盐酸温度;
②用另一量筒量取50mL0.55mol·L-1NaOH溶液,并用同一温度计测出其温度;
③将NaOH溶液倒入小烧杯中,设法使之混合均匀,测得混合液最高温度。
下列说法错误的是

①用量筒量取50mL0.50mol·L-1盐酸倒入小烧杯中,测出盐酸温度;
②用另一量筒量取50mL0.55mol·L-1NaOH溶液,并用同一温度计测出其温度;
③将NaOH溶液倒入小烧杯中,设法使之混合均匀,测得混合液最高温度。
下列说法错误的是
| A.NaOH溶液要稍过量 |
| B.倒入NaOH溶液的方法是一次性迅速倒入 |
| C.可以用Ba(OH)2溶液和硫酸代替氢氧化钠溶液和盐酸 |
| D.取三次测量所得的温度差的平均值作为计算依据 |
您最近半年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐3】下列热化学方程式书写正确的是(ΔH的绝对值均正确)
| A.C2H5OH(l)+3O2(g)=2CO2(g)+3H2O(g) ΔH=-1 322.8 kJ·mol-1(燃烧热) |
| B.NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l) ΔH=+57.3 kJ·mol-1(中和热) |
| C.S(s)+O2(g)=SO2(g) ΔH=-296.8 kJ·mol-1(反应热) |
| D.2NO2=O2+2NO ΔH=+116.2 kJ·mol-1(反应热) |
您最近半年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】下列有关中和反应反应热测定实验的说法正确的是
| A.温度计能代替玻璃搅拌器,用于搅拌反应物 |
| B.强酸与强碱反应生成1molH2O(l)释放的热量都约为57.3kJ |
| C.该实验中,读取混合溶液不再变化的温度为终止温度 |
| D.内筒内若有水残留,会使测得的反应热数值绝对值偏小 |
您最近半年使用:0次
单选题
|
较易
(0.85)
【推荐2】实验室用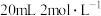 盐酸和
盐酸和 溶液反应进行中和热测定时,下列操作能减小实验误差的是( )
溶液反应进行中和热测定时,下列操作能减小实验误差的是( )
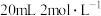 盐酸和
盐酸和 溶液反应进行中和热测定时,下列操作能减小实验误差的是( )
溶液反应进行中和热测定时,下列操作能减小实验误差的是( )| A.用铜制搅拌棒代替玻璃搅拌棒 | B.将盐酸逐滴缓慢滴入 溶液中 溶液中 |
C.用 固体代替 固体代替 溶液 溶液 | D.将反应所用的烧杯盖上泡沫盖 |
您最近半年使用:0次



