VL 浓度为 0.5mol/L 的盐酸,欲使其浓度 增大 1 倍,可采取的措施是
| A.通入标准状况下的 HCl 气体 11.2VL |
| B.加入 10mol/L 的盐酸 0.1VL,再稀释至 1.5VL |
| C.将溶液加热浓缩到 0.5VL |
| D.加入 2mol/L 的盐酸 VL 混合均匀 |
18-19高一上·湖南·阶段练习 查看更多[2]
更新时间:2018-10-17 13:24:35
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】下列关于物质的量的相关叙述正确的是
A. 的摩尔质量为71 的摩尔质量为71 |
B.18g 在标准状况下的体积约为22.4L 在标准状况下的体积约为22.4L |
C. 中含氢原子数为3 中含氢原子数为3 ( ( 为阿伏伽德罗常数的值) 为阿伏伽德罗常数的值) |
| D.0.1molNaOH溶解在1L水中,所得溶液中溶质的物质的量浓度为0.1mol/L |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】将一定质量的镁和铝的混合物投入100 mL盐酸中,固体全部溶解后,向所得溶液中加入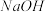 溶液,生成沉淀的物质的量与加入
溶液,生成沉淀的物质的量与加入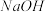 溶液的体积关系如下图所示。若不考虑金属和盐酸反应时
溶液的体积关系如下图所示。若不考虑金属和盐酸反应时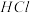 的发挥,则下列说法正确的是
的发挥,则下列说法正确的是

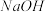 溶液,生成沉淀的物质的量与加入
溶液,生成沉淀的物质的量与加入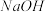 溶液的体积关系如下图所示。若不考虑金属和盐酸反应时
溶液的体积关系如下图所示。若不考虑金属和盐酸反应时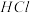 的发挥,则下列说法正确的是
的发挥,则下列说法正确的是
| A.镁和铝的总质量为9 g |
| B.盐酸的物质的量浓度为5mol·L-1 |
C.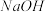 溶液的物质的量浓度为0.5mol·L-1 溶液的物质的量浓度为0.5mol·L-1 |
| D.生成的氢气在标准状况下的体积为11.2L |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】在环保、化工行业有一种溶液浓度的表示方法:质量—体积浓度,用单位体积溶液中所含的溶质质量来表示,单位g·m-3或g·L-1。现有一种20 ℃时的饱和CuSO4溶液,密度为1.2 g·cm-3,质量—体积浓度为200 g·L-1,则对此溶液的说法不正确的是( )
| A.该溶液的质量分数为16.7% |
| B.该溶液的物质的量浓度为1.25 mol·L-1 |
| C.在20 ℃时,硫酸铜的溶解度为20 g |
| D.在20 ℃时把200 g CuSO4·5H2O溶解于1 L水中恰好得到饱和溶液 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】下图是某学校实验室从化学试剂商店买回的硫酸试剂标签上的部分内容。据此下列说法正确的是


| A.该试剂的物质的量浓度为9.2 mol/L |
| B.该硫酸50 mL若用5 mol/L的氢氧化钠中和,需要该氢氧化钠溶液100毫升 |
| C.该硫酸与等体积的水混合所得溶液的质量分数等于49% |
| D.配制200 mL 4.6 mol/L的稀硫酸需取该硫酸50 mL |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】化学是以实验为基础的学科,下列有关实验操作正确的是
A.配制 溶液,应用托盘天平准确称取 溶液,应用托盘天平准确称取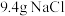 固体 固体 |
| B.中和反应反应热的测定实验中,测量反应前酸溶液的温度后立即测量碱溶液的温度,并记录数据 |
C.用碱式滴定管移取 溶液时,平视读数 溶液时,平视读数 |
| D.用标准氢氧化钠溶液滴定未知浓度的草酸时,滴定管的起始读数可以在0刻度以下 |
您最近一年使用:0次



