A、B、C、D、E、F是短周期主族元素,且原子序数依次增大。在短周期中A元素原子半径最小,D元素原子半径最大,B的简单氢化物的水溶液呈碱性,C、E同主族,形成的化合物为EC2、EC3。回答下列问题:
(1)E在元素周期表中的位置为_____________________________ 。
(2)比较B与C简单氢化物的热稳定性:_____ > 。(填化学式)
(3)D,C两元素组成的化合物D2C2的电子式为_____________________ ,D2C2与水反应的化学方程式为 ______________________________________________ 。
(4)下列事实能说明元素F的非金属性比元素E的非金属性强的是______ 。
A.元素F形成的单质比元素E形成的单质的熔点低
B.F和E两元素的简单氢化物受热分解,前者的分解温度高
C.F2通入到D2E的溶液中出现浑浊
D.F氢化物的酸性比E氢化物的酸性强
(1)E在元素周期表中的位置为
(2)比较B与C简单氢化物的热稳定性:
(3)D,C两元素组成的化合物D2C2的电子式为
(4)下列事实能说明元素F的非金属性比元素E的非金属性强的是
A.元素F形成的单质比元素E形成的单质的熔点低
B.F和E两元素的简单氢化物受热分解,前者的分解温度高
C.F2通入到D2E的溶液中出现浑浊
D.F氢化物的酸性比E氢化物的酸性强
更新时间:2018-10-29 17:38:37
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】已知有五种元素的原子序数的大小顺序为C>A>B>D>E,A、C同周期,B、C同主族;A与B形成的离子化合物A2B中所有离子的电子数都相同,其电子总数为30;D和E可形成4核10电子分子。试回答下列问题:
(1)C、D两种元素的名称分别为_______ 、_______ 。
(2)A,B,C离子半径从大到小的顺序_______ (用具体离子符号表示)。
(3)写出D元素形成的单质的结构式:_______ 。
(4)比较B、D氢化物的稳定性:_______ (用化学式表示)。
(5)A、B两种元素组成的化合物A2B2属于_______ (填“离子”或“共价”)化合物,存在的化学键类型是_______ ;写出A2B2与水反应的化学方程式:_______ 。
(6)D元素的最高价氧化物对应水化物的稀溶液与Cu反应的离子方程式:_______ 。
(1)C、D两种元素的名称分别为
(2)A,B,C离子半径从大到小的顺序
(3)写出D元素形成的单质的结构式:
(4)比较B、D氢化物的稳定性:
(5)A、B两种元素组成的化合物A2B2属于
(6)D元素的最高价氧化物对应水化物的稀溶液与Cu反应的离子方程式:
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】原子序数由小到大排列的四种短周期元素X、Y、Z、W,四种元素的原子序数之和为32,在周期表中X是原子半径最小的元素,Y、Z左右相邻,Z、W位于同主族。
(1)W在周期表的位置____________________ ;
(2)Z、W形成的气态氢化物的稳定性大小_______________ (写化学式)。
(3)由X、Y、Z、W四种元素中的三种组成的一种强酸,该强酸的稀溶液能与铜反应,离子方程式为________ 。
(4)由X、Y、Z、W和Fe五种元素组成的相对分子质量为392的化合物B,lmolB中含有6mol结晶水。对化合物B进行如下实验:
a.取B的溶液加入过量浓NaOH溶液并加热,产生白色沉淀和无色刺激性气味气体;过一段时间白色沉淀变为灰绿色,最终变为红褐色。
b.另取B的溶液,加入过量BaCl2溶液产生白色沉淀,加盐酸沉淀不溶解。
由实验a、b推知B的化学式为____________________ 。
(1)W在周期表的位置
(2)Z、W形成的气态氢化物的稳定性大小
(3)由X、Y、Z、W四种元素中的三种组成的一种强酸,该强酸的稀溶液能与铜反应,离子方程式为
(4)由X、Y、Z、W和Fe五种元素组成的相对分子质量为392的化合物B,lmolB中含有6mol结晶水。对化合物B进行如下实验:
a.取B的溶液加入过量浓NaOH溶液并加热,产生白色沉淀和无色刺激性气味气体;过一段时间白色沉淀变为灰绿色,最终变为红褐色。
b.另取B的溶液,加入过量BaCl2溶液产生白色沉淀,加盐酸沉淀不溶解。
由实验a、b推知B的化学式为
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】下表列出了①~⑨九种元素在周期表中的位置:
请按要求回答下列问题。
(1)元素③在周期表中所处位置_______ 。
(2)元素⑧的原子结构示意图是_______ 。
(3)②③④的简单气态氢化物的稳定性由强到弱的顺序为:_______ (用氢化物的化学式表示)。
(4)写出元素⑥形成的单质在氧气中燃烧的化学方程式:_______ 。
(5)⑥与⑨组成化合物甲,用电子式表示甲的形成过程:_______ 。
IA | 0族 | |||||||
1 | ① | IIA | IIIA | IVA | VA | VIA | VIIA | |
2 | ② | ③ | ④ | ⑤ | ||||
3 | ⑥ | ⑦ | ⑧ | ⑨ |
(1)元素③在周期表中所处位置
(2)元素⑧的原子结构示意图是
(3)②③④的简单气态氢化物的稳定性由强到弱的顺序为:
(4)写出元素⑥形成的单质在氧气中燃烧的化学方程式:
(5)⑥与⑨组成化合物甲,用电子式表示甲的形成过程:
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】X、Y、Z、W、R是五种短周期元素,其原子序数依次增大。X是周期表中原子半径最小的元素,Y 元素原子的最外层电子数是其次外层电子数的3倍,Z、W、R处于同一周期,R与Y处于同一族,Z、W原子的核外电子数之和与Y、R原子的核外电子数之和相等。请填写下列空白:
(1)画出W的原子结构示意图;_________________________ 。
(2)Z和W最高价氧化物的水化物的碱性较强的是:___________ (写化学式),它们之间在溶液中反应的离子方程式是;_______________________________________________ ;
(3)Z2Y2 中阴离子的化学式是________________ 。
(4)在同周期元素中,R 元素及与其相邻元素的原子半径从大到小的顺序是:____________________________________ 。与R元素同周期且非金属性最强的元素是:_________________ 。
(5)W的单质、石墨和二氧化钛(TiO2)按比例混合,高温下反应得到的化合物均由两种元素组成,且都是新型陶瓷材料,其反应的化学方程式是:_______________________________________ 。
(1)画出W的原子结构示意图;
(2)Z和W最高价氧化物的水化物的碱性较强的是:
(3)Z2Y2 中阴离子的化学式是
(4)在同周期元素中,R 元素及与其相邻元素的原子半径从大到小的顺序是:
(5)W的单质、石墨和二氧化钛(TiO2)按比例混合,高温下反应得到的化合物均由两种元素组成,且都是新型陶瓷材料,其反应的化学方程式是:
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】元素周期表是学习化学的重要工具。下表列出了①~⑩十种元素在周期表中的位置:
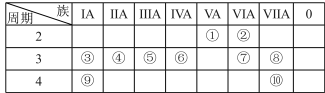
请按要求回答下列问题:
(1)写出元素①单质的电子式是______ ,元素②简单氢化物的结构式_____ 。
(2)③、④、⑨三种元素按原子半径由大到小的顺序排列为______ 。(用元素符号表示)
(3)元素⑥、⑦、⑧三种元素最高价氧化物对应水化物的酸性最强的为______ 。(用化学式表示)
(4)向元素③的单质与水反应后的溶液中加入元素⑤的单质,发生反应的化学方程式为_________ 。
(5)小组利用如图所示装置探究卤族元素的非金属性强弱。
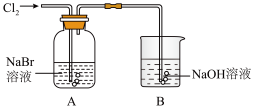
①写出装置A中发生的离子反应方程_________ 。
②取2mL A中橙黄色溶液于试管中,再滴入几滴KI淀粉溶液,观察到溶液变为蓝色。通过以上实验,不能得出非金属性:Br>I,理由________ 。

请按要求回答下列问题:
(1)写出元素①单质的电子式是
(2)③、④、⑨三种元素按原子半径由大到小的顺序排列为
(3)元素⑥、⑦、⑧三种元素最高价氧化物对应水化物的酸性最强的为
(4)向元素③的单质与水反应后的溶液中加入元素⑤的单质,发生反应的化学方程式为
(5)小组利用如图所示装置探究卤族元素的非金属性强弱。

①写出装置A中发生的离子反应方程
②取2mL A中橙黄色溶液于试管中,再滴入几滴KI淀粉溶液,观察到溶液变为蓝色。通过以上实验,不能得出非金属性:Br>I,理由
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】A、B、C、D四种元素,它们原子的核电荷数均小于18,且依次增大,A原子核内仅有一个质子;B原子的电子总数与D原子的最外层电子数相等;A原子与B原子最外层电子数之和与C原子的最外层电子数相等;D原子有两个电子层,最外层电子数是次外层电子数的3倍。
(1)试推断它们各是什么元素? 按要求写出合适的化学用语:A的元素符号:______ ,C单质的电子式:_________________ ,用电子式表示D的简单氢化物的形成过程________ 。
(2)甲、乙、丙、丁是由以上四种元素中的几种组成的10 电子微粒;
①甲为分子,且为天然气的主要成分,则甲的化学式为______
②乙为气体,且遇到无色酚酞溶液变成红色,则乙的电子式为_______
③丙为阳离子,丁为阴离子,且丙和丁在加热条件下生成的两种物质也是10电子微粒,请写出该反应的离子方程式_______________ 。
(1)试推断它们各是什么元素? 按要求写出合适的化学用语:A的元素符号:
(2)甲、乙、丙、丁是由以上四种元素中的几种组成的10 电子微粒;
①甲为分子,且为天然气的主要成分,则甲的化学式为
②乙为气体,且遇到无色酚酞溶液变成红色,则乙的电子式为
③丙为阳离子,丁为阴离子,且丙和丁在加热条件下生成的两种物质也是10电子微粒,请写出该反应的离子方程式
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】X、Y、Z、W、R、Q为元素周期表中前四周期的六种元素。回答下列问题:
(1)R的元素符号为_______ ,基态Q原子核外电子排布式为_______
(2) 的电子式为
的电子式为_______ ,其中Y的杂化方式为_______ ,分子的空间构型为_______
(3)X、Y、Z、W的第一电离能由大到小顺序为_______ (用元素符号表示)。
(4)现需要鉴定某化合物中是否含有X元素,可以采用的方法是_______ (填方法的名称)。
| X | 所有元素中非金属性最强 |
| Y | 核外有三个能级,每个能级的电子数相等 |
| Z | 原子2p轨道上成对电子数等于未成对电子数 |
| W | 第二周期中单电子数最多 |
| R | 核外电子有16种空间运动状态,有2个未成对电子 |
| Q | 原子序数等于Z与R二种元素原子序数之和 |
(2)
 的电子式为
的电子式为(3)X、Y、Z、W的第一电离能由大到小顺序为
(4)现需要鉴定某化合物中是否含有X元素,可以采用的方法是
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】有A、B、C、D、E五种元素,它们的核电荷数依次增大,且都小于18。其中只有C、D为金属元素;A和C的最外层均只有1个电子;B和E的最外层电子数相同,且B的L层电子数是K层电子数的3倍;D常用作易拉罐外壳。完成下列问题:
(1)写出相应元素的元素符号:B___________ ,E___________ 。
(2)A的一种核素中质子数为质量数的 ,则以
,则以 X的形式表示该核素为
X的形式表示该核素为___________ 。
(3)E元素的最高化合价为___________ 。
(4)A2B和C2B2反应的化学方程式___________ 。
(5)D与氢氧化钠溶液反应的化学方程式___________ 。
(1)写出相应元素的元素符号:B
(2)A的一种核素中质子数为质量数的
 ,则以
,则以 X的形式表示该核素为
X的形式表示该核素为(3)E元素的最高化合价为
(4)A2B和C2B2反应的化学方程式
(5)D与氢氧化钠溶液反应的化学方程式
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】短周期元素R、X、Y、Z的原子序数依次增大, a、b、c、d是这4种元素的单质(a、b、c、d顺序不与R、X、Y、Z对应),a为生活中常见的金属,厨房中常见a金属合金餐具和器具。在甲的溶液中通入丙气体,产生白色沉淀,它们之间转化关系如图所示。
回答下列问题:
(1)写出Z元素在元素周期表中的位置______________________ ;
(2)写出物质丙的电子式__________________ ;
(3)X、Y、Z元素简单离子的半径由大到小排列的顺序为(用离子符号表示)______________ ;
(4)写出Y元素的氢氧化物与NaOH溶液反应的离子方程式______________________________ ;
(5)As(砷)与X是同族元素,位于第四周期,请写出砷原子的原子结构示意图____________ 。

回答下列问题:
(1)写出Z元素在元素周期表中的位置
(2)写出物质丙的电子式
(3)X、Y、Z元素简单离子的半径由大到小排列的顺序为(用离子符号表示)
(4)写出Y元素的氢氧化物与NaOH溶液反应的离子方程式
(5)As(砷)与X是同族元素,位于第四周期,请写出砷原子的原子结构示意图
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】有A、B、C、D、E五种短周期主族元素,它们的原子序数依次增大。已知A的L层电子数是K层电子数的两倍,D是短周期元素中原子半径最大的元素,D的单质在高温下与C的单质充分反应,可以得到与E单质颜色相同的淡黄色固态化合物,试根据以上叙述回答:
(1)写出A、B对应的元素名称:A____________ ; B_____________ ;
(2)元素E在周期表中的位置:_________________________ ;
(3)元素C与D可以形成两种不同的化合物,写出D2C2的电子式:_______________ ;D2C的化学键类型为______________________ (填“离子键”“非极性共价键”或“极性共价键”)。
(4)AC2的结构式为______________ ,写出AC2与D2C2反应的化学方程式_______________________
(1)写出A、B对应的元素名称:A
(2)元素E在周期表中的位置:
(3)元素C与D可以形成两种不同的化合物,写出D2C2的电子式:
(4)AC2的结构式为
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】现有X、Y、Z三种元素,已知:
① X、Y、Z的单质在常温下均为气体。
② X的单质在Z的单质中燃烧,生成XZ ,燃烧时火焰为苍白色。
③ XZ的水溶液可使紫色石蕊溶液变红。
④ 两分子X的单质与一分子Y的单质化合,生成两分子X2Y,X2Y常温下为液体。
⑤ Z的单质溶于X2Y中,所得溶液具有漂白性。
据此推断:
(1)X_________ ;Y___________ ;Z__________ (写元素符号)。
(2)写出⑤的反应方程式________________________________________
(3)Z的单质工业制法的化学方程式:_______________________________________________
① X、Y、Z的单质在常温下均为气体。
② X的单质在Z的单质中燃烧,生成XZ ,燃烧时火焰为苍白色。
③ XZ的水溶液可使紫色石蕊溶液变红。
④ 两分子X的单质与一分子Y的单质化合,生成两分子X2Y,X2Y常温下为液体。
⑤ Z的单质溶于X2Y中,所得溶液具有漂白性。
据此推断:
(1)X
(2)写出⑤的反应方程式
(3)Z的单质工业制法的化学方程式:
您最近半年使用:0次



