分别用一种试剂将下列物质中混入的少量杂质除去(括号内为混入的杂质)
物质 | 需加入的试剂 | 有关离子方程式 |
HNO3(H2SO4) | ||
Cu(Fe) | ||
| ZnSO4(CuSO4) | ||
Fe(OH)3[Al(OH)3] |
更新时间:2018-10-31 20:22:55
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
名校
【推荐1】从海水中可以获得淡水、食盐并可提取镁、溴等物质。
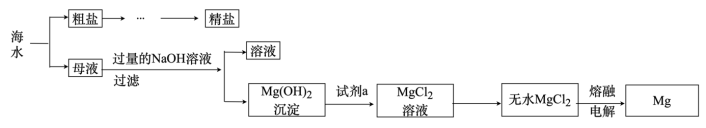
(1)试剂a是_______ 。
(2)从母液中提取镁的过程中,镁元素经历了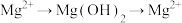 的过程,目的是
的过程,目的是_______ 。
(3)若要验证所得 溶液中是否含有
溶液中是否含有 ,可采用的方法是
,可采用的方法是_______ 。(不要求描述操作步骤和现象)
(4)用 溶液制成无水
溶液制成无水 ,加热溶液过程中,会生成
,加热溶液过程中,会生成 溶液和一种酸性气体。写出该反应的化学方程式
溶液和一种酸性气体。写出该反应的化学方程式_______ 。
(5)为了除去粗盐中 、
、 、
、 及泥沙可将粗盐溶于水,然后进行下列操作,正确的操作顺序是_______。
及泥沙可将粗盐溶于水,然后进行下列操作,正确的操作顺序是_______。
①过滤 ②加过量 溶液 ③加适量盐酸 ④加过量
溶液 ③加适量盐酸 ④加过量 溶液 ⑤加过量
溶液 ⑤加过量 溶液
溶液

(1)试剂a是
(2)从母液中提取镁的过程中,镁元素经历了
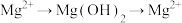 的过程,目的是
的过程,目的是(3)若要验证所得
 溶液中是否含有
溶液中是否含有 ,可采用的方法是
,可采用的方法是(4)用
 溶液制成无水
溶液制成无水 ,加热溶液过程中,会生成
,加热溶液过程中,会生成 溶液和一种酸性气体。写出该反应的化学方程式
溶液和一种酸性气体。写出该反应的化学方程式(5)为了除去粗盐中
 、
、 、
、 及泥沙可将粗盐溶于水,然后进行下列操作,正确的操作顺序是_______。
及泥沙可将粗盐溶于水,然后进行下列操作,正确的操作顺序是_______。①过滤 ②加过量
 溶液 ③加适量盐酸 ④加过量
溶液 ③加适量盐酸 ④加过量 溶液 ⑤加过量
溶液 ⑤加过量 溶液
溶液| A.②⑤④①③ | B.①④②⑤③ | C.④②⑤③① | D.⑤②④①③ |
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐2】通过海水晾晒可得粗盐,粗盐除NaCl外,还含有MgCl2、CaCl2、Na2SO4以及泥沙等杂质.以下是制备精盐的实验方案,各步操作流程如下:

(1)第②步操作的目的是除去粗盐中的______ (填化学式)。
(2)第⑤步“过滤”操作中得到沉淀的成分有:泥沙、BaSO4、Mg(OH)2、CaCO3、___ (填化学式)。
(3)在第③步操作中,选择的除杂试剂不能用KOH代替NaOH,理由是________ 。
(4)写出第⑥步反应的离子方程式_______________ ,______________ 。

(1)第②步操作的目的是除去粗盐中的
(2)第⑤步“过滤”操作中得到沉淀的成分有:泥沙、BaSO4、Mg(OH)2、CaCO3、
(3)在第③步操作中,选择的除杂试剂不能用KOH代替NaOH,理由是
(4)写出第⑥步反应的离子方程式
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】某同学在实验室纯盐的流程如下:

请回答:
(1)步骤③、⑤的操作名称是_______ 、_______ 。
(2)粗盐中含有 、
、 、
、 等杂质离子,步骤②所用的除杂试剂有:①碳酸钠溶液;②氯化钡溶液;③氢氧化钠溶液,则加入试剂的顺序
等杂质离子,步骤②所用的除杂试剂有:①碳酸钠溶液;②氯化钡溶液;③氢氧化钠溶液,则加入试剂的顺序_______ (填编号)。
a.②③① b.①②③ c.③②① d.③①②
(3)除杂过程中,加入 溶液的目的是
溶液的目的是_____________ 。
(4)步骤④判断加入的盐酸“适量”的方法是______________________ ,步骤⑤加热时要用玻璃棒搅拌,这是为了防止________ ,加热到_________ 时,停止加热。

请回答:
(1)步骤③、⑤的操作名称是
(2)粗盐中含有
 、
、 、
、 等杂质离子,步骤②所用的除杂试剂有:①碳酸钠溶液;②氯化钡溶液;③氢氧化钠溶液,则加入试剂的顺序
等杂质离子,步骤②所用的除杂试剂有:①碳酸钠溶液;②氯化钡溶液;③氢氧化钠溶液,则加入试剂的顺序a.②③① b.①②③ c.③②① d.③①②
(3)除杂过程中,加入
 溶液的目的是
溶液的目的是(4)步骤④判断加入的盐酸“适量”的方法是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐1】硫酸铵一种优良的氮肥,适用于各种土壤和作物,硫酸铵还可用于纺织、皮革、医药等方面。某化工厂以硫酸钙为原料制备硫酸铵,其工艺流程如下:

(1)X为___________ ,操作a名称为___________ 。NH3是工业制硝酸的重要原料,写出氨的催化氧化反应的化学方程式___________ 。
(2)煅烧CaCO3生成生石灰和CO2的反应为___________ 反应(填“吸热”或“放热”),欲加快该反应速率可采取的措施为___________ (写出一种即可)。
(3)上述流程中,可以循环使用的物质有___________ (写化学式)。
(4)从滤液中获得(NH4)2SO4晶体,必要的操作步骤是蒸发浓缩、___________ 、过滤等。
(5)写出利用该流程制备(NH4)2SO4的总化学方程式:___________ 。

(1)X为
(2)煅烧CaCO3生成生石灰和CO2的反应为
(3)上述流程中,可以循环使用的物质有
(4)从滤液中获得(NH4)2SO4晶体,必要的操作步骤是蒸发浓缩、
(5)写出利用该流程制备(NH4)2SO4的总化学方程式:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】某混合物A含有KAl(SO4)2、Al2O3和Fe2O3,在一定条件下可实现下图所示的物质之间的变化:

据此回答下列问题:
(1)I、II、IV四步中对于溶液和沉淀的分离采取的方法是_________ ;获得沉淀后,要对沉淀进行洗涤,请简述洗涤沉淀的操作是______________________________________ 。
(2)根据上述框图反应关系,写出下列B、E所含物质的化学式并回答相关问题:
固体B_______ ;溶液液E_______ ;沉淀D的重要用途是__________________ ;KAl(SO4)2 的重要用途是_____________________________ 。
(3)写出写出①、②、③三个反应的离子方程式:①______ ;②______ ;③______ 。

据此回答下列问题:
(1)I、II、IV四步中对于溶液和沉淀的分离采取的方法是
(2)根据上述框图反应关系,写出下列B、E所含物质的化学式并回答相关问题:
固体B
(3)写出写出①、②、③三个反应的离子方程式:①
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐3】回答下列问题。
(1)从硝酸钾、少量氯化钠和不溶性杂质(泥沙)的混合物中得到硝酸钾的流程如图:
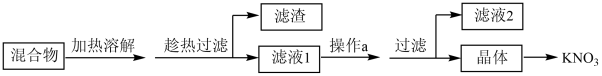
①结合如表分析,趁热过滤的原因是_______ 。
②操作a的名称是_______ 。
③滤液2的溶质是_______ 。
(2)A-D为初中化学常见物质,A、D为金属,在常温下通过如图所示转化可获取硝酸钾。回答下列问题。
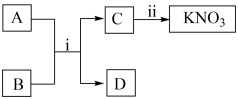
①反应i能发生的原因是。_______ 。
②若D为银白色贵重金属,则反应i的化学方程式是_______ ,基本反应类型是_______ 。
③一步实现反应ii,能否加入氯化钾?判断并说明理由_______ 。
(1)从硝酸钾、少量氯化钠和不溶性杂质(泥沙)的混合物中得到硝酸钾的流程如图:

①结合如表分析,趁热过滤的原因是
| 温度 | 0 | 20 | 40 | 60 | 80 | |
| 溶解度 | NaCl | 35.7 | 36.0 | 36.6 | 37.3 | 38.4 |
| KNO3 | 13.3 | 31.6 | 63.9 | 110 | 169 | |
②操作a的名称是
③滤液2的溶质是
(2)A-D为初中化学常见物质,A、D为金属,在常温下通过如图所示转化可获取硝酸钾。回答下列问题。

①反应i能发生的原因是。
②若D为银白色贵重金属,则反应i的化学方程式是
③一步实现反应ii,能否加入氯化钾?判断并说明理由
您最近一年使用:0次



