下列有关热化学方程式书写及对应表述均正确的是
| A.浓H2SO4与0.1 mol·L-1NaOH反应:H+(aq)+OH-(aq)===H2O(l) ΔH=-57.3 kJ·mol-1 |
| B.密闭容器中,9.6 g硫粉与11.2 g铁粉混合加热充分反应,放出19.12 kJ热量。则Fe(s)+S(s)===FeS(s) ΔH=-95.6 kJ·mol-1 |
| C.已知1 mol氢气完全燃烧生成液态水所放出的热量为285.5 kJ,则水分解的热化学方程式:2H2O(l)===2H2(g)+O2(g) ΔH=+285.5 kJ·mol-1 |
| D.已知2C(s)+O2(g)===2CO(g) ΔH=-221 kJ·mol-1,则可知C的燃烧热ΔH=-110.5 kJ·mol-1 |
更新时间:2018-01-27 10:33:50
|
相似题推荐
单选题
|
适中
(0.64)
【推荐1】工业制氢气的一个重要反应是: 已知在25℃时:
已知在25℃时: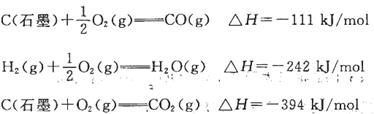
则2 5℃时1 mol CO与水蒸气作用转化为氢气和二氧化碳反应△H为
 已知在25℃时:
已知在25℃时: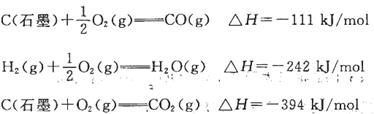
则2 5℃时1 mol CO与水蒸气作用转化为氢气和二氧化碳反应△H为
| A.+41.kJ/mol | B.-41kJ/mol | C.283kJ/mol | D.-131kJ/mol |
您最近半年使用:0次
单选题
|
适中
(0.64)
【推荐2】已知:①2CO(g)+O2(g)===2CO2(g) ΔH=-568 kJ·mol-1
②H2(g)+1/2O2(g)===H2O(g)ΔH=-248 kJ·mol-1
已知CO和H2的混合物1 mol在氧气中充分燃烧放出的热量272 kJ,则该混合气体中CO和氢气的物质的量的比值为
②H2(g)+1/2O2(g)===H2O(g)ΔH=-248 kJ·mol-1
已知CO和H2的混合物1 mol在氧气中充分燃烧放出的热量272 kJ,则该混合气体中CO和氢气的物质的量的比值为
| A.1∶1 | B.3∶37 |
| C.2∶1 | D.3∶2 |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐1】N2可以与O2化合生成NO,是自然界固氮的重要方式之一、下图所示是以1mol N2和1mol O2,作为反应物的相应能量变化。判断下列说法不正确的是


| A.上图所示的反应中转移电子的物质的量为4 mol |
| B.完全断开1mol NO中的化学键需吸收1264kJ能量 |
| C.该反应中产物所具有的总能量高于反应物所具有的总能量 |
| D.NO分解的热化学方程式为2NO(g)=N2(g) +O2(g) △H=-180kJ·mol-1 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】实验测得:101kPa时,1molH2完全燃烧生成液态水,放出285.8kJ的热量;1molCH4完全燃烧生成液态水和CO2,放出890.3kJ的热量。下列热化学方程式书写正确的是
| A.CH4(g)+2O2(g)=CO2(g)+2H2O(g) ΔH=−890.3kJ·mol−1 |
| B.CH4(g)+2O2(g)=CO2(g)+2H2O(l) ΔH=890.3kJ·mol−1 |
| C.H2(g)+1/2O2(g)=H2O(g) ΔH=−285.8kJ·mol−1 |
| D.2H2(g)+O2(g)=2H2O(l) ΔH=−571.6kJ·mol−1 |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐1】下列关于中和热的叙述中正确的是。
| A.在稀溶液中,所有酸和碱反应的中和热都相等 |
| B.在稀溶液中,强酸和强碱反应的中和热都相等 |
| C.在稀溶液中,1 mol酸和1 mol碱反应放出的热量都相等 |
| D.将浓硫酸滴入氢氧化钠溶液中刚好生成1 mol水时,产生的热量即为中和热 |
您最近半年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】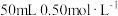 盐酸与
盐酸与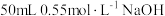 溶液进行中和反应,通过测定反应过程中所放出的热量可计算中和热,下列说法错误的是
溶液进行中和反应,通过测定反应过程中所放出的热量可计算中和热,下列说法错误的是
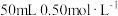 盐酸与
盐酸与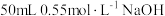 溶液进行中和反应,通过测定反应过程中所放出的热量可计算中和热,下列说法错误的是
溶液进行中和反应,通过测定反应过程中所放出的热量可计算中和热,下列说法错误的是| A.为防止混合溶液时溅出产生误差,混合时速度要慢 |
B.玻璃搅拌器材料若用铜代替,则测得的 会偏大 会偏大 |
C.用相同浓度、相同体积的醋酸溶液代替盐酸进行上述实验,测得的 会偏大 会偏大 |
D.为了保证盐酸完全被中和,采用稍过量的 溶液 溶液 |
您最近半年使用:0次
【推荐1】下列有关热化学方程式的表示及说法正确的是
A.已知  ,则氢气的燃烧热241.8 kJ/mol ,则氢气的燃烧热241.8 kJ/mol |
| B.25℃、101 kPa时,1 mol S和2 mol S的燃烧热不相等 |
C.含20.0g NaOH的稀溶液与稀硫酸完全中和,放出28.7 kJ的热量,则表示该反应中和热的热化学方程式为: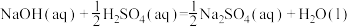 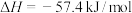 |
D.已知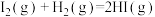  , ,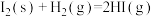  ,则 ,则 |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列各组热化学方程式中ΔH前者大于后者的是 ( )
①C(s)+O2(g)=CO2(g) ΔH1;C(s)+1/2O2(g)=CO(g) ΔH2。
②S(s)+O2(g)=SO2(g) ΔH3;S(g)+O2(g)=SO2(g) ΔH4。
③H2(g)+1/2O2(g)=H2O(g) ΔH5 ;2H2(g)+O2(g)=2H2O(g)ΔH6。
①C(s)+O2(g)=CO2(g) ΔH1;C(s)+1/2O2(g)=CO(g) ΔH2。
②S(s)+O2(g)=SO2(g) ΔH3;S(g)+O2(g)=SO2(g) ΔH4。
③H2(g)+1/2O2(g)=H2O(g) ΔH5 ;2H2(g)+O2(g)=2H2O(g)ΔH6。
| A.① | B.② | C.②③ | D.①②③ |
您最近半年使用:0次

 CO(g)+H2(g)
CO(g)+H2(g)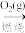 CO2(g)+H2O(g);途径b:C(s)
CO2(g)+H2O(g);途径b:C(s) 完全燃烧生成
完全燃烧生成 与水蒸气时放出802kJ的能量,根据下表的键能(断开1mol化学键或形成1mol化学键时吸收或放出的能量叫键能)数据,则x的数值为
与水蒸气时放出802kJ的能量,根据下表的键能(断开1mol化学键或形成1mol化学键时吸收或放出的能量叫键能)数据,则x的数值为

 )
)

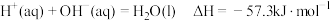
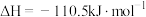
 的能量比
的能量比 的能量高
的能量高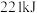
 水时,放出的热量为
水时,放出的热量为
 的
的 与
与 固体反应,放出的热量为
固体反应,放出的热量为
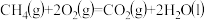
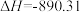 kJ·mol-1
kJ·mol-1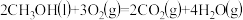
 kJ·mol-1
kJ·mol-1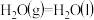
 kJ·mol-1
kJ·mol-1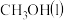 的燃烧热
的燃烧热
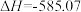 kJ·mol-1
kJ·mol-1 和
和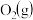 不能形成燃料电池
不能形成燃料电池

