元素在周期表中的位置,反映了元素的原子结构和元素的性质,下图是元素周期表的一部分。
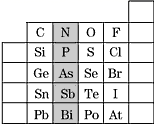
(1)上图中元素N在元素周期表中的位置为_________________ ,根据元素周期律,请预测H3AsO4、H3PO4的酸性强弱:H3AsO4________ H3PO4(填“强于”或“弱于”)。
(2)上图中元素O、S、Se的氢化物的沸点由高到低为:________>________>________。(用化学式填写)_____________
(3)写出S2-的离子结构示意图为______________ ;判断表中Bi和Te两种元素的金属性强弱:Bi________ Te(填“<”或“>”或“=”)。
(4)Br2具有较强的氧化性,SO2具有较强的还原性,请写出将SO2气体通入溴水中反应的离子方程式:________________________________ 。

(1)上图中元素N在元素周期表中的位置为
(2)上图中元素O、S、Se的氢化物的沸点由高到低为:________>________>________。(用化学式填写)
(3)写出S2-的离子结构示意图为
(4)Br2具有较强的氧化性,SO2具有较强的还原性,请写出将SO2气体通入溴水中反应的离子方程式:
更新时间:2018-11-16 00:52:03
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】向盛有硫酸铜水溶液的试管里加入氨水,首先形成蓝色沉淀,继续添加氨水,沉淀溶解病得到深蓝色的透明液体;若向试管中加入一定量乙醇,析出深蓝色晶体。结合有关知识,回答下列问题:
(1)Cu、N、O、S元素第一电离能由大到小的顺序是_______ (填元素符号);蓝色沉淀溶解时发生反应的离子方程式是________________ 。
(2)请解释加入乙醇后析出晶体的原因______________ 。
(3)SO42-的空间构型是_____________ ,其中S原子的杂化轨道类型是___________ 。
(4)NH3、H2O分子中,键角的大小顺序为_______ (用分子式表示);NH3极易溶于H2O的原因,除了两种分子都是极性分子外,还因为_______________ 。
(5)Cu和O能形成一种化合物,其晶胞结构如图所示,则R所表示微粒的价电子排布式为_____ ;若相邻的两不同微粒间的距离为a cm,设阿伏伽德罗常数的数值为NA,则该晶体的密度为_______ (用含a、NA的代数式表示)g/cm3。
(1)Cu、N、O、S元素第一电离能由大到小的顺序是
(2)请解释加入乙醇后析出晶体的原因
(3)SO42-的空间构型是
(4)NH3、H2O分子中,键角的大小顺序为
(5)Cu和O能形成一种化合物,其晶胞结构如图所示,则R所表示微粒的价电子排布式为

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】(1)锡元素可形成白锡、灰锡、脆锡三种单质。研究灰锡晶体的结构最常用的仪器是:_____ 。
(2)某气态团簇分子结构如图所示,每个原子都属于这个分子所有,则该气态团簇分子的分子式为______ 。

(3)如图为20个碳原子组成的空心笼状分子 C20,该笼状结构是由许多正五边形构成如图。C20分子中每个碳原子只跟相邻的3个碳原子形成化学键(欧拉定理:面数=2+棱边数-顶点数),则:C20分子共有___ 个正五边形,共有_______ 条棱边。

(4)Ni与Al形成的一种合金可用于铸造飞机发动机叶片,其晶胞结构如图所示,该合金的化学式为____ 。

(2)某气态团簇分子结构如图所示,每个原子都属于这个分子所有,则该气态团簇分子的分子式为

(3)如图为20个碳原子组成的空心笼状分子 C20,该笼状结构是由许多正五边形构成如图。C20分子中每个碳原子只跟相邻的3个碳原子形成化学键(欧拉定理:面数=2+棱边数-顶点数),则:C20分子共有

(4)Ni与Al形成的一种合金可用于铸造飞机发动机叶片,其晶胞结构如图所示,该合金的化学式为

您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】合成尿素的反应为:2NH3(g)+CO2(g) CO(NH2)2(s)+H2O(g)+Q(Q>0)。一定条件下,在10 L的恒容密闭容器中,充入2 mol NH3和1 mol CO2,反应经5 min后达到平衡,测得容器中气体的密度为4.2 g/L。
CO(NH2)2(s)+H2O(g)+Q(Q>0)。一定条件下,在10 L的恒容密闭容器中,充入2 mol NH3和1 mol CO2,反应经5 min后达到平衡,测得容器中气体的密度为4.2 g/L。
完成下列填空:
(1).平均反应速率υ(NH3)=____________ 。
(2).下列描述中能说明上述反应已达平衡的是_________ (填序号)。
a.2υ正(NH3)=υ逆(H2O)
b.气体的平均相对分子质量不随时间而变化
c.NH3和CO2的比例保持不变
d.气体的压强不再发生变化
(3).为提高尿素的产率,工业上用该反应生产尿素时,合适的反应条件是_______ (填序号)。
a.200℃ b.800℃ c.101 kPa d.24000 kPa
(4).上述反应所涉及的4种元素中,原子半径从大到小的排列顺序为_________ ;原子核外有2个未成对电子的元素是________ ;反应所涉及的化合物中仅有一种是非极性分子,其电子式为_____________ 。
(5).下列能用于判断氮、碳两种元素非金属性强弱的是________ (填序号)。
a.气态氢化物沸点 b.最高价氧化物对应水化物酸性强弱
c.HCN中,碳为+2价 d.单质晶体类型
 CO(NH2)2(s)+H2O(g)+Q(Q>0)。一定条件下,在10 L的恒容密闭容器中,充入2 mol NH3和1 mol CO2,反应经5 min后达到平衡,测得容器中气体的密度为4.2 g/L。
CO(NH2)2(s)+H2O(g)+Q(Q>0)。一定条件下,在10 L的恒容密闭容器中,充入2 mol NH3和1 mol CO2,反应经5 min后达到平衡,测得容器中气体的密度为4.2 g/L。完成下列填空:
(1).平均反应速率υ(NH3)=
(2).下列描述中能说明上述反应已达平衡的是
a.2υ正(NH3)=υ逆(H2O)
b.气体的平均相对分子质量不随时间而变化
c.NH3和CO2的比例保持不变
d.气体的压强不再发生变化
(3).为提高尿素的产率,工业上用该反应生产尿素时,合适的反应条件是
a.200℃ b.800℃ c.101 kPa d.24000 kPa
(4).上述反应所涉及的4种元素中,原子半径从大到小的排列顺序为
(5).下列能用于判断氮、碳两种元素非金属性强弱的是
a.气态氢化物沸点 b.最高价氧化物对应水化物酸性强弱
c.HCN中,碳为+2价 d.单质晶体类型
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】元素周期表被认为是“科学共同的语言”,它的发现使化学学习和研究变得有规律可循。其简洁有序的背后,是众多科学家艰苦奋斗的结果。下图是元素周期表的一部分。请按要求回答下列问题:

(1)317年左右,东晋炼丹家葛洪在炼丹时分离出了元素砷。砷在周期表中的位置是______ 。我国“天宫”空间站的核心舱“天和”选择了高效柔性砷化镓(GaAs)薄膜太阳能电池来供电。原子半径:Ga______ As(填“>”或“<”)。
(2)1787年,法国化学家拉瓦锡首次发现硅存在于岩石中。碳和硅元素简单气态氢化物稳定性更强的是______ 。碳的最高价氧化物的电子式为______ 。
(3)1817年瑞典化学家贝采利乌斯发现硒元素。硒元素和溴元素最高价氧化物水化物酸性较强的是______ (填化学式)。
(4)1825年,丹麦化学家奥斯特首次分离出了铝的单质。往 溶液中滴入过量氨水,写出该反应的离子方程式
溶液中滴入过量氨水,写出该反应的离子方程式______ 。
(5)经研究,发现可能存在的第119号元素,有人称“类钫”,位于元素周期表第八周期IA族。有关“类钫”的预测正确的是______。

(1)317年左右,东晋炼丹家葛洪在炼丹时分离出了元素砷。砷在周期表中的位置是
(2)1787年,法国化学家拉瓦锡首次发现硅存在于岩石中。碳和硅元素简单气态氢化物稳定性更强的是
(3)1817年瑞典化学家贝采利乌斯发现硒元素。硒元素和溴元素最高价氧化物水化物酸性较强的是
(4)1825年,丹麦化学家奥斯特首次分离出了铝的单质。往
 溶液中滴入过量氨水,写出该反应的离子方程式
溶液中滴入过量氨水,写出该反应的离子方程式(5)经研究,发现可能存在的第119号元素,有人称“类钫”,位于元素周期表第八周期IA族。有关“类钫”的预测正确的是______。
| A.“类钫”在化合物中显+1价 | B.“类钫”单质具有强氧化性 |
| C.“类钫”最高价氧化物对应的水化物为弱碱 | D.“类钫”单质能与冷水剧烈反应 |
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】元素的“价—类”二维图是学习元素及其化合物的重要工具。如图是部分硫及其化合物的“价—类”二维图。根据图示回答下列问题:

(1)X的化学式为____ 。
(2)根据“价—类”二维图预测,SO2与氯水反应表现____ 性,反应的化学方程式为____ 。
(3)下列物质与SO2反应,SO2能表现出氧化性的是___ (填序号)。
a.H2O b.H2S溶液 c.Na2SO3溶液
(4)SO2与CO2类似,可以和NaOH溶液反应,反应的化学方程式为____ 。
(5)下列事实能说明硫的非金属性弱于氯的是____ (填序号)。
a.稳定性:H2S<HCl
b.酸性:H2S<HCl
c.酸性:H2SO4<HClO4
d.往氢硫酸溶液中通入Cl2,产生淡黄色沉淀:H2S+Cl2=2HCl+S↓

(1)X的化学式为
(2)根据“价—类”二维图预测,SO2与氯水反应表现
(3)下列物质与SO2反应,SO2能表现出氧化性的是
a.H2O b.H2S溶液 c.Na2SO3溶液
(4)SO2与CO2类似,可以和NaOH溶液反应,反应的化学方程式为
(5)下列事实能说明硫的非金属性弱于氯的是
a.稳定性:H2S<HCl
b.酸性:H2S<HCl
c.酸性:H2SO4<HClO4
d.往氢硫酸溶液中通入Cl2,产生淡黄色沉淀:H2S+Cl2=2HCl+S↓
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】研究物质的微观结构,有助于人们理解物质变化的本质。请回答下列问题。
(1)C、Si、N元素的电负性由大到小的顺序是___________________________ 。C60和金刚石都是碳的同素异形体,金刚石熔点高于C60熔点,原因是__________________________________________________________________________ 。
(2)A、B均为短周期金属元素。依据下表数据和已学知识,
写出B原子的电子排布式:___________________________ 。
(3)过渡金属离子与水分子形成的配合物是否有颜色,与其d轨道电子排布有关。一般地,为d0或d10排布时,无颜色;为d1~d9排布时,有颜色,如[Co(H2O) 6]2+显粉红色。据此判断,[Mn(H2O) 6]]2+_______ (填“无”或“有”)颜色。
(4)利用CO可以合成化工原料COCl2、络合物Fe(CO)5等。
①已知COCl2分子的结构式为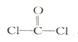 ,则 COCl2分子内含
,则 COCl2分子内含_______ (填标号)。
A.4个 键
键
B.2个 键、2个
键、2个 键
键
C.2个 键、1个
键、1个 键
键
D.3个 键、1个
键、1个 键
键
②Fe(CO)5在一定条件下发生分解反应:Fe(CO)5=Fe(s)+5CO,反应过程中,断裂的化学键只有配位键,形成的化学键是___________ 。
(1)C、Si、N元素的电负性由大到小的顺序是
(2)A、B均为短周期金属元素。依据下表数据和已学知识,
| 电离能/KJ·mol-1 | I1 | I2 | I3 | I4 |
| A | 932 | 1821 | 15390 | 21771 |
| B | 738 | 1451 | 7733 | 10540 |
写出B原子的电子排布式:
(3)过渡金属离子与水分子形成的配合物是否有颜色,与其d轨道电子排布有关。一般地,为d0或d10排布时,无颜色;为d1~d9排布时,有颜色,如[Co(H2O) 6]2+显粉红色。据此判断,[Mn(H2O) 6]]2+
(4)利用CO可以合成化工原料COCl2、络合物Fe(CO)5等。
①已知COCl2分子的结构式为
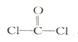 ,则 COCl2分子内含
,则 COCl2分子内含A.4个
 键
键B.2个
 键、2个
键、2个 键
键C.2个
 键、1个
键、1个 键
键D.3个
 键、1个
键、1个 键
键②Fe(CO)5在一定条件下发生分解反应:Fe(CO)5=Fe(s)+5CO,反应过程中,断裂的化学键只有配位键,形成的化学键是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】无机物及有机物在工农业生产和人类生活中都有着重要的应用。
(1)比较离子半径大小:Li+___________ H一(选填“>"、“<”或“=”)。
(2)LiAlH4中电负性最大的元素是___________ ,它与水反应生成的单质气体为___________ 。
(3)LiCl溶液显酸性,用离子方程式说明原因___________ 。
(4)泡沫灭火器的灭火原理:___________ (用离子方程式说明)。
(5)如图所示,已知B可用作燃料,则A的官能团名称为___________ ;A生成B的有机反应类型为___________ 。

(1)比较离子半径大小:Li+
(2)LiAlH4中电负性最大的元素是
(3)LiCl溶液显酸性,用离子方程式说明原因
(4)泡沫灭火器的灭火原理:
(5)如图所示,已知B可用作燃料,则A的官能团名称为

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】C和Si元素在化学中占有极其重要的地位。
(1)写出Si的基态原子核外电子排布式___________ 。C、Si和O元素的电负性由大至小的顺序为___________ 。
(2)SiC的晶体结构与晶体硅相似,其中C原子的杂化方式为___________ ,微粒间存在的作用力是___________ ;lmol硅晶体中有___________ molSi-Si键。
(3)氧化物MO的电子总数与SiC的相等,则M为___________ (填元素符号)。MO是优良的耐高温材料,其晶体结构与NaCl晶体相似。MO的熔点比CaO的高,其原因是___________ 。
(4)C、Si为同一主族的元素,CO2和SiO2化学式相似,但结构和性质有很大不同。CO2中C与O原子间形成σ键和π键,SiO2中Si与О原子间不形成上述π键。从原子半径大小的角度分析,为何C、O原子间能形成,而Si、O原子间不能形成上述π键?___________ 。
(1)写出Si的基态原子核外电子排布式
(2)SiC的晶体结构与晶体硅相似,其中C原子的杂化方式为
(3)氧化物MO的电子总数与SiC的相等,则M为
(4)C、Si为同一主族的元素,CO2和SiO2化学式相似,但结构和性质有很大不同。CO2中C与O原子间形成σ键和π键,SiO2中Si与О原子间不形成上述π键。从原子半径大小的角度分析,为何C、O原子间能形成,而Si、O原子间不能形成上述π键?
您最近一年使用:0次



