某同学在实验室以下图所示的仪器和药品,进行氯气和铜粉反应的实验(部分夹持装置已省略)。请按要求回答下列问题:
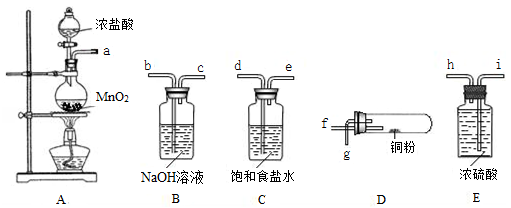
(1)装置A烧瓶中发生反应的化学方程式为_____________________________________ 。
(2)按气流方向连接各仪器接口的顺序是(填接口字母):
a→______________________ 。
(3)装置B中发生反应的离子方程式为________________________ ,装置C中饱和食盐水的作用是__________________________________ 。
(4)加热装置D时,铜粉发生反应的化学方程式为____________________________ 。
(5)比较下列两组实验,你认为下列说法正确的是_____ (填序号)。
实验①:将足量的二氧化锰与含0.4molHCl的浓盐酸反应。
实验②:将8.7g二氧化锰与足量的浓盐酸反应。
A.①产生的氯气多 B.产生的氯气一样多
C.②产生的氯气多 D.无法判断

(1)装置A烧瓶中发生反应的化学方程式为
(2)按气流方向连接各仪器接口的顺序是(填接口字母):
a→
(3)装置B中发生反应的离子方程式为
(4)加热装置D时,铜粉发生反应的化学方程式为
(5)比较下列两组实验,你认为下列说法正确的是
实验①:将足量的二氧化锰与含0.4molHCl的浓盐酸反应。
实验②:将8.7g二氧化锰与足量的浓盐酸反应。
A.①产生的氯气多 B.产生的氯气一样多
C.②产生的氯气多 D.无法判断
更新时间:2018-11-26 11:52:09
|
相似题推荐
解答题-实验探究题
|
较难
(0.4)
名校
解题方法
【推荐1】次氯酸溶液是常用的消毒剂和漂白剂。某学习小组根据需要欲制备次氯酸溶液。
资料1:常温常压下,Cl2O为棕黄色气体,沸点为3.8 ℃,42 ℃以上会分解生成Cl2和O2,Cl2O易溶于水并与水立即反应生成 HClO。
资料2:将氯气和空气(不参与反应)按体积比1:3混合通入潮湿的碳酸钠中发生反应2Cl2+2Na2CO3+H2O=Cl2O+2NaCl+2NaHCO3,用水吸收Cl2O(不含Cl2)制得次氯酸溶液。
该学习小组同学用以下装置制备次氯酸溶液。
(1)请写出装置B的玻璃容器名称_________ 。
(2)各装置的连接顺序为____ →______ →_____ →_____ →E。
(3)装置A中反应的离子方程式是________ 。
(4)反应过程中,装置B需放在冷水中,其目的是________ 。
(5)装置E采用棕色烧瓶是因为________ 。
(6)已知次氯酸可被H2O2、FeCl2等物质还原成Cl-。测定E中次氯酸溶液的物质的量浓度的实验方案为:用酸式滴定管准确量取20.00 mL次氯酸溶液,加入足量的_______ 溶液,再加入足量的_____ 溶液,过滤,洗涤,真空干燥,称量沉淀的质量。(可选用的试剂:H2O2溶液、FeCl2溶液、AgNO3溶液。)
(7)若装置B中生成的Cl2O气体有20%滞留在E前各装置中,其余均溶于装置E的水中,装置E所得500 mL次氯酸溶液浓度为0.8 mol/L,则至少需要碳酸钠的质量为______ g。
资料1:常温常压下,Cl2O为棕黄色气体,沸点为3.8 ℃,42 ℃以上会分解生成Cl2和O2,Cl2O易溶于水并与水立即反应生成 HClO。
资料2:将氯气和空气(不参与反应)按体积比1:3混合通入潮湿的碳酸钠中发生反应2Cl2+2Na2CO3+H2O=Cl2O+2NaCl+2NaHCO3,用水吸收Cl2O(不含Cl2)制得次氯酸溶液。
该学习小组同学用以下装置制备次氯酸溶液。

(1)请写出装置B的玻璃容器名称
(2)各装置的连接顺序为
(3)装置A中反应的离子方程式是
(4)反应过程中,装置B需放在冷水中,其目的是
(5)装置E采用棕色烧瓶是因为
(6)已知次氯酸可被H2O2、FeCl2等物质还原成Cl-。测定E中次氯酸溶液的物质的量浓度的实验方案为:用酸式滴定管准确量取20.00 mL次氯酸溶液,加入足量的
(7)若装置B中生成的Cl2O气体有20%滞留在E前各装置中,其余均溶于装置E的水中,装置E所得500 mL次氯酸溶液浓度为0.8 mol/L,则至少需要碳酸钠的质量为
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
解题方法
【推荐2】氯可形成多种含氧酸盐,广泛应用于杀菌、消毒及化工领域。实验室中利用如图装置(部分装置省略)制备 和NaClO,并探究其性质。
和NaClO,并探究其性质。

(1)装置A中发生反应的化学方程式是___________ 。
(2)装置B的作用是___________ 。
(3)反应结束后,取出C中试管,经冷却结晶、___________ 、干燥得到 晶体,生成
晶体,生成 的离子方程式为
的离子方程式为___________ 。
(4)比较C、D的反应条件,可以得出的结论是___________ 。
(5)取少量NaClO和 溶液分别置于1号和2号试管中,滴加中性KI溶液,1号试管溶液变为棕色,加入
溶液分别置于1号和2号试管中,滴加中性KI溶液,1号试管溶液变为棕色,加入 振荡,静置后
振荡,静置后 层显紫色,2号试管溶液颜色不变,该条件下NaClO的氧化能力
层显紫色,2号试管溶液颜色不变,该条件下NaClO的氧化能力___________  (填“大于”或“小于”或“等于”)的。
(填“大于”或“小于”或“等于”)的。
(6)工业上利用D装置中的反应原理生产“84消毒液”,若向100kg16%的NaOH溶液中通入 恰好完全反应,计算理论上制得“84”消毒液中有效成分的质量
恰好完全反应,计算理论上制得“84”消毒液中有效成分的质量___________ 。(写出计算过程)
 和NaClO,并探究其性质。
和NaClO,并探究其性质。
(1)装置A中发生反应的化学方程式是
(2)装置B的作用是
(3)反应结束后,取出C中试管,经冷却结晶、
 晶体,生成
晶体,生成 的离子方程式为
的离子方程式为(4)比较C、D的反应条件,可以得出的结论是
(5)取少量NaClO和
 溶液分别置于1号和2号试管中,滴加中性KI溶液,1号试管溶液变为棕色,加入
溶液分别置于1号和2号试管中,滴加中性KI溶液,1号试管溶液变为棕色,加入 振荡,静置后
振荡,静置后 层显紫色,2号试管溶液颜色不变,该条件下NaClO的氧化能力
层显紫色,2号试管溶液颜色不变,该条件下NaClO的氧化能力 (填“大于”或“小于”或“等于”)的。
(填“大于”或“小于”或“等于”)的。(6)工业上利用D装置中的反应原理生产“84消毒液”,若向100kg16%的NaOH溶液中通入
 恰好完全反应,计算理论上制得“84”消毒液中有效成分的质量
恰好完全反应,计算理论上制得“84”消毒液中有效成分的质量
您最近一年使用:0次
【推荐3】氯化苄(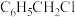 )是一种重要的有机化学原料。工业上采用甲苯与干燥氯气在光照条件下反应合成氯化苄。
)是一种重要的有机化学原料。工业上采用甲苯与干燥氯气在光照条件下反应合成氯化苄。
(1)写出实验室制取氯气的化学方程式_______ 。
(2)用下列方法分析氯化苄粗产品的纯度。
步骤Ⅰ:称取5.11g样品于烧瓶中,加入200.00 mL 4 mol/L氢氧化钠溶液共热,冷却至室温。加入200.00 mL 4 mol/L硝酸,一段时间后,将烧瓶中的溶液全部转移至2500mL的容量瓶中,加水定容。
步骤Ⅱ:从容量瓶中各取25.00mL溶液于三只锥形瓶中,各加入25.00mL 0.2000 moL/L硝酸银溶液。
步骤Ⅲ:以硫酸铁铵作指示剂,用0.2000 mol/L 溶液分别滴定剩余的硝酸银,所得滴定数据如下表。
溶液分别滴定剩余的硝酸银,所得滴定数据如下表。
①加入硝酸的目的是_______ 。
②使用滴定管过程中所涉及下列操作的先后顺序是_______ (填字母)。
a.排除滴定管尖嘴处的气泡
b.检查滴定管是否漏液
c.用待装液润洗滴定管
③在步骤操作Ⅲ中,判断达到滴定终点的现象是_______ 。
(3)该样品中氯化苄的质量分数(写出计算过程)_______ 。
(4)上述测定结果常高于氯化苄中氯元素的理论含量,原因是_______ 。
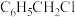 )是一种重要的有机化学原料。工业上采用甲苯与干燥氯气在光照条件下反应合成氯化苄。
)是一种重要的有机化学原料。工业上采用甲苯与干燥氯气在光照条件下反应合成氯化苄。(1)写出实验室制取氯气的化学方程式
(2)用下列方法分析氯化苄粗产品的纯度。
步骤Ⅰ:称取5.11g样品于烧瓶中,加入200.00 mL 4 mol/L氢氧化钠溶液共热,冷却至室温。加入200.00 mL 4 mol/L硝酸,一段时间后,将烧瓶中的溶液全部转移至2500mL的容量瓶中,加水定容。
步骤Ⅱ:从容量瓶中各取25.00mL溶液于三只锥形瓶中,各加入25.00mL 0.2000 moL/L硝酸银溶液。
步骤Ⅲ:以硫酸铁铵作指示剂,用0.2000 mol/L
 溶液分别滴定剩余的硝酸银,所得滴定数据如下表。
溶液分别滴定剩余的硝酸银,所得滴定数据如下表。| 滴定序号 |  标准溶液 标准溶液 | |
| 滴定管起点读数/mL | 滴定管终点读数/mL | |
| 1 | 0.40 | 10.38 |
| 2 | 0.30 | 10.32 |
| 3 | 0.20 | 10.41 |
②使用滴定管过程中所涉及下列操作的先后顺序是
a.排除滴定管尖嘴处的气泡
b.检查滴定管是否漏液
c.用待装液润洗滴定管
③在步骤操作Ⅲ中,判断达到滴定终点的现象是
(3)该样品中氯化苄的质量分数(写出计算过程)
(4)上述测定结果常高于氯化苄中氯元素的理论含量,原因是
您最近一年使用:0次



