已知FeS溶于盐酸中生成FeCl2和H2S气体。现将8.8g FeS固体置于200mL、2.0mol•L﹣1的盐酸中,以制备H2S气体。完全反应后假定溶液体积不变,试计算:
(1)收集到标准状况下H2S气体的体积_______ 。
(2)溶液中FeCl2的物质的量浓度_______ 。
(1)收集到标准状况下H2S气体的体积
(2)溶液中FeCl2的物质的量浓度
更新时间:2018-12-16 23:12:17
|
相似题推荐
填空题
|
较易
(0.85)
解题方法
【推荐1】图像分析是化学研究的一种重要的手段。某同学分析某无色透明溶液,已知其中可能含有Fe3+、Mg2+、Cu2+、Al3+、NH ,加入淡黄色粉末(过氧化钠)并加热,产生沉淀或气体的物质的量与淡黄色粉末的物质的量的关系如图所示(假设产生的气体全部逸出)。请回答:
,加入淡黄色粉末(过氧化钠)并加热,产生沉淀或气体的物质的量与淡黄色粉末的物质的量的关系如图所示(假设产生的气体全部逸出)。请回答:
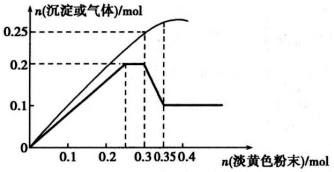
(1)根据图像所示,推测溶液中肯定有__ (写化学式)离子。
(2)过氧化钠物质的量在0.3~0.35mol时,粗的曲线出现下滑的现象,请用两个离子方程式解释该过程:__ 。
(3)溶液中Al3+、Mg2+、NH ,的物质的量之比为
,的物质的量之比为__ 。
 ,加入淡黄色粉末(过氧化钠)并加热,产生沉淀或气体的物质的量与淡黄色粉末的物质的量的关系如图所示(假设产生的气体全部逸出)。请回答:
,加入淡黄色粉末(过氧化钠)并加热,产生沉淀或气体的物质的量与淡黄色粉末的物质的量的关系如图所示(假设产生的气体全部逸出)。请回答:
(1)根据图像所示,推测溶液中肯定有
(2)过氧化钠物质的量在0.3~0.35mol时,粗的曲线出现下滑的现象,请用两个离子方程式解释该过程:
(3)溶液中Al3+、Mg2+、NH
 ,的物质的量之比为
,的物质的量之比为
您最近半年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】按要求完成下列题目:
(1)在标准状况下,0.2NA二氧化碳所占体积是_____________ ;
(2)将含有4mol氢原子的硫酸,配成1L的溶液,则溶质的物质的量浓度是__________ 。
(1)在标准状况下,0.2NA二氧化碳所占体积是
(2)将含有4mol氢原子的硫酸,配成1L的溶液,则溶质的物质的量浓度是
您最近半年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】(1)用洁净的烧杯取少量蒸馏水,用酒精灯加热至沸腾,向烧杯中逐滴加入饱和的FeCl3溶液,继续煮沸,待溶液呈红褐色停止加热。
①写出该反应方程式________________________________________ 。
②证明该分散系是胶体最简单的实验操作名称________________________ 。
(2)对于反应2CO+O2=2CO2,在标准状况下,4.48 L一氧化碳与足量的氧气发生反应,生成的二氧化碳分子个数是__________________ 。
(3)现有一种泉水样品,1.0 L这种泉水含有4.8×10-2 g Mg2+。那么,该泉水中Mg2+的物质的量浓度是_______________ ,含1.0 mol Mg2+的这种泉水的体积是_______________ 。
①写出该反应方程式
②证明该分散系是胶体最简单的实验操作名称
(2)对于反应2CO+O2=2CO2,在标准状况下,4.48 L一氧化碳与足量的氧气发生反应,生成的二氧化碳分子个数是
(3)现有一种泉水样品,1.0 L这种泉水含有4.8×10-2 g Mg2+。那么,该泉水中Mg2+的物质的量浓度是
您最近半年使用:0次
填空题
|
较易
(0.85)
【推荐2】如图为一“铁链”图案,小明在图案上分别写了H2、CO2、Na2O、NaCl、FeCl3五种物质,图中相连的两种物质均可归属为一类,相交部分A、B、C、D为其相应的分类依据代号。
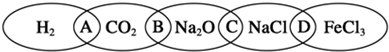
请回答下列问题:
(1)请将分类依据代号填入括号内_____________ 两种物质都不是电解质。
(2)用洁净的烧杯取少量蒸馏水,用酒精灯加热至沸腾,向烧杯中逐滴加入1 mol·L-1图中某物质M的水溶液,继续煮沸可制得一种红褐色液体。
①物质M的化学式为____________ 。
②证明所制得的红褐色液体是胶体的实验操作是__________________________________ 。
(3)下图是硫酸试剂瓶标签上的内容:

①该硫酸的物质的量浓度是_________________ mol·L-1。
②某化学兴趣小组进行硫酸性质的实验探究时,上述硫酸进行稀释的实验操作为___________ 。

请回答下列问题:
(1)请将分类依据代号填入括号内
(2)用洁净的烧杯取少量蒸馏水,用酒精灯加热至沸腾,向烧杯中逐滴加入1 mol·L-1图中某物质M的水溶液,继续煮沸可制得一种红褐色液体。
①物质M的化学式为
②证明所制得的红褐色液体是胶体的实验操作是
(3)下图是硫酸试剂瓶标签上的内容:

①该硫酸的物质的量浓度是
②某化学兴趣小组进行硫酸性质的实验探究时,上述硫酸进行稀释的实验操作为
您最近半年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】(1)配制2mol/L NaOH溶液250mL,在下列所叙述的操作中选择必要的操作,用序号写出操作顺序____________________________________________ .
A.在100mL烧杯中放入适量的水,溶解NaOH.
B.NaOH溶液冷却后,注入容量瓶
C.在托盘天平上放2张大小一样的纸,称取20.0g NaOH
D.用滴管加蒸馏水,使溶液凹液面和刻度相切,摇匀.
E.向容量瓶加蒸馏水,使溶液凹液面和刻度相切,摇匀.
F.在烧杯中放NaOH,用托盘天平称出20.0g NaOH.
G.把20g NaOH溶于250mL蒸馏水中.
H.NaOH溶液冷却后,沿玻璃棒注入250mL容量瓶
I.向容量瓶加蒸馏水,直至液面接近瓶颈刻度线1~2cm处
J.容量瓶用NaOH溶液润洗后使用
K.用蒸馏水洗涤烧杯、玻璃棒2~3次,并把洗涤液注入容量瓶,振荡
(2)0.1L 2mol/L MgCl2溶液与0.4L 1mol/L AlCl3溶液中Cl- 物质的量浓度比为________ 。
A.在100mL烧杯中放入适量的水,溶解NaOH.
B.NaOH溶液冷却后,注入容量瓶
C.在托盘天平上放2张大小一样的纸,称取20.0g NaOH
D.用滴管加蒸馏水,使溶液凹液面和刻度相切,摇匀.
E.向容量瓶加蒸馏水,使溶液凹液面和刻度相切,摇匀.
F.在烧杯中放NaOH,用托盘天平称出20.0g NaOH.
G.把20g NaOH溶于250mL蒸馏水中.
H.NaOH溶液冷却后,沿玻璃棒注入250mL容量瓶
I.向容量瓶加蒸馏水,直至液面接近瓶颈刻度线1~2cm处
J.容量瓶用NaOH溶液润洗后使用
K.用蒸馏水洗涤烧杯、玻璃棒2~3次,并把洗涤液注入容量瓶,振荡
(2)0.1L 2mol/L MgCl2溶液与0.4L 1mol/L AlCl3溶液中Cl- 物质的量浓度比为
您最近半年使用:0次



