利用相关知识填空.
(1)标准状况下11.2LNH3 中含______ 个氨分子,含______ mol 氢原子.
(2)等质量的SO2和SO3物质的量之比是_______ ;所含的氧原子个数之比是______ .
(3)4.8gCH4中所含氢原子数与______ g水所含氢原子数相等.
(4)12.4gNa2R含Na+0.4mol,则Na2R的摩尔质量为______ .
(5)标况下,一定量的N2与22.4LCO所含电子的物质的量相等,则N2的质量是______ .
(1)标准状况下11.2LNH3 中含
(2)等质量的SO2和SO3物质的量之比是
(3)4.8gCH4中所含氢原子数与
(4)12.4gNa2R含Na+0.4mol,则Na2R的摩尔质量为
(5)标况下,一定量的N2与22.4LCO所含电子的物质的量相等,则N2的质量是
更新时间:2019-10-01 16:49:18
|
相似题推荐
填空题
|
较易
(0.85)
名校
【推荐1】双原子分子构成的气体,其摩尔质量为M g/mol,该气体质量为m g,阿伏伽德罗常数为NA,则:
(1)气体的物质的量为__________ mol;
(2)该气体在标准状况下的体积为__________ L;
(3)该气体所含原子总数为__________ 个。
(1)气体的物质的量为
(2)该气体在标准状况下的体积为
(3)该气体所含原子总数为
您最近半年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】回答下列问题:
(1)0.25molCH4在标准状况下的体积为____ L,0.25molCH4的含有____ 个氢原子。
(2)同温同压下,等体积的O2和O3所含分子个数比为____ ,质量比为____ 。
(3)在9.5g某二价金属的氯化物中含有0.2molCl-,此氯化物的摩尔质量为____ ,该金属元素的相对原子质量为____ 。
(1)0.25molCH4在标准状况下的体积为
(2)同温同压下,等体积的O2和O3所含分子个数比为
(3)在9.5g某二价金属的氯化物中含有0.2molCl-,此氯化物的摩尔质量为
您最近半年使用:0次
填空题
|
较易
(0.85)
【推荐3】完成下列空白(设NA为阿伏加德罗常数的值,也可使用阿伏加德罗常数的近似值):
(1)4g H 2的物质的量是_______ mol;2molH2O中H个数为_______ ;在标准状况下, 2molO2占有的体积是 _______ L。
(2)18.6 g Na2R含0.6 mol Na+,则Na2R的摩尔质量为_______ 。
(3)22gCO2中的质子数为_______ ;物质的量为0.45mol的CO2和CO的混合气体,质量为18g,则CO2和CO的分子数之比为_______ 。
(1)4g H 2的物质的量是
(2)18.6 g Na2R含0.6 mol Na+,则Na2R的摩尔质量为
(3)22gCO2中的质子数为
您最近半年使用:0次
填空题
|
较易
(0.85)
【推荐1】计算
(1)19.2gSO2在标准状况下的体积为_______ L,其中含氧原子的物质的量为_______ mol,该气体在标准状况下的密度是_______ g∙L-1(保留两位有效数字)。
(2)0.5molH3PO4的质量是_______ g,含_______ 个氧原子。
(3)在标准状况下,将_______ LNH3溶于水得到500mL0.5mol∙L-1的氨水;配制100mL0.1mol∙L-1FeSO4溶液,需要用托盘天平称FeSO4∙7H2O_______ g。
(4)同温同压下,同体积的氨气(NH3)和硫化氢(H2S)气体的质量比为_______ ;氨气和硫化氢气体的密度比为_______ 。
(5)现有14.4gCO和CO2的混合气体,在标准状况下所占体积约为8.96L,求该混合气体的平均摩尔质量_______ 。
(1)19.2gSO2在标准状况下的体积为
(2)0.5molH3PO4的质量是
(3)在标准状况下,将
(4)同温同压下,同体积的氨气(NH3)和硫化氢(H2S)气体的质量比为
(5)现有14.4gCO和CO2的混合气体,在标准状况下所占体积约为8.96L,求该混合气体的平均摩尔质量
您最近半年使用:0次
填空题
|
较易
(0.85)
【推荐2】物质的量是学习化学的基础。
(1)14.4gCO和CO2的混合气体在标准状况下所占的体积为8.96L,其中CO的质量为___ 。
(2)市售浓H2SO4的质量分数为98%、密度为1.84g/cm3,其浓度为___ mol•L-1。
(3)19g某二价金属的氯化物ACl3中含有0.4molCl-离子,金属A的相对原子质量是___ 。
(4)根据反应14CuSO4+5FeS2+12H2O 7Cu2S+5FeSO4+12H2SO4,可知当有2.5molFeS2参加反应时,氧化产物的物质的量为
7Cu2S+5FeSO4+12H2SO4,可知当有2.5molFeS2参加反应时,氧化产物的物质的量为__ mol。
(1)14.4gCO和CO2的混合气体在标准状况下所占的体积为8.96L,其中CO的质量为
(2)市售浓H2SO4的质量分数为98%、密度为1.84g/cm3,其浓度为
(3)19g某二价金属的氯化物ACl3中含有0.4molCl-离子,金属A的相对原子质量是
(4)根据反应14CuSO4+5FeS2+12H2O
 7Cu2S+5FeSO4+12H2SO4,可知当有2.5molFeS2参加反应时,氧化产物的物质的量为
7Cu2S+5FeSO4+12H2SO4,可知当有2.5molFeS2参加反应时,氧化产物的物质的量为
您最近半年使用:0次
填空题
|
较易
(0.85)
【推荐1】回答下列问题
(1)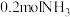 的质量为
的质量为___________ g,其中氢原子的物质的量为___________  。
。
(2)标准状态下, 由
由 和
和 组成的混合气体的质量为
组成的混合气体的质量为 ,则
,则 和
和 的物质的量之比是
的物质的量之比是___________ 。
(3) 某气体含有
某气体含有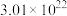 个分子,该气体的摩尔质量为
个分子,该气体的摩尔质量为___________ 。
(4)把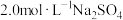 溶液和
溶液和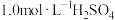 溶液等体积混合(假设混合后溶液的体积等于混合前两种溶液的体积之和),则
溶液等体积混合(假设混合后溶液的体积等于混合前两种溶液的体积之和),则 的物质的量浓度为
的物质的量浓度为___________  。
。
(1)
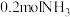 的质量为
的质量为 。
。(2)标准状态下,
 由
由 和
和 组成的混合气体的质量为
组成的混合气体的质量为 ,则
,则 和
和 的物质的量之比是
的物质的量之比是(3)
 某气体含有
某气体含有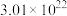 个分子,该气体的摩尔质量为
个分子,该气体的摩尔质量为(4)把
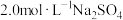 溶液和
溶液和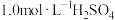 溶液等体积混合(假设混合后溶液的体积等于混合前两种溶液的体积之和),则
溶液等体积混合(假设混合后溶液的体积等于混合前两种溶液的体积之和),则 的物质的量浓度为
的物质的量浓度为 。
。
您最近半年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】按要求填写下列空白(NA表示阿伏德罗常数的值)。
(1)0.5molCH4质量为___ ,在标准状况下的体积为___ 。
(2)15.6gNa2R含0.4molNa+,则Na2R的摩尔质量为___ ,含R质量为3.2g的Na2R,其物质的量为___ 。
(3)在300mL3 mol∙L−1的K2SO4的溶液中,SO 物质的量为
物质的量为___ ,K+的物质的量浓度为___ 。
(4)同温同压下,同体积的CO2和SO2物质的量之比为___ ,密度之比为___ ;同温同压下,同质量的CO2和SO2体积之比为___ 。
(5)标准状况下,CH4和CO的混合气体6.72L,质量为6g,此混合物中CH4质量是__ ,CO物质的量是__ ,混合气体的平均摩尔质量是___ 。
(1)0.5molCH4质量为
(2)15.6gNa2R含0.4molNa+,则Na2R的摩尔质量为
(3)在300mL3 mol∙L−1的K2SO4的溶液中,SO
 物质的量为
物质的量为(4)同温同压下,同体积的CO2和SO2物质的量之比为
(5)标准状况下,CH4和CO的混合气体6.72L,质量为6g,此混合物中CH4质量是
您最近半年使用:0次
填空题
|
较易
(0.85)
【推荐1】回答下列问题:
(1)1.204×1024个Na+约含___________ mol Na+,其质量为___________ g;
(2)4.9gH2SO4约含有___________ 个H,共含有___________ mol原子。
(3)标准状况下,224mL的氨气(NH3)中含有的氢原子数为___________ 。
(4)同温同压下,有0.3mol O2(气)0.2mol O3(气),它们所含的原子数之比为___________ ,它们的体积之比为___________ 。
(1)1.204×1024个Na+约含
(2)4.9gH2SO4约含有
(3)标准状况下,224mL的氨气(NH3)中含有的氢原子数为
(4)同温同压下,有0.3mol O2(气)0.2mol O3(气),它们所含的原子数之比为
您最近半年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】CH4和H2是两种重要的气体燃料
(1)标准状况下,5.6L的CH4的质量为________ 。
(2)4gH2在标准状况下的体积为________ ,所含的氢原子数约为________ 。
(3)相同质量的CH4和H2,所含的原子数之比为________ 。
(4)含6.02×1023个电子的CH4在标准状况下的体积为________ 。
(5)0.5molH2完全燃烧,生成的水的质量为________ 。
(1)标准状况下,5.6L的CH4的质量为
(2)4gH2在标准状况下的体积为
(3)相同质量的CH4和H2,所含的原子数之比为
(4)含6.02×1023个电子的CH4在标准状况下的体积为
(5)0.5molH2完全燃烧,生成的水的质量为
您最近半年使用:0次



