物质的量是学习化学的基础。
(1)14.4gCO和CO2的混合气体在标准状况下所占的体积为8.96L,其中CO的质量为___ 。
(2)市售浓H2SO4的质量分数为98%、密度为1.84g/cm3,其浓度为___ mol•L-1。
(3)19g某二价金属的氯化物ACl3中含有0.4molCl-离子,金属A的相对原子质量是___ 。
(4)根据反应14CuSO4+5FeS2+12H2O 7Cu2S+5FeSO4+12H2SO4,可知当有2.5molFeS2参加反应时,氧化产物的物质的量为
7Cu2S+5FeSO4+12H2SO4,可知当有2.5molFeS2参加反应时,氧化产物的物质的量为__ mol。
(1)14.4gCO和CO2的混合气体在标准状况下所占的体积为8.96L,其中CO的质量为
(2)市售浓H2SO4的质量分数为98%、密度为1.84g/cm3,其浓度为
(3)19g某二价金属的氯化物ACl3中含有0.4molCl-离子,金属A的相对原子质量是
(4)根据反应14CuSO4+5FeS2+12H2O
 7Cu2S+5FeSO4+12H2SO4,可知当有2.5molFeS2参加反应时,氧化产物的物质的量为
7Cu2S+5FeSO4+12H2SO4,可知当有2.5molFeS2参加反应时,氧化产物的物质的量为
更新时间:2021-10-29 10:42:30
|
相似题推荐
【推荐1】实验室利用二氧化锰和浓盐酸反应制取Cl2,化学方程式如下:MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O
(1)请用单线桥标出该反应电子转移的方向和数目__ ,该反应的氧化产物是__ 。
(2)其中氧化剂与还原剂的物质的量之比是__ ;若实验中有87g的MnO2完全反应,则制得的Cl2在标况下的体积是__ L。
 MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O(1)请用单线桥标出该反应电子转移的方向和数目
(2)其中氧化剂与还原剂的物质的量之比是
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】进行下列化学基本量的计算,并将结果直接填入空格中。
(1)0.1摩H2SO4约含________ 个H原子,溶于水后电离出_______ mol SO 。
。
(2)36克水与_______ g CO2具有相同的氧原子数。
(3)71gNa2SO4中所含Na+的物质的量为_______ mol。
(4)在9.5g某二价金属的氯化物中含0.2mol Cl-,此氯化物的摩尔质量为________ ;该金属元素的相对原子质量为_______ 。
(5)标准状况是指_____ ℃,_____ Pa;在标准状况下,0.5molN2的体积都约为_____ L,质量为_______ g。
(1)0.1摩H2SO4约含
 。
。(2)36克水与
(3)71gNa2SO4中所含Na+的物质的量为
(4)在9.5g某二价金属的氯化物中含0.2mol Cl-,此氯化物的摩尔质量为
(5)标准状况是指
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】(1)3.6 g H2O的物质的量是____ ,含有水分子的数目是_____ ,含有氢原子的物质的量是_____ 。
(2)1.5molCO2和______ g CH4在标准状况下占有相同的体积,其体积为________ 。
(3)在标准状况下,100mL某气体的质量为0.179g,该气体的相对分子质量为________ 。
(4)现有mg某X2气体,它的摩尔质量为M g/mol,阿伏加 德罗常数用NA表示,则:该气体的物质的量为______ mol;一个X原子的质量为_______ g;该气体在标准状况下的体积为______ L。
(2)1.5molCO2和
(3)在标准状况下,100mL某气体的质量为0.179g,该气体的相对分子质量为
(4)现有mg某X2气体,它的摩尔质量为M g/mol,阿伏加 德罗常数用NA表示,则:该气体的物质的量为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】取10g 硫酸铁溶于水配成100ml溶液,
(1)该硫酸铁的物质的量浓度___________
(2)Fe3+物质的量浓度___________
(3)取出该溶液20ml含SO 物质的量为
物质的量为___________ ,然后稀释,使其硫酸铁物质的量浓度变为0.05mol/L,则应加水___________ ml(设稀释时,对溶液体积的影响忽略不计)
(1)该硫酸铁的物质的量浓度
(2)Fe3+物质的量浓度
(3)取出该溶液20ml含SO
 物质的量为
物质的量为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】现有一瓶气体为 ,气体的物质的量为0.2mol。
,气体的物质的量为0.2mol。
(1)气体的质量为_______ ,气体中原子的物质的量为_______ mol。
(2)气体中所含分子数约为_______ 。
(3)气体在标准状况下的体积为_______ 。
(4)将气体完全溶于水中形成500mL溶液,所得溶液溶质的物质的量浓度为_______  。
。
(5)将(4)中所得溶液取出100mL,加水稀释至1000mL,所得溶液溶质的物质的量浓度为_______  。
。
 ,气体的物质的量为0.2mol。
,气体的物质的量为0.2mol。(1)气体的质量为
(2)气体中所含分子数约为
(3)气体在标准状况下的体积为
(4)将气体完全溶于水中形成500mL溶液,所得溶液溶质的物质的量浓度为
 。
。(5)将(4)中所得溶液取出100mL,加水稀释至1000mL,所得溶液溶质的物质的量浓度为
 。
。
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】氧化还原反应在生产、生活等领域有广泛的应用。
(1)铝热反应可用于焊接钢轨,其反应原理为: 。在该反应中
。在该反应中___________ 元素(填元素符号)的化合价升高,通过此反应的分析可知规律:氧化还原反应中元素化合价升高总数___________ (填“>”、“<”或“=”)元素化合价降低总数。
(2)汽车常装有安全气囊,当发生强烈碰撞时,瞬间引发以下反应: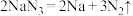 ,所产生的气体快速充满气囊,可以达到保护车内人员的目的。某安全气囊
,所产生的气体快速充满气囊,可以达到保护车内人员的目的。某安全气囊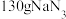 完全分解,反应中转移电子的物质的量为
完全分解,反应中转移电子的物质的量为___________  ,在标准状况下,气囊膨胀的体积约为
,在标准状况下,气囊膨胀的体积约为___________  。
。
(3)钠—钾合金(化学式为 )可在核反应堆中用作热交换液。合金与水反应原理为:
)可在核反应堆中用作热交换液。合金与水反应原理为: ,现将
,现将 加入
加入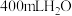 中充分反应,忽略溶液体积的变化。
中充分反应,忽略溶液体积的变化。
①反应生成 的质量为
的质量为___________ 。
②所得溶液中 的物质的量浓度为
的物质的量浓度为___________ 。
(1)铝热反应可用于焊接钢轨,其反应原理为:
 。在该反应中
。在该反应中(2)汽车常装有安全气囊,当发生强烈碰撞时,瞬间引发以下反应:
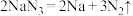 ,所产生的气体快速充满气囊,可以达到保护车内人员的目的。某安全气囊
,所产生的气体快速充满气囊,可以达到保护车内人员的目的。某安全气囊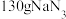 完全分解,反应中转移电子的物质的量为
完全分解,反应中转移电子的物质的量为 ,在标准状况下,气囊膨胀的体积约为
,在标准状况下,气囊膨胀的体积约为 。
。(3)钠—钾合金(化学式为
 )可在核反应堆中用作热交换液。合金与水反应原理为:
)可在核反应堆中用作热交换液。合金与水反应原理为: ,现将
,现将 加入
加入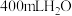 中充分反应,忽略溶液体积的变化。
中充分反应,忽略溶液体积的变化。①反应生成
 的质量为
的质量为②所得溶液中
 的物质的量浓度为
的物质的量浓度为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】已知 中含有
中含有 。
。
(1) 的摩尔质量为
的摩尔质量为__________ 。
(2)R的相对原子质量为__________ 。
(3)若 中含
中含 的质量为
的质量为 ,则
,则 的物质的量为
的物质的量为__________ , 的数目为
的数目为__________ 。
(4)现有标准状况下 和
和 混合气体8.96 L,其质量为
混合气体8.96 L,其质量为 ,则此混合气体中,
,则此混合气体中, 与
与 的体积之比是
的体积之比是__________ ,C和 的原子个数比是
的原子个数比是__________ 。
 中含有
中含有 。
。(1)
 的摩尔质量为
的摩尔质量为(2)R的相对原子质量为
(3)若
 中含
中含 的质量为
的质量为 ,则
,则 的物质的量为
的物质的量为 的数目为
的数目为(4)现有标准状况下
 和
和 混合气体8.96 L,其质量为
混合气体8.96 L,其质量为 ,则此混合气体中,
,则此混合气体中, 与
与 的体积之比是
的体积之比是 的原子个数比是
的原子个数比是
您最近一年使用:0次

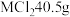 ,含有
,含有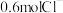 ,则该化合物的摩尔质量为
,则该化合物的摩尔质量为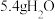 含有
含有 表示,
表示,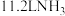 (标况)约含
(标况)约含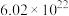 个
个 含
含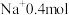 ,R的相对原子质量为
,R的相对原子质量为

