实验小组探究ClO-、I2、SO42-在酸性条件下的氧化性强弱,实验如下:
实验①:在淀粉碘化钾溶液中加入少量次氯酸钠溶液,并加入少量的稀硫酸,溶液立即变蓝;
实验②:向实验①的溶液中加入4 mL 0.5 mol/L的亚硫酸钠溶液,蓝色恰好完全褪去。
(1)写出实验①中发生反应的离子方程式________________ 。
(2)实验②的化学反应中,氧化剂得到电子的物质的量是_____ mol。
(3)以上实验说明,在酸性条件下ClO-、I2、SO42-的氧化性由弱到强的顺序是______ 。
实验①:在淀粉碘化钾溶液中加入少量次氯酸钠溶液,并加入少量的稀硫酸,溶液立即变蓝;
实验②:向实验①的溶液中加入4 mL 0.5 mol/L的亚硫酸钠溶液,蓝色恰好完全褪去。
(1)写出实验①中发生反应的离子方程式
(2)实验②的化学反应中,氧化剂得到电子的物质的量是
(3)以上实验说明,在酸性条件下ClO-、I2、SO42-的氧化性由弱到强的顺序是
更新时间:2018/12/19 11:59:20
|
相似题推荐
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】某课外活动小组进行Fe(OH)3胶体的制备实验并检验其性质。
(1)在小烧杯中加入20mL蒸馏水,加热至沸腾后,向沸水中滴入几滴饱和FeCl3溶液,继续煮沸至溶液呈___________ 色,停止加热,即制得Fe(OH)3胶体。写出该反应的离子方程式___________ 。
(2)将制得的胶体放入半透膜制成的袋内,如图所示,放置一段时间后,取少量半透膜外的液体于试管中,置于暗处,用一束强光从侧面照射,观察___________ (填“有”或“无”)丁达尔现象。

(3)若向Fe(OH)3胶体中滴入硫酸直到过量,描述此过程的实验现象___________ 。
(1)在小烧杯中加入20mL蒸馏水,加热至沸腾后,向沸水中滴入几滴饱和FeCl3溶液,继续煮沸至溶液呈
(2)将制得的胶体放入半透膜制成的袋内,如图所示,放置一段时间后,取少量半透膜外的液体于试管中,置于暗处,用一束强光从侧面照射,观察

(3)若向Fe(OH)3胶体中滴入硫酸直到过量,描述此过程的实验现象
您最近半年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】下列物质中,①Cu②NaCl晶体③ ④
④ ⑤碘酒⑥液态HCl⑦AgCl⑧
⑤碘酒⑥液态HCl⑦AgCl⑧ ⑨
⑨ ⑩NaCl溶液。
⑩NaCl溶液。
(1)属于电解质的是___________ (填序号,下同),属于非电解的是___________ ,能导电的是___________ 。
(2)写出下列物质在水溶液中的电离方程式:
NaBr:___________ 。
 :
:___________ 。
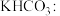
___________ 。
(3)写出下列反应的离子方程式:
① 溶液中通入少量
溶液中通入少量 :
:___________ 。
② 固体中加入足量稀硫酸:
固体中加入足量稀硫酸:___________ 。
 ④
④ ⑤碘酒⑥液态HCl⑦AgCl⑧
⑤碘酒⑥液态HCl⑦AgCl⑧ ⑨
⑨ ⑩NaCl溶液。
⑩NaCl溶液。(1)属于电解质的是
(2)写出下列物质在水溶液中的电离方程式:
NaBr:
 :
: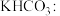
(3)写出下列反应的离子方程式:
①
 溶液中通入少量
溶液中通入少量 :
:②
 固体中加入足量稀硫酸:
固体中加入足量稀硫酸:
您最近半年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】在化学家的眼中,丰富多彩的化学物质可以按一定的标准进行分类。电解质和非电解质是中学化学中两个重要的概念,辨析清楚有利于我们对元素化合物知识的学习。
Ⅰ.现有下列几种物质:
①4%HCl溶液 ②CuSO4·5H2O ③纳米级氧化铁 ④苛性钾 ⑤SO2 ⑥Fe(OH)3胶体 ⑦CH3CH2OH ⑧氨水 ⑨硫酸铁溶液
(1)上述几种物质中属于电解质的有___________ (填序号)。
(2)有两种物质在水溶液中可发生反应,离子方程式为:Fe3++3OH-=Fe(OH)3↓,这两种物质的序号是___________ (填序号)。
Ⅱ.写出下列典型物质在水中的电离方程式。
(3)NaHSO4:___________ 。
(4)KAl(SO4)2:___________ 。
Ⅲ.写出下列典型反应的离子方程式:
(5)石灰石与足量盐酸溶液反应:___________ 。
(6)CuSO4溶液与Ba(OH)2溶液混合:___________ 。
(7)NaHCO3溶液与稀盐酸混合:___________ 。
(8)已知次磷酸(H3PO2)是一元中强酸,请写出其与足量氢氧化钠反应的离子方程式:___________ 。
Ⅰ.现有下列几种物质:
①4%HCl溶液 ②CuSO4·5H2O ③纳米级氧化铁 ④苛性钾 ⑤SO2 ⑥Fe(OH)3胶体 ⑦CH3CH2OH ⑧氨水 ⑨硫酸铁溶液
(1)上述几种物质中属于电解质的有
(2)有两种物质在水溶液中可发生反应,离子方程式为:Fe3++3OH-=Fe(OH)3↓,这两种物质的序号是
Ⅱ.写出下列典型物质在水中的电离方程式。
(3)NaHSO4:
(4)KAl(SO4)2:
Ⅲ.写出下列典型反应的离子方程式:
(5)石灰石与足量盐酸溶液反应:
(6)CuSO4溶液与Ba(OH)2溶液混合:
(7)NaHCO3溶液与稀盐酸混合:
(8)已知次磷酸(H3PO2)是一元中强酸,请写出其与足量氢氧化钠反应的离子方程式:
您最近半年使用:0次
填空题
|
较易
(0.85)
【推荐1】回答下列问题:
(1)写出下列反应的化学方程式,用双线桥标明电子转移的方向和数目,注明“被氧化”、“被还原”并指出氧化剂、还原剂。
①Fe2O3与CO在高温下的反应:_______ 。
②KClO3与MnO2加热条件下反应:_______ 。
(2)已知:
Se+2H2SO4(浓)→2SO2↑+SeO2+2H2O
2SO2+SeO2+2H2O→Se+2SO +4H+
+4H+
SeO2、H2SO4(浓)、SO2的氧化性由强到弱的顺序是_______ 。
(1)写出下列反应的化学方程式,用双线桥标明电子转移的方向和数目,注明“被氧化”、“被还原”并指出氧化剂、还原剂。
①Fe2O3与CO在高温下的反应:
②KClO3与MnO2加热条件下反应:
(2)已知:
Se+2H2SO4(浓)→2SO2↑+SeO2+2H2O
2SO2+SeO2+2H2O→Se+2SO
 +4H+
+4H+SeO2、H2SO4(浓)、SO2的氧化性由强到弱的顺序是
您最近半年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】复印机工作时易产生臭氧,臭氧具有强氧化性,可使润湿的KI-淀粉试纸变蓝。反应为O3+2KI+H2O=2KOH+I2+O2,回答下列问题:
(1)反应4.8gO3得到___________ mol电子;
(2)___________ 是氧化剂,___________ 是还原剂;
(3)O3的氧化性___________ I2的氧化性(填写“>”、“<”、“=”);
(4)反应中被还原的氧原子与未被还原的氧子个数比为___________ 。
(1)反应4.8gO3得到
(2)
(3)O3的氧化性
(4)反应中被还原的氧原子与未被还原的氧子个数比为
您最近半年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】对于数以千万计的化学物质和为数更多的化学反应,分类法的作用几乎是无可替代的。
(1)现有下列6种物质:H2O、SiO2、CaO、MgO、Fe2O3、Na2O2。按照不同的分类标准,它们中有一种物质与其他5种有明显不同,请找出这种物质,并写出依据(写出两种分类方法):
①__ ;__ ;
②__ ;__ ;
(2)KClO3和浓盐酸在一定温度下反应会生成黄绿色的易爆物二氧化氯,其化学方程式为:2KClO3+4HCl(浓)=2KCl+2ClO2↑+Cl2↑+2H2O。(ClO2中氯元素的化合价为+4价)
(i)浓盐酸在反应中表现出来的性质是___ (填写编号)
①只有还原性 ②还原性和酸性 ③只有氧化性 ④氧化性和酸性
(ii)产生0.1molCl2,则消耗浓HCl的物质的量为___ mol。
(1)现有下列6种物质:H2O、SiO2、CaO、MgO、Fe2O3、Na2O2。按照不同的分类标准,它们中有一种物质与其他5种有明显不同,请找出这种物质,并写出依据(写出两种分类方法):
①
②
(2)KClO3和浓盐酸在一定温度下反应会生成黄绿色的易爆物二氧化氯,其化学方程式为:2KClO3+4HCl(浓)=2KCl+2ClO2↑+Cl2↑+2H2O。(ClO2中氯元素的化合价为+4价)
(i)浓盐酸在反应中表现出来的性质是
①只有还原性 ②还原性和酸性 ③只有氧化性 ④氧化性和酸性
(ii)产生0.1molCl2,则消耗浓HCl的物质的量为
您最近半年使用:0次
【推荐2】高锰酸钾是一种典型的强氧化剂。
Ⅰ.用 酸性溶液处理
酸性溶液处理 和CuS的混合物时,发生如下反应:
和CuS的混合物时,发生如下反应:
①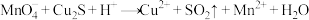 (未配平)
(未配平)
②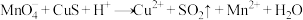 (未配平)
(未配平)
(1)反应①中被氧化的元素是__________ ,氧化剂与还原剂的物质的量之比为__________ 。
(2)当反应①中转移0.8mol电子,生成 的体积为
的体积为__________ L(标准状况下)。
(3)配平并用单线桥法标出反应②中电子转移的方向和数目______________ 。
Ⅱ.在稀硫酸中, 和
和 能发生氧化还原反应:
能发生氧化还原反应:
氧化反应:
还原反应:
(4)写出该氧化还原反应的离子方程式______________________________ 。
(5)反应中若有 参加此反应,转移电子的个数为
参加此反应,转移电子的个数为__________ 。
(6)由上述反应得出物质氧化性强弱的结论是
__________ (填“>”或“<”) 。
。
(7)实验中发现,当加入的少量 完全反应后,
完全反应后, 仍能发生反应放出气体,其原因可能是
仍能发生反应放出气体,其原因可能是__________ 。
Ⅰ.用
 酸性溶液处理
酸性溶液处理 和CuS的混合物时,发生如下反应:
和CuS的混合物时,发生如下反应:①
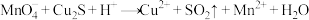 (未配平)
(未配平)②
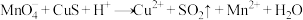 (未配平)
(未配平)(1)反应①中被氧化的元素是
(2)当反应①中转移0.8mol电子,生成
 的体积为
的体积为(3)配平并用单线桥法标出反应②中电子转移的方向和数目
Ⅱ.在稀硫酸中,
 和
和 能发生氧化还原反应:
能发生氧化还原反应:氧化反应:

还原反应:

(4)写出该氧化还原反应的离子方程式
(5)反应中若有
 参加此反应,转移电子的个数为
参加此反应,转移电子的个数为(6)由上述反应得出物质氧化性强弱的结论是

 。
。(7)实验中发现,当加入的少量
 完全反应后,
完全反应后, 仍能发生反应放出气体,其原因可能是
仍能发生反应放出气体,其原因可能是
您最近半年使用:0次
填空题
|
较易
(0.85)
【推荐3】运动会上发令枪所用“火药”的主要成分是氯酸钾和红磷,撞击时发生的化学反应为:5KClO3+6P=3P2O5+5A(已配平)。
(1)生成物A的化学式是_____ 。
(2)该反应是否是氧化还原反应?_____ (填“是”或“不是”)。若是,请指出被还原的元素;若不是,请说明理由:_________ 。
(3)已知铜在加热时能被浓硫酸溶解,其反应的化学方程式如下:Cu+2H2SO4(浓)=CuSO4+SO2↑+2H2O,用双线桥法表示电子得失的方向和数目:____________ 。
(4)若2molCu参加反应,则该过程转移的电子是___________ mol。
(1)生成物A的化学式是
(2)该反应是否是氧化还原反应?
(3)已知铜在加热时能被浓硫酸溶解,其反应的化学方程式如下:Cu+2H2SO4(浓)=CuSO4+SO2↑+2H2O,用双线桥法表示电子得失的方向和数目:
(4)若2molCu参加反应,则该过程转移的电子是
您最近半年使用:0次

 3CO2+2Fe
3CO2+2Fe

