过氧化钠常作漂白剂、杀菌剂、消毒剂。过氧化钠保存不当容易吸收空气中CO2而变质。
(1)某课外活动小组欲探究某过氧化钠样品是否已经变质,取少量样品,溶解,加入______ 溶液,充分振荡后有白色沉淀,证明Na2O2已经变质。
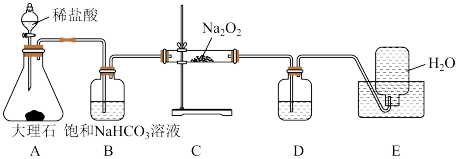
(2)该课外活动小组为了粗略测定过氧化钠的纯度,他们称取a g样品,并设计用如图装置来测定过氧化钠的质量分数。
①将仪器连接好以后,必须进行的第一步操作是____________________________________ 。
②B装置出来的气体是否需要干燥______ (填“是”或“否”)。
③D中NaOH溶液的作用____________________ 。
④实验结束时,读取实验中生成气体的体积时,不合理的是__________ 。
a.直接读取气体体积,不需冷却到室温
b.上下移动量筒,使得E、F中液面高度相同
c.视线与凹液面的最低点相平读取量筒中水的体积
⑤读出量筒内水的体积后,折算成标准状况下氧气的体积为V mL,则样品中过氧化钠的质量分数为_____________ 。
⑥实验完成后E到F之间导管内残留水的体积会使测量结果________ (填“偏大”“偏小”或“不影响”)。
(1)某课外活动小组欲探究某过氧化钠样品是否已经变质,取少量样品,溶解,加入
(2)该课外活动小组为了粗略测定过氧化钠的纯度,他们称取a g样品,并设计用如图装置来测定过氧化钠的质量分数。

①将仪器连接好以后,必须进行的第一步操作是
②B装置出来的气体是否需要干燥
③D中NaOH溶液的作用
④实验结束时,读取实验中生成气体的体积时,不合理的是
a.直接读取气体体积,不需冷却到室温
b.上下移动量筒,使得E、F中液面高度相同
c.视线与凹液面的最低点相平读取量筒中水的体积
⑤读出量筒内水的体积后,折算成标准状况下氧气的体积为V mL,则样品中过氧化钠的质量分数为
⑥实验完成后E到F之间导管内残留水的体积会使测量结果
更新时间:2018-12-19 10:15:21
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
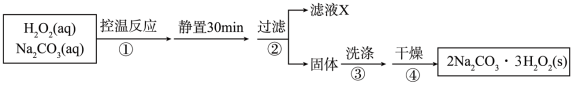
【推荐1】过碳酸钠( ,相对分子质量314)俗名固体双氧水,是一种新型家用清洁剂和消毒剂,相比于传统消毒剂有高效、绿色的优点;过碳酸钠是一种白色细小颗粒状粉末,具有碳酸钠和双氧水的双重性质,其3%水溶液的pH约为10.某兴趣小组制备过碳酸钠的实验方案如下:
,相对分子质量314)俗名固体双氧水,是一种新型家用清洁剂和消毒剂,相比于传统消毒剂有高效、绿色的优点;过碳酸钠是一种白色细小颗粒状粉末,具有碳酸钠和双氧水的双重性质,其3%水溶液的pH约为10.某兴趣小组制备过碳酸钠的实验方案如下:
已知: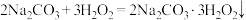 。
。
回答下列问题:
(1)过碳酸钠中O元素有两种化合价,分别是_______ ;某同学取适量过碳酸钠溶液,滴加酚酞,微热后振荡,观察到的现象是_______ 。
(2)制备过程中“过滤”用到的主要玻璃仪器是_______ 。“控温反应”中一般控制温度不高于50℃的原因是_______ ,向滤液X中加入无水乙醇可析出过碳酸钠,原因是_______ 。
(3)以下关于过碳酸钠的说法正确的是_______(填选项字母)。
(4)有研究认为过碳酸钠溶液强力的杀菌消毒效果来自于 在碱性条件下转化为氧化性更强的
在碱性条件下转化为氧化性更强的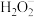 离子。请将过碳酸钠溶液中产生
离子。请将过碳酸钠溶液中产生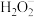 离子的方程式补充完整并配平:
离子的方程式补充完整并配平:______
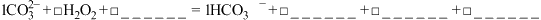
(5)市售过碳酸钠一般都含有碳酸钠,现用以下方案测定某过碳酸钠样品的纯度:
称量73.4g样品;全部溶于水中并加入足量稀盐酸充分反应;加热蒸发至蒸发皿中出现大量晶体时,停止加热,利用余热蒸干蒸发皿中剩余水分;称量所得固体质量为58.5g。
①“全部溶于水中并加入足量稀盐酸”产生两种无色无味的气体,写出该反应的化学方程式_______ ;
②该样品中过碳酸钠的质量分数_______ (保留小数点后一位)。
 ,相对分子质量314)俗名固体双氧水,是一种新型家用清洁剂和消毒剂,相比于传统消毒剂有高效、绿色的优点;过碳酸钠是一种白色细小颗粒状粉末,具有碳酸钠和双氧水的双重性质,其3%水溶液的pH约为10.某兴趣小组制备过碳酸钠的实验方案如下:
,相对分子质量314)俗名固体双氧水,是一种新型家用清洁剂和消毒剂,相比于传统消毒剂有高效、绿色的优点;过碳酸钠是一种白色细小颗粒状粉末,具有碳酸钠和双氧水的双重性质,其3%水溶液的pH约为10.某兴趣小组制备过碳酸钠的实验方案如下:
已知:
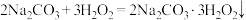 。
。回答下列问题:
(1)过碳酸钠中O元素有两种化合价,分别是
(2)制备过程中“过滤”用到的主要玻璃仪器是
(3)以下关于过碳酸钠的说法正确的是_______(填选项字母)。
| A.过碳酸钠是混合物 |
B.过碳酸钠水溶液的显碱性可能与 有关 有关 |
| C.制备过碳酸钠的过程涉及氧化还原反应 |
D.可用 粉末大致判断过碳酸钠水溶液是否已经失效 粉末大致判断过碳酸钠水溶液是否已经失效 |
(4)有研究认为过碳酸钠溶液强力的杀菌消毒效果来自于
 在碱性条件下转化为氧化性更强的
在碱性条件下转化为氧化性更强的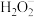 离子。请将过碳酸钠溶液中产生
离子。请将过碳酸钠溶液中产生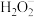 离子的方程式补充完整并配平:
离子的方程式补充完整并配平: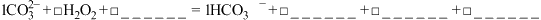
(5)市售过碳酸钠一般都含有碳酸钠,现用以下方案测定某过碳酸钠样品的纯度:
称量73.4g样品;全部溶于水中并加入足量稀盐酸充分反应;加热蒸发至蒸发皿中出现大量晶体时,停止加热,利用余热蒸干蒸发皿中剩余水分;称量所得固体质量为58.5g。
①“全部溶于水中并加入足量稀盐酸”产生两种无色无味的气体,写出该反应的化学方程式
②该样品中过碳酸钠的质量分数
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】某课外活动小组模拟呼吸面具中的反应原理(
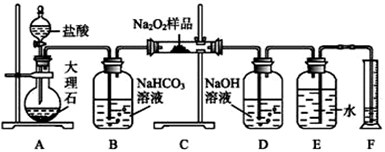
 )设计并用如图所示的装置(连接胶管及夹持装置均省略)来制取氧气并测量氧气的体积。图中量气装置E由甲、乙两根玻璃管组成,它们由橡皮管连通,并装入适量水。甲管有刻度(0~50mL)供量气用,乙管可上下移动调节液面高低。
)设计并用如图所示的装置(连接胶管及夹持装置均省略)来制取氧气并测量氧气的体积。图中量气装置E由甲、乙两根玻璃管组成,它们由橡皮管连通,并装入适量水。甲管有刻度(0~50mL)供量气用,乙管可上下移动调节液面高低。
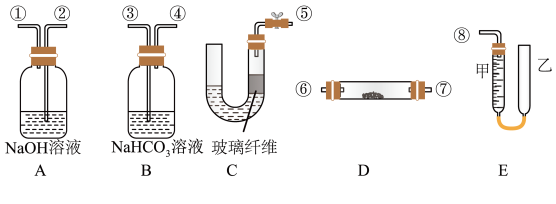
实验可供选用的药品还有稀硫酸、盐酸、过氧化钠、大理石、水。试回答:
(1)图中各装置接口连接顺序是_____ (填各接口的编号)。
(2)装置A的作用是_____ ,反应的化学方程式_____ 。
(3)装置B的作用是____ ,反应的化学方程式为______ 。
(4)装置C中放入的反应物是_____ ,反应的化学方程式为_____ 。
(5)实验结束读取氧气体积时,若乙管中液面高于甲管中液面,会使测得的氧气体积___ (填“偏大”“偏小”或“无影响”)。若有影响,应向___ (填“上”或“下”)移动乙管,使甲、乙管液面相平(注:若第一空填无影响,第二空不用填写)。

 )设计并用如图所示的装置(连接胶管及夹持装置均省略)来制取氧气并测量氧气的体积。图中量气装置E由甲、乙两根玻璃管组成,它们由橡皮管连通,并装入适量水。甲管有刻度(0~50mL)供量气用,乙管可上下移动调节液面高低。
)设计并用如图所示的装置(连接胶管及夹持装置均省略)来制取氧气并测量氧气的体积。图中量气装置E由甲、乙两根玻璃管组成,它们由橡皮管连通,并装入适量水。甲管有刻度(0~50mL)供量气用,乙管可上下移动调节液面高低。
实验可供选用的药品还有稀硫酸、盐酸、过氧化钠、大理石、水。试回答:
(1)图中各装置接口连接顺序是
(2)装置A的作用是
(3)装置B的作用是
(4)装置C中放入的反应物是
(5)实验结束读取氧气体积时,若乙管中液面高于甲管中液面,会使测得的氧气体积
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐1】Cr2O3可作为某些化学反应的催化剂。工业上利用铬铁矿生产Cr2O3的工艺流程如图:

铬铁矿的主要成分有Cr2O3•FeO、FeO、SiO2、Al2O3,铵铁矾的化学式为NH4Fe(SO4)2•12H2O。回答下列问题:
(1)“酸浸氧化”时,为提高反应速率,除采用120~150℃外,还可采取的措施为____ 。
(2)“酸浸氧化”时,Cr2O3•FeO发生反应的化学方程式为____ 。
(3)流程中,第二次加氨水的目的是___ 。
(4)已知:常温下,Al(OH)3+H2O Al(OH)
Al(OH) +H+Ka=10-13.37;Al(OH)3(s)
+H+Ka=10-13.37;Al(OH)3(s) 3OH-(aq)+Al3+(aq)Ksp=1.9×10-33;通常认为离子浓度小于10-5mol·L-1为沉淀完全。用pH计精确测得“沉淀”工序实际操作时pH为7.87,经“沉淀”后所得滤液中Al(OH)
3OH-(aq)+Al3+(aq)Ksp=1.9×10-33;通常认为离子浓度小于10-5mol·L-1为沉淀完全。用pH计精确测得“沉淀”工序实际操作时pH为7.87,经“沉淀”后所得滤液中Al(OH) 的浓度为
的浓度为____ mol·L-1,c(Al3+)____ (填“已”或“未”)达到沉淀完全的标准。
(5)将“滤液1”中的主要溶质回收后的用途为____ 。
(6)“分离”时,反应的离子方程式为____ 。
(7)已知:亚铁氧化物(含FeO、Cr2O3•FeO中的FeO部分)在铬铁矿中的质量分数为28%,当处理1t铬铁矿时,至少需要消耗CrO3____ t(保留2位有效数字)。

铬铁矿的主要成分有Cr2O3•FeO、FeO、SiO2、Al2O3,铵铁矾的化学式为NH4Fe(SO4)2•12H2O。回答下列问题:
(1)“酸浸氧化”时,为提高反应速率,除采用120~150℃外,还可采取的措施为
(2)“酸浸氧化”时,Cr2O3•FeO发生反应的化学方程式为
(3)流程中,第二次加氨水的目的是
(4)已知:常温下,Al(OH)3+H2O
 Al(OH)
Al(OH) +H+Ka=10-13.37;Al(OH)3(s)
+H+Ka=10-13.37;Al(OH)3(s) 3OH-(aq)+Al3+(aq)Ksp=1.9×10-33;通常认为离子浓度小于10-5mol·L-1为沉淀完全。用pH计精确测得“沉淀”工序实际操作时pH为7.87,经“沉淀”后所得滤液中Al(OH)
3OH-(aq)+Al3+(aq)Ksp=1.9×10-33;通常认为离子浓度小于10-5mol·L-1为沉淀完全。用pH计精确测得“沉淀”工序实际操作时pH为7.87,经“沉淀”后所得滤液中Al(OH) 的浓度为
的浓度为(5)将“滤液1”中的主要溶质回收后的用途为
(6)“分离”时,反应的离子方程式为
(7)已知:亚铁氧化物(含FeO、Cr2O3•FeO中的FeO部分)在铬铁矿中的质量分数为28%,当处理1t铬铁矿时,至少需要消耗CrO3
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】I.磁性材料A是由两种元素组成的化合物,某研究小组按如图流程探究其组成:
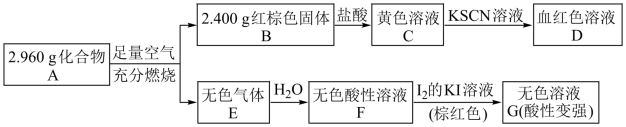
请回答:
(1)A的化学式为__________ 。A煅烧生成B和E的化学方程式为___________________ 。
(2)溶液C可溶解铜片,反应的离子方程式为__________ ,例举该反应的一个实际应用是____________ 。
(3)已知化合物A能与稀硫酸反应,生成一种淡黄色不溶物和一种气体(标况下的密度为1.518 g/L),该气体分子的电子式为____________ 。该反应的离子方程式为______________ 。
II.某同学用副产品FeCl3溶液吸收H2S,得到单质硫;过滤后,再以石墨为电极,在一定条件下电解滤液。
(1) FeCl3与H2S反应的离子方程式为________________
(2) 电解池中H+再阴极放电产生H2,阳极的电极反应为____________
(3) 综合分析实验II的两个反应,可知该实验有两个显著优点:①H2S的原子利用率100%;②________________

请回答:
(1)A的化学式为
(2)溶液C可溶解铜片,反应的离子方程式为
(3)已知化合物A能与稀硫酸反应,生成一种淡黄色不溶物和一种气体(标况下的密度为1.518 g/L),该气体分子的电子式为
II.某同学用副产品FeCl3溶液吸收H2S,得到单质硫;过滤后,再以石墨为电极,在一定条件下电解滤液。
(1) FeCl3与H2S反应的离子方程式为
(2) 电解池中H+再阴极放电产生H2,阳极的电极反应为
(3) 综合分析实验II的两个反应,可知该实验有两个显著优点:①H2S的原子利用率100%;②
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】纳米材料一直是人们研究的重要课题,例如纳米级Fe粉表面积大,具有超强的磁性、高效催化性等优良的性质。
Ⅰ.实验室采用气相还原法制备纳米级Fe,其流程如图所示:

(1)纳米级Fe和稀盐酸反应的离子方程式为__________________________ 。
(2)如何将FeCl2·nH2O固体加热脱水制得无水FeCl2_________ (用简要文字描述)。
(3)生成纳米级Fe的化学方程式为__________________ 。
Ⅱ.查阅资料:在不同温度下,纳米级Fe粉与水蒸气反应的固体产物不同,温度低于570 ℃时生成FeO,高于570 ℃时生成Fe3O4。甲同学用如图甲所示装置进行纳米级Fe粉与水蒸气反应的实验,乙同学用图乙所示的装置进行纳米级Fe粉与水蒸气的反应并验证产物。
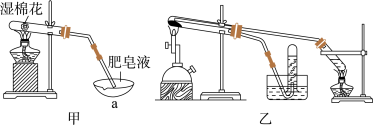
(4)甲装置中纳米级Fe粉与水蒸气反应的化学方程式是____________ 。
(5)乙同学为探究实验结束后试管内的固体物质成分,进行了下列实验:
根据以上实验,乙同学认为该条件下反应的固体产物为FeO。丙同学认为乙同学的结论不正确,他的理由是________ (用简要文字描述)。
(6)丁同学称取5.60 g Fe粉,用乙装置反应一段时间后,停止加热。将试管内的固体物质在干燥器中冷却后,称得质量为6.88 g,则丁同学实验后的固体物质中氧化物的质量分数为___ (结果保留三位有效数字)。
Ⅰ.实验室采用气相还原法制备纳米级Fe,其流程如图所示:

(1)纳米级Fe和稀盐酸反应的离子方程式为
(2)如何将FeCl2·nH2O固体加热脱水制得无水FeCl2
(3)生成纳米级Fe的化学方程式为
Ⅱ.查阅资料:在不同温度下,纳米级Fe粉与水蒸气反应的固体产物不同,温度低于570 ℃时生成FeO,高于570 ℃时生成Fe3O4。甲同学用如图甲所示装置进行纳米级Fe粉与水蒸气反应的实验,乙同学用图乙所示的装置进行纳米级Fe粉与水蒸气的反应并验证产物。

(4)甲装置中纳米级Fe粉与水蒸气反应的化学方程式是
(5)乙同学为探究实验结束后试管内的固体物质成分,进行了下列实验:
| 实验步骤 | 实验操作 | 实验现象 |
| ① | 将反应后得到的黑色粉末X(假定为均匀的),取出少量放入另一试管中,加入少量盐酸,微热 | 黑色粉末逐渐溶解,溶液呈浅绿色;有少量气泡产生 |
| ② | 向实验①得到的溶液中滴加几滴KSCN溶液,振荡 | 溶液没有出现红色 |
根据以上实验,乙同学认为该条件下反应的固体产物为FeO。丙同学认为乙同学的结论不正确,他的理由是
(6)丁同学称取5.60 g Fe粉,用乙装置反应一段时间后,停止加热。将试管内的固体物质在干燥器中冷却后,称得质量为6.88 g,则丁同学实验后的固体物质中氧化物的质量分数为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】实验室模拟合成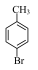 和CH3CH2CH2Br的方法如图1。
和CH3CH2CH2Br的方法如图1。
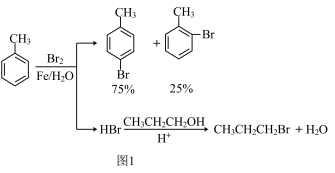
已知:甲苯和液溴在有少量水存在时也能反应(如图2):
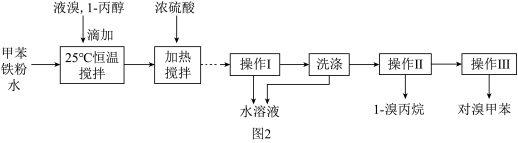
实验室模拟合成对溴甲苯和1-溴丙烷的流程和相关数据如表:
(1)实验室存放液溴的试剂瓶需密闭,同时瓶中要加入____ ,以减少溴的挥发.写出甲苯和液溴反应生成对溴甲苯的化学方程式___ 。
(2)反应装置如图3所示:
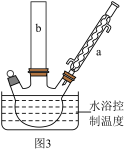
①图中玻璃仪器a的名称是____ ,方块b中为某玻璃仪器,其名称是___ 。
②三颈烧瓶中开始加入了甲苯、铁粉和水。加入的适量水的作用是:易于控制温度和____ ,加热搅拌操作中加入浓硫酸,完成1-丙醇的取代反应,浓硫酸的作用是____ 。
(3)操作I的名称是___ ,操作Ⅲ的名称是___ 。
 和CH3CH2CH2Br的方法如图1。
和CH3CH2CH2Br的方法如图1。
已知:甲苯和液溴在有少量水存在时也能反应(如图2):

实验室模拟合成对溴甲苯和1-溴丙烷的流程和相关数据如表:
| 物质 | 甲苯 | 1-丙醇 | 1-溴丙烷 | 对溴甲苯 | 邻溴甲苯 |
| 沸点(℃) | 110.8 | 97.2 | 71 | 184.3 | 181.7 |
(2)反应装置如图3所示:

①图中玻璃仪器a的名称是
②三颈烧瓶中开始加入了甲苯、铁粉和水。加入的适量水的作用是:易于控制温度和
(3)操作I的名称是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】重铬酸铵[(NH4)2Cr2O7]可用作媒染剂和有机合成催化剂,具有强氧化性。实验室将NH3通入重铬酸(H2Cr2O7)溶液中制备[(NH4)2Cr2O7]的装置如图所示(夹持装置略)。回答下列问题:
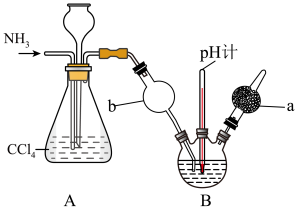
已知: (橙色)+H2O⇌2
(橙色)+H2O⇌2 (黄色)+2H+。
(黄色)+2H+。
(1)仪器a的名称是_______ ,A装置的作用为_______ 。
(2)在试管中加入少量(NH4)2Cr2O7固体,加水溶解,再滴加足量KOH浓溶液,振荡,微热,观察到的主要现象是_______ 。
(3)实验室常用甲醛法测定含(NH4)2Cr2O7的产品中(NH4)2Cr2O7的质量分数,其反应原理为2Ba2++ +H2O=2BaCrO4+2H+、4
+H2O=2BaCrO4+2H+、4 +6HCHO=(CH2)6N4H++6H2O+3H+,然后用NaOH标准溶液滴定反应生成的酸。
+6HCHO=(CH2)6N4H++6H2O+3H+,然后用NaOH标准溶液滴定反应生成的酸。
实验步骤:
I.称取样品12.00g,配成250mL溶液。
II.量取25.00mL样品溶液,用氯化钡溶液使Cr2O72-完全沉淀后,加入足量的20%中性甲醛溶液,摇匀,静置5min。
III.以酚酞作指示剂,用1.00mol·L-1的NaOH标准溶液滴定,记录数据。
IV.重复步骤II、III2~3次,处理数据。
①滴定终点的颜色变化为_______ 。
②用_______ (填“酸式”或“碱式”)滴定管量取25.00mL样品溶液于250mL锥形瓶中。
③与NaOH反应时,1mol(CH2)6N4H+与1molH+相当,步骤III中(CH2)6N4H+与NaOH发生反应的离子方程式是_______ 。
④若实验平均消耗NaOH溶液的体积为16.00mL,则所得产物中(NH4)2Cr2O7(摩尔质量为252g·mol-1)的质量分数为_______ %。
⑤若滴定终点时仰视读数,则测定的质量分数将_______ (填“偏大”、“偏小”或“不变”)。

已知:
 (橙色)+H2O⇌2
(橙色)+H2O⇌2 (黄色)+2H+。
(黄色)+2H+。(1)仪器a的名称是
(2)在试管中加入少量(NH4)2Cr2O7固体,加水溶解,再滴加足量KOH浓溶液,振荡,微热,观察到的主要现象是
(3)实验室常用甲醛法测定含(NH4)2Cr2O7的产品中(NH4)2Cr2O7的质量分数,其反应原理为2Ba2++
 +H2O=2BaCrO4+2H+、4
+H2O=2BaCrO4+2H+、4 +6HCHO=(CH2)6N4H++6H2O+3H+,然后用NaOH标准溶液滴定反应生成的酸。
+6HCHO=(CH2)6N4H++6H2O+3H+,然后用NaOH标准溶液滴定反应生成的酸。实验步骤:
I.称取样品12.00g,配成250mL溶液。
II.量取25.00mL样品溶液,用氯化钡溶液使Cr2O72-完全沉淀后,加入足量的20%中性甲醛溶液,摇匀,静置5min。
III.以酚酞作指示剂,用1.00mol·L-1的NaOH标准溶液滴定,记录数据。
IV.重复步骤II、III2~3次,处理数据。
①滴定终点的颜色变化为
②用
③与NaOH反应时,1mol(CH2)6N4H+与1molH+相当,步骤III中(CH2)6N4H+与NaOH发生反应的离子方程式是
④若实验平均消耗NaOH溶液的体积为16.00mL,则所得产物中(NH4)2Cr2O7(摩尔质量为252g·mol-1)的质量分数为
⑤若滴定终点时仰视读数,则测定的质量分数将
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
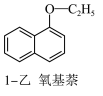
【推荐3】1−乙氧基萘常用作香料,也可合成其他香料。实验室制备1−乙氧基萘的过程如下:
 +CH3CH2OH
+CH3CH2OH
 +H2O
+H2O
已知:1−萘酚的性质与苯酚相似,有难闻的苯酚气味。相关物质的物理常数:
(1)将一定量 1−萘酚溶于无水乙醇中,并加入少量浓硫酸混合。将混合液置于如图所示的容器中加热充分反应。实验中使用过量乙醇的原因是__________ 。
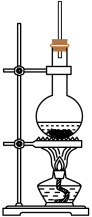
(2)装置中长玻璃管的作用是:______ 。
(3)该反应不能用实验室制备乙酸乙酯的装置,简述理由____________ ;
(4)反应结束,需要提纯产物,在下面的横线上填上相应操作的名称:倒入冷水,碱洗并_______ → 水洗并_______ →加入CaCl2干燥并______ →___________ 。
 +CH3CH2OH
+CH3CH2OH
 +H2O
+H2O已知:1−萘酚的性质与苯酚相似,有难闻的苯酚气味。相关物质的物理常数:
| 物质 | 相对分子质量 | 状态 | 熔点(℃) | 沸点(℃) | 溶解度 | |
| 水 | 乙醇 | |||||
| 1−萘酚 | 144 | 无色或黄色菱形结晶或粉末 | 96℃ | 278℃ | 微溶于水 | 易溶于乙醇 |
| 1−乙氧基萘 | 172 | 无色液体 | 5.5℃ | 267℃ | 不溶于水 | 易溶于乙醇 |
| 乙醇 | 46 | 无色液体 | −114.1℃ | 78.5℃ | 任意比混溶 | |

(2)装置中长玻璃管的作用是:
(3)该反应不能用实验室制备乙酸乙酯的装置,简述理由
(4)反应结束,需要提纯产物,在下面的横线上填上相应操作的名称:倒入冷水,碱洗并
您最近一年使用:0次