已知有一白色粉末是由Na2CO3、NaCl、Na2SO4、CuSO4、MgCl2中的一种或几种组成。欲探究这一粉末的组成,甲同学做了如下实验:
①取少量粉末,加水溶解,得无色透明溶液;
②取①中溶液少量,加入NaOH溶液,无明显现象发生;
③另取少量粉末,加入稀盐酸,无明显现象发生。
(1)根据实验①,能得到的结论是__________ 。
(2)甲同学根据以上实验现象,推测这一粉末的可能组成是__________ 。
(3)乙同学在甲同学实验基础上设计了后续实验,确认该粉末只含有Na2SO4,请你在下表中填写乙同学所做的实验。[可供选择的试剂有:BaCl2溶液、AgNO3溶液、稀HNO3、NaOH溶液、Na2CO3溶液、Ba(NO3)2溶液、稀盐酸]
注:填写实验现象、离子方程式和结论要与相应的实验步骤一一对应。
①取少量粉末,加水溶解,得无色透明溶液;
②取①中溶液少量,加入NaOH溶液,无明显现象发生;
③另取少量粉末,加入稀盐酸,无明显现象发生。
(1)根据实验①,能得到的结论是
(2)甲同学根据以上实验现象,推测这一粉末的可能组成是
(3)乙同学在甲同学实验基础上设计了后续实验,确认该粉末只含有Na2SO4,请你在下表中填写乙同学所做的实验。[可供选择的试剂有:BaCl2溶液、AgNO3溶液、稀HNO3、NaOH溶液、Na2CO3溶液、Ba(NO3)2溶液、稀盐酸]
| 实验步骤 | 实验现象 | 反应的离子方程式和结论 |
更新时间:2018-12-26 22:25:59
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
【推荐1】三氧化硫(SO3)是生产硫酸重要的中间产物,熔点16.8℃,沸点44.8℃,与水反应的化学方程式为SO3+H2O=H2SO4。某小组设计了如图实验装置制备并吸收SO3(夹持仪器略)。回答下列问题:
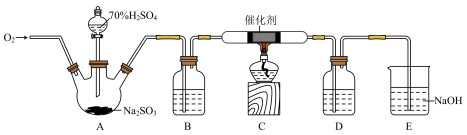
(1)盛放70%H2SO4的仪器名称是________ ,A中制备SO2的化学方程式为_________ 。
(2)装置B、D中盛放的试剂相同,该试剂是___________ 。
(3)O2除作反应物外,另一个作用是________ ,C中发生反应的化学方程式为________ 。
(4)对装置E中吸收液的成分进行探究,完成下表实验过程(限选试剂:稀盐酸、稀硫酸、稀硝酸、MgCl2溶液、BaCl2溶液、酸性KMnO4溶液、品红溶液、石蕊溶液)

(1)盛放70%H2SO4的仪器名称是
(2)装置B、D中盛放的试剂相同,该试剂是
(3)O2除作反应物外,另一个作用是
(4)对装置E中吸收液的成分进行探究,完成下表实验过程(限选试剂:稀盐酸、稀硫酸、稀硝酸、MgCl2溶液、BaCl2溶液、酸性KMnO4溶液、品红溶液、石蕊溶液)
| 操作步骤 | 实验现象 | 结论 |
| 取少量吸收液于试管中,滴加几滴MgCl2溶液 | 有白色沉淀生成 | 吸收液中含有NaOH |
| 取少量吸收液于试管中,滴加几滴酸性KMnO4溶液 | ① | 吸收液中含有② |
| 取少量吸收液于试管中,③ | ④ | 吸收液中含有Na2SO4 |
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】某无色透明溶液中可能含有 、
、 、
、 、
、 、
、 、
、 中的几种。兴趣小组同学为确定其成分,进行如下实验:
中的几种。兴趣小组同学为确定其成分,进行如下实验:
①用pH试纸对溶液进行测试,结果表明溶液显酸性;
②取少量溶液于试管中,加入过量 溶液,有白色沉淀生成,再加入稀硝酸,沉淀不溶解,过滤;
溶液,有白色沉淀生成,再加入稀硝酸,沉淀不溶解,过滤;
③取少量实验②中的滤液于试管中,加入 溶液,有白色沉淀生成,再加入稀硝酸,沉淀不溶解。
溶液,有白色沉淀生成,再加入稀硝酸,沉淀不溶解。
回答下列问题:
(1)该溶液中肯定含有的离子是___________ ,肯定不含有的离子是___________ ,可能含有的离子是___________ 。
(2)步骤②中发生反应的离子方程式为___________ 。
(3)若要进一步检验可能含有的离子是否存在,可采取的方法是___________ 。
 、
、 、
、 、
、 、
、 、
、 中的几种。兴趣小组同学为确定其成分,进行如下实验:
中的几种。兴趣小组同学为确定其成分,进行如下实验:①用pH试纸对溶液进行测试,结果表明溶液显酸性;
②取少量溶液于试管中,加入过量
 溶液,有白色沉淀生成,再加入稀硝酸,沉淀不溶解,过滤;
溶液,有白色沉淀生成,再加入稀硝酸,沉淀不溶解,过滤;③取少量实验②中的滤液于试管中,加入
 溶液,有白色沉淀生成,再加入稀硝酸,沉淀不溶解。
溶液,有白色沉淀生成,再加入稀硝酸,沉淀不溶解。回答下列问题:
(1)该溶液中肯定含有的离子是
(2)步骤②中发生反应的离子方程式为
(3)若要进一步检验可能含有的离子是否存在,可采取的方法是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】先有一瓶无色澄清溶液,可能由Na+、K+、NH4+、Fe2+、SO42-、I-、CO32-、Cl-、SO32-、MnO4-中的几种组成,请根据以下实验步骤及现象回答下列问题:
步骤一:取适量待测液,加入NaOH溶液并加热,得到溶液A,并产生刺激性气味的气体;
步骤二:向溶液A中加入足量稀盐酸和BaCl2溶液,得到溶液B、白色沉淀及有刺激性气味的气体;
步骤三:向溶液B中通入适量Cl2,得到黄褐色溶液C。
(1)下列有关该溶液说法正确的是________________ (填字母)。
A.一定存在SO42-、I-、NH4+、SO32-
B.一定不存在Fe2+、CO32-、MnO4-
C.可能存在CO32-、Cl-、Na+、K+、
D.可用AgNO3溶液确认原溶液中是否存在Cl-
(2)步骤三得到黄褐色溶液的离子方程式是____________________ 。
(3)若向原溶液中先加入足量的盐酸,再加入足量的______________ (填化学式)并加热,也能得出步骤一、步骤二相同的结论。
(4)对于溶液中还可能存在的阳离子,确认其存在的实验方法是__________________ 。
步骤一:取适量待测液,加入NaOH溶液并加热,得到溶液A,并产生刺激性气味的气体;
步骤二:向溶液A中加入足量稀盐酸和BaCl2溶液,得到溶液B、白色沉淀及有刺激性气味的气体;
步骤三:向溶液B中通入适量Cl2,得到黄褐色溶液C。
(1)下列有关该溶液说法正确的是
A.一定存在SO42-、I-、NH4+、SO32-
B.一定不存在Fe2+、CO32-、MnO4-
C.可能存在CO32-、Cl-、Na+、K+、
D.可用AgNO3溶液确认原溶液中是否存在Cl-
(2)步骤三得到黄褐色溶液的离子方程式是
(3)若向原溶液中先加入足量的盐酸,再加入足量的
(4)对于溶液中还可能存在的阳离子,确认其存在的实验方法是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】碳酸钠(Na2CO3)和碳酸氢钠(NaHCO3)都可作为食用碱。

(1)用右图装置分别加热上述两种固体,当观察到澄清石灰水变浑浊时,则试管中受热的固体是_________ 。通过本实验证明,这两种固体对热的稳定性是Na2CO3 ________ 于(选填“强”或“弱”)NaHCO3。
(2)若分别向碳酸钠溶液和碳酸氢钠溶液中滴加足量稀盐酸,都能 观察到的现象是__________________ ,其中碳酸氢钠和稀盐酸反应的化学方程式为_______________________________ 。
(3)钠的化合物中,除了碳酸钠和碳酸氢钠外,还有_________ 、_________ 等。

(1)用右图装置分别加热上述两种固体,当观察到澄清石灰水变浑浊时,则试管中受热的固体是
(2)若分别向碳酸钠溶液和碳酸氢钠溶液中滴加足量稀盐酸,
(3)钠的化合物中,除了碳酸钠和碳酸氢钠外,还有
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】今有碱金属的两种碳酸盐和碱土金属(镁、钙等二价金属)的一种不溶性碳酸盐(碱式盐)组成的混合物。取7.560g该混合物与过量盐酸完全反应,放出CO2体积为1.344L(标准状况)。另取等质量的原混合物加水搅拌,可虑出不溶性盐1.420g
(1)过滤后1/10体积的滤液,向其中缓慢滴加浓度为0.2500mol/L的盐酸,并同时记录放出的CO2的体积(标准状况)和消耗盐酸的体积,得到如图所示的曲线。

写出向滤液中缓慢滴加盐酸的有关化学方程式(写离子方程式不给分):_______ 、_______ 。
(2)将滤出的不溶性盐(420g)投入到浓度为2.500mol/L盐酸中,当反应完全时,耗去16.00mL盐酸。写出原不溶性碳酸盐与盐酸反应的离子方程式:_______ 。
(1)过滤后1/10体积的滤液,向其中缓慢滴加浓度为0.2500mol/L的盐酸,并同时记录放出的CO2的体积(标准状况)和消耗盐酸的体积,得到如图所示的曲线。

写出向滤液中缓慢滴加盐酸的有关化学方程式(写离子方程式不给分):
(2)将滤出的不溶性盐(420g)投入到浓度为2.500mol/L盐酸中,当反应完全时,耗去16.00mL盐酸。写出原不溶性碳酸盐与盐酸反应的离子方程式:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】某小组同学进行 和
和 性质的探究,实验如下(夹持装置已略去,气密性已检验)。
性质的探究,实验如下(夹持装置已略去,气密性已检验)。
【实验一】
(1)实验I,能够证明 的热稳定性强于
的热稳定性强于 的证据是
的证据是_______ 。
(2)实验II,方框中为洗气装置,请将该装置补充完整_______ 。
(3)实验II,试剂a为_______ 。
(4)实验II,持续一段时间后,观察到饱和 溶液中有细小晶体析出,用化学方程式表示产生细小晶体的原因:
溶液中有细小晶体析出,用化学方程式表示产生细小晶体的原因:_______ 。
【实验二】
【查阅资料】pH越小, 越小,溶液碱性越弱。
越小,溶液碱性越弱。
【实验过程】
【分析与解释】
(5)实验I中,溶解时吸收热量的物质是_______ (写化学式)。
(6)澄清石灰水显碱性的原因用电离方程式表示为_______ 。
(7)实验II中, 溶液和澄清石灰水反应的离子方程式为
溶液和澄清石灰水反应的离子方程式为_______ , 未参与该反应的实验证据是
未参与该反应的实验证据是_______ 。
(8)实验II中,滴加 溶液的pH变化与滴加
溶液的pH变化与滴加 溶液的有明显差异,原因是滴加
溶液的有明显差异,原因是滴加 ,溶液的烧杯中,参与反应的离子有
,溶液的烧杯中,参与反应的离子有_______ 。
 和
和 性质的探究,实验如下(夹持装置已略去,气密性已检验)。
性质的探究,实验如下(夹持装置已略去,气密性已检验)。【实验一】
| 实验Ⅰ | 实验Ⅱ |
 |  |
 的热稳定性强于
的热稳定性强于 的证据是
的证据是(2)实验II,方框中为洗气装置,请将该装置补充完整
(3)实验II,试剂a为
(4)实验II,持续一段时间后,观察到饱和
 溶液中有细小晶体析出,用化学方程式表示产生细小晶体的原因:
溶液中有细小晶体析出,用化学方程式表示产生细小晶体的原因:【实验二】
【查阅资料】pH越小,
 越小,溶液碱性越弱。
越小,溶液碱性越弱。【实验过程】
| 编号 | 实验操作 | 实验数据 |
| 实验I | 测量下述实验过程的温度变化 |  |
| 实验操作 | 实验数据 | |
| 实验II | 测量下述实验过程的pH变化 | ②和③中均产生白色沉淀。 各烧杯中pH变化如下图所示  |
(5)实验I中,溶解时吸收热量的物质是
(6)澄清石灰水显碱性的原因用电离方程式表示为
(7)实验II中,
 溶液和澄清石灰水反应的离子方程式为
溶液和澄清石灰水反应的离子方程式为 未参与该反应的实验证据是
未参与该反应的实验证据是(8)实验II中,滴加
 溶液的pH变化与滴加
溶液的pH变化与滴加 溶液的有明显差异,原因是滴加
溶液的有明显差异,原因是滴加 ,溶液的烧杯中,参与反应的离子有
,溶液的烧杯中,参与反应的离子有
您最近一年使用:0次
【推荐1】已知B是常见金属单质,E为常见非金属单质,H常温下为无色液体,C的浓溶液在加热时才与D反应。根据下列框图所示,试回答:
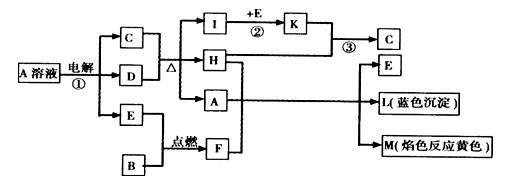
(1)写出化学式:A_______ ;E_______ ;L_______ 。
(2)反应①的离子方程式:_______ 。
(3)反应②,工业上采取的反应条件是_______ 。
(4)反应③,工业上采取的操作不是K直接与H反应,原因是_______ 。
(5)每生成1 mol K,反应放出98.3 kJ热量,该反应的热化学方程式为:_______ 。

(1)写出化学式:A
(2)反应①的离子方程式:
(3)反应②,工业上采取的反应条件是
(4)反应③,工业上采取的操作不是K直接与H反应,原因是
(5)每生成1 mol K,反应放出98.3 kJ热量,该反应的热化学方程式为:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】硫酸铜是一种应用极其广泛的化工原料。实验中可将适量浓硝酸分多次加入到铜粉与稀硫酸的混合物中,加热使之反应完全,通过蒸发、结晶得到硫酸铜晶体(装置如图1所示)。
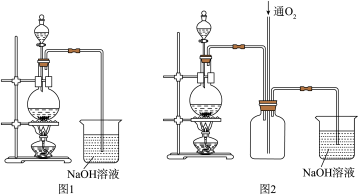
(1)配制质量分数20%的硫酸需要100mL98%的浓硫酸(密度为1.84g/cm3)和_____ mL蒸馏水。配制所需仪器除烧杯、量筒、胶头滴管外,还需要的仪器_____ 。
(2)图1烧瓶中发生的离子反应方程式为:_____ 。
(3)图2是图1的改进装置,其优点有:①_____ ;②_____ 。
为符合绿色化学的要求,某研究性学习小组进行如下设计:
方案1:以空气为氧化剂。将铜粉在某仪器A中反复灼烧,使铜与空气充分反应生成氧化铜,再将氧化铜与稀硫酸反应。反应后,过滤、蒸发、结晶等,用少量95%的酒精淋洗后晾干,得CuSO4·5H2O 晶体。
方案2:将空气或氧气直接通入到铜粉与稀硫酸的混合物中,发现在常温下几乎不反应。向反应液中加Fe2(SO4)3,即发生反应。反应完全后向其中加物质甲、物质乙,取样检验后,过滤、蒸发、结晶,滤渣可循环使用。[已知Fe(OH)2、Fe(OH)3和Cu(OH)2完全沉淀时的pH分别为9.6、3.7、6.4。]
(4)方案1中的A仪器名称是_____ 。晶体采用酒精淋洗的优点是_____ 。
(5)方案2中物质甲可以是_____ (选填答案编号,下同),物质乙可以是_____ 。
a.Cu b.CuCO3 c.CuO d.氨水 e.氯水 f 双氧水
取样检验是为了确认Fe3+是否除尽。有同学设计了以下两种方法:
方法①:取样于试管→滴加KSCN溶液;方法②:径向层析→喷KSCN溶液。
指出你认为不合理的方法及存在的问题_____ 。
(6)用铜粉制硫酸,上述方案1、方案2都不是十分理想,一种更符合绿色化学理念的是在氧气存在时用热稀硫酸与铜反应,其化学方程式是:_____ 。

(1)配制质量分数20%的硫酸需要100mL98%的浓硫酸(密度为1.84g/cm3)和
(2)图1烧瓶中发生的离子反应方程式为:
(3)图2是图1的改进装置,其优点有:①
为符合绿色化学的要求,某研究性学习小组进行如下设计:
方案1:以空气为氧化剂。将铜粉在某仪器A中反复灼烧,使铜与空气充分反应生成氧化铜,再将氧化铜与稀硫酸反应。反应后,过滤、蒸发、结晶等,用少量95%的酒精淋洗后晾干,得CuSO4·5H2O 晶体。
方案2:将空气或氧气直接通入到铜粉与稀硫酸的混合物中,发现在常温下几乎不反应。向反应液中加Fe2(SO4)3,即发生反应。反应完全后向其中加物质甲、物质乙,取样检验后,过滤、蒸发、结晶,滤渣可循环使用。[已知Fe(OH)2、Fe(OH)3和Cu(OH)2完全沉淀时的pH分别为9.6、3.7、6.4。]
(4)方案1中的A仪器名称是
(5)方案2中物质甲可以是
a.Cu b.CuCO3 c.CuO d.氨水 e.氯水 f 双氧水
取样检验是为了确认Fe3+是否除尽。有同学设计了以下两种方法:
方法①:取样于试管→滴加KSCN溶液;方法②:径向层析→喷KSCN溶液。
指出你认为不合理的方法及存在的问题
(6)用铜粉制硫酸,上述方案1、方案2都不是十分理想,一种更符合绿色化学理念的是在氧气存在时用热稀硫酸与铜反应,其化学方程式是:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】为测定CuSO4溶液的浓度,某同学设计了一个方案。回答下列问题:
实验原理: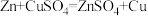 ,
,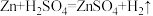

实验步骤:
①按图安装装置(夹持仪器略去)
②……
③在仪器A、B、C、D、E…中加入图示的试剂
④调整D、E中两液面相平,使D中液面保持在0或略低于0刻度位置,读数并记录。
⑤将CuSO4溶液滴入A中搅拌,反应完成后,再滴加稀硫酸至体系不再有气体产生。
⑥待体系恢复到室温,移动E管,保持D、E中两液面相平,读数并记录。
⑦处理数据
(1)仪器A的名称________ 。
(2)步骤②为__________ 。
(3)步骤⑥需保证体系恢复到室温的原因是________ (填序号)。
a.反应热受温度影响
b.气体密度受温度影响
c.反应速率受温度影响
(4)Zn粉质量为ag,若测得H2体积为bmL,已知实验条件下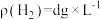 ,则c(CuSO4)
,则c(CuSO4)______ mol/L(列出计算表达式)。
(5)若步骤⑥E管液面高于D管,未调液面即读数,则测c(CuSO4)________ (填“偏高”、“偏低”或“无影响”)。
(6)是否能用同样的装置和方法测定MgSO4溶液的浓度:_________ (填“是”或“否”)。
实验原理:
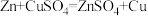 ,
,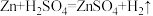

实验步骤:
①按图安装装置(夹持仪器略去)
②……
③在仪器A、B、C、D、E…中加入图示的试剂
④调整D、E中两液面相平,使D中液面保持在0或略低于0刻度位置,读数并记录。
⑤将CuSO4溶液滴入A中搅拌,反应完成后,再滴加稀硫酸至体系不再有气体产生。
⑥待体系恢复到室温,移动E管,保持D、E中两液面相平,读数并记录。
⑦处理数据
(1)仪器A的名称
(2)步骤②为
(3)步骤⑥需保证体系恢复到室温的原因是
a.反应热受温度影响
b.气体密度受温度影响
c.反应速率受温度影响
(4)Zn粉质量为ag,若测得H2体积为bmL,已知实验条件下
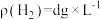 ,则c(CuSO4)
,则c(CuSO4)(5)若步骤⑥E管液面高于D管,未调液面即读数,则测c(CuSO4)
(6)是否能用同样的装置和方法测定MgSO4溶液的浓度:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】塑化剂DBP(邻苯二甲酸二丁酯)主要应用于PVC等合成材料中作软化剂。反应原理为:

实验步骤如下:
步骤1:在三颈瓶中放入14.8g邻苯二甲酸酐、25mL正丁醇、4滴浓硫酸,开动搅拌器b(反应装置如图)。
步骤2:缓缓加热至邻苯二甲酸酐固体消失,升温至沸腾。
步骤3:等酯化到一定程度时,升温至150℃
步骤4:冷却,将三颈瓶中的液体倒入分漏斗中,用饱和食盐水和5%碳酸钠洗涤。
步骤5:减压蒸馏,收集200~210℃2666Pa馏分,即得DBP产品
(1)浓硫酸的作用______________________ ,搅拌器的作用______________________ 。
(2)反应过程中正丁醇过量的目的是___________________________________________ 。

(3)图中仪器a的名称是分水器,试分析它的作用是_____________________________ 。
步骤3中确定有大量酯生成的依据是_______________________________________ 。
(4)碳酸钠溶液洗涤的目的是_________________________________________________ 。
用减压蒸馏的目的是_____________________________________________________ 。
(5)写出正丁醇在135℃生成醚的反应方程式___________________________________ 。
写出DBP在氢氧化钠溶液中水解的方程式_______________________________ 。

实验步骤如下:
步骤1:在三颈瓶中放入14.8g邻苯二甲酸酐、25mL正丁醇、4滴浓硫酸,开动搅拌器b(反应装置如图)。
步骤2:缓缓加热至邻苯二甲酸酐固体消失,升温至沸腾。
步骤3:等酯化到一定程度时,升温至150℃
步骤4:冷却,将三颈瓶中的液体倒入分漏斗中,用饱和食盐水和5%碳酸钠洗涤。
步骤5:减压蒸馏,收集200~210℃2666Pa馏分,即得DBP产品
(1)浓硫酸的作用
(2)反应过程中正丁醇过量的目的是

(3)图中仪器a的名称是分水器,试分析它的作用是
步骤3中确定有大量酯生成的依据是
(4)碳酸钠溶液洗涤的目的是
用减压蒸馏的目的是
(5)写出正丁醇在135℃生成醚的反应方程式
写出DBP在氢氧化钠溶液中水解的方程式
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】我国自主开发的“钛战甲”是一种钛合金材料,为深潜万米的“奋斗者”号建造了世界最大、搭载人数最多的潜水器载人舱球壳。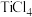 是制备钛及其化合物的重要中间体。可利用下列装置在实验空制备
是制备钛及其化合物的重要中间体。可利用下列装置在实验空制备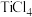 (夹持装置略去):
(夹持装置略去):
已知:①
②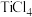 为无色或淡黄色液体,熔点为-30℃,沸点为136.4℃,极易与水反应
为无色或淡黄色液体,熔点为-30℃,沸点为136.4℃,极易与水反应
③ 的盐酸溶液可吸收CO而生成黑色颗粒Pd
的盐酸溶液可吸收CO而生成黑色颗粒Pd

回答下列问题:
(1)盛放浓盐酸的仪器名称为_______ ,圆底烧瓶内所装试剂可为_______ 。
① ②
② ③
③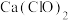 ④浓
④浓
(2)装置的连接顺序为_______ (D装置可重复使用)
(3)对于实验过程的控制,开始操作为_______ (填①或②),实验结束的操作为_______ (填③或④)
①先打开分液漏斗活塞,一段时间后,再陶瓷管通电加热
②先陶瓷管通电加热,一段时间后,再打开分液漏斗活塞
③先陶瓷管断电停止加热,一段时间后,再关闭分液漏斗活塞
④先关闭分液漏斗活塞,一段时间后,再陶瓷管断电停止加热
(4)装置C左边进气的细长导管作用为_______ 。
(5)吸收尾气中CO的化学方程式_______ 。
(6)所得的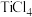 可用Mg制Ti,该过程可在
可用Mg制Ti,该过程可在_______ 气氛围保护下进行。
①氯气 ②氧气 ③水蒸气 ④氩气
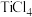 是制备钛及其化合物的重要中间体。可利用下列装置在实验空制备
是制备钛及其化合物的重要中间体。可利用下列装置在实验空制备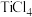 (夹持装置略去):
(夹持装置略去):已知:①

②
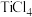 为无色或淡黄色液体,熔点为-30℃,沸点为136.4℃,极易与水反应
为无色或淡黄色液体,熔点为-30℃,沸点为136.4℃,极易与水反应③
 的盐酸溶液可吸收CO而生成黑色颗粒Pd
的盐酸溶液可吸收CO而生成黑色颗粒Pd
回答下列问题:
(1)盛放浓盐酸的仪器名称为
①
 ②
② ③
③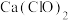 ④浓
④浓
(2)装置的连接顺序为
(3)对于实验过程的控制,开始操作为
①先打开分液漏斗活塞,一段时间后,再陶瓷管通电加热
②先陶瓷管通电加热,一段时间后,再打开分液漏斗活塞
③先陶瓷管断电停止加热,一段时间后,再关闭分液漏斗活塞
④先关闭分液漏斗活塞,一段时间后,再陶瓷管断电停止加热
(4)装置C左边进气的细长导管作用为
(5)吸收尾气中CO的化学方程式
(6)所得的
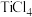 可用Mg制Ti,该过程可在
可用Mg制Ti,该过程可在①氯气 ②氧气 ③水蒸气 ④氩气
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐3】“烂版液”是制印刷锌板时,用稀硝酸腐蚀锌板后得到的“废液”(含有少量的Cl-、Fe3+),某化学兴趣小组拟用“烂版液”制取Zn(NO3)2·6H2O的过程如下:
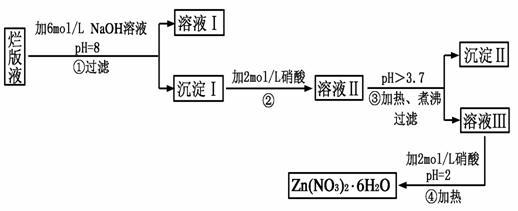
已知:Zn(NO3)2·6H2O是一种无色晶体,水溶液呈酸性,Zn(NO3)2能与碱反应,得到的产物具有两性。
(1)“烂版液”中溶质的主要成分是______ (填化学式),若稀硝酸腐蚀锌板产生的气体为N2O,写出稀硝酸腐蚀锌板反应的主要化学方程式______ 。
(2)在操作①中保持pH=8的目的是______ 。
(3)沉淀Ⅰ的主要成分是______ 。
(4)操作③中加热、煮沸的目的是______ ;此步骤操作的理论依据是______ 。
(5)操作④保持pH=2的目的是______ ;此步骤操作中所用的主要仪器是______ 。

已知:Zn(NO3)2·6H2O是一种无色晶体,水溶液呈酸性,Zn(NO3)2能与碱反应,得到的产物具有两性。
(1)“烂版液”中溶质的主要成分是
(2)在操作①中保持pH=8的目的是
(3)沉淀Ⅰ的主要成分是
(4)操作③中加热、煮沸的目的是
(5)操作④保持pH=2的目的是
您最近一年使用:0次



