按如图所示装置进行实验,填写有关现象及化学方程式。

(1) D中的现象是______________ ,E中收集的气体是_________ (填名称)。
(2) A中发生反应的化学方程式为____________________________________________ 。
(3) C中发生反应的化学方程式为__________________________________________ 。

(1) D中的现象是
(2) A中发生反应的化学方程式为
(3) C中发生反应的化学方程式为
更新时间:2019-01-01 11:21:26
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】有A、B、C、D、E五种短周期元素,其原子序数依次增大。在周期表中A的原子半径最小,B的主族序数是周期序数的2倍,D是地壳中含量最多的元素,在周期表中A和E同主族,回答下列问题:
(1)化合物BD2的电子式是_______ 。
(2)化合物CA3的结构式为_______ 。
(3)用电子式表示化合物A2D的形成过程:_______ 。
(4)将物质的量比为1:1的CO2和H2O组成的混合气通入到a mol的过量固体E2D2中,将反应后的固体混合物加入到500 mL 1 mol·L-1盐酸中,则产生无色混合气体的体积在标准状况下为b L,反应后溶液呈中性,则a=_______ ,b=_______ 。
(1)化合物BD2的电子式是
(2)化合物CA3的结构式为
(3)用电子式表示化合物A2D的形成过程:
(4)将物质的量比为1:1的CO2和H2O组成的混合气通入到a mol的过量固体E2D2中,将反应后的固体混合物加入到500 mL 1 mol·L-1盐酸中,则产生无色混合气体的体积在标准状况下为b L,反应后溶液呈中性,则a=
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】A、B、C、D是按原子序数由小到大排列的前20号元素的单质。B、E均为组成空气的成分。F的焰色反应呈黄色。在G中,非金属元素与金属元素的原子个数比为1:2。在一定条件下,各物质之间的相互转化关系如右(部分产物未列出):
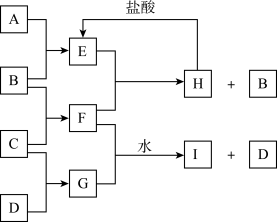
(1)A是_____ ,C是______ (填元素名称)。
(2)H与盐酸反应生成 E 的化学方程式是_________ 。
(3)E与F反应的化学方程式是___________ 。
(4)F与G的水溶液反应生成I和D的离子方程式是_____________ 。

(1)A是
(2)H与盐酸反应生成 E 的化学方程式是
(3)E与F反应的化学方程式是
(4)F与G的水溶液反应生成I和D的离子方程式是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】某化学小组在实验室制取Na2O2.查阅资料可知:钠与空气在453~473K之间可生成Na2O,迅速提高温度到573~673K之间可生成Na2O2,若温度提高到733~873K之间Na2O2可分解。已知Na不与N2反应。
(1)甲组设计制取Na2O2装置如图。
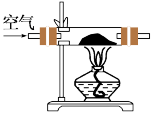
①使用该装置制取的Na2O2中可能含有的杂质为___________ 。
A.Na3N B.Na2CO3 C.Na2O D.NaOH E.NaHCO3
②该小组为测定制得的Na2O2样品的纯度,设计装置如下图。
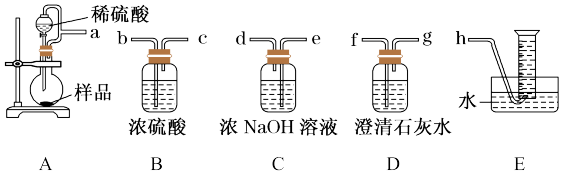
烧瓶中发生的主要反应的化学方程式是___________ 。分液漏斗和烧瓶用导管连接,其作用有两个,一是___________ ,二是防止产生实验误差,若没有该导管将导致测定结果___________ (填“偏大”、“偏小”或“无影响”)。测定装置的接口从左至右正确的连接顺序是___________ 。
(2)乙组从反应历程上分析该测定反应存在中间产物,为证明其分析的正确性,设计实验方案如下:
在上述实验中,能够证明乙组分析正确的最佳方案是___________ (填实验序号)。根据上述实验可知,反应溶液中存在的中间产物与酚酞作用的条件是___________ 。
(3)只选用上图中A,E装置(药品可重新选择),可快速准确测定样品的纯度,其选用的药品除了样品外,还应有___________ 。
(1)甲组设计制取Na2O2装置如图。

①使用该装置制取的Na2O2中可能含有的杂质为
A.Na3N B.Na2CO3 C.Na2O D.NaOH E.NaHCO3
②该小组为测定制得的Na2O2样品的纯度,设计装置如下图。

烧瓶中发生的主要反应的化学方程式是
(2)乙组从反应历程上分析该测定反应存在中间产物,为证明其分析的正确性,设计实验方案如下:
| 实验方案 | 产生的现象 |
| Ⅰ。取烧瓶中的反应液加入少量MnO2粉末 | 有大量气泡逸出 |
| Ⅱ。向NaOH稀溶液中加入2〜3滴酚酞试液,然后加入少量的反应液 | 溶液先变红后褪色 |
| Ⅲ。向反应液中加入2〜3滴酚酞试液,充分振荡,然后逐滴加入过量的NaOH稀溶液 | 开始无明显现象。加NaOH溶 液先变红后褪色 |
(3)只选用上图中A,E装置(药品可重新选择),可快速准确测定样品的纯度,其选用的药品除了样品外,还应有
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】现代工业常以氯化钠为原料制备纯碱,部分工艺流程如下:

已知反应I为: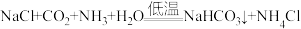
(1)从海水中获取淡水的常用方法实验操作是____ ,需要的玻璃仪器有:酒精灯、冷凝管、牛角管、锥形瓶、____ 、____ 。
(2)从溴水中获得单质溴时,采用的方法是萃取、___ 、蒸馏。下列可选作萃取剂的是___ 。
A.酒精 B.苯 C.CCl4
(3)海水中含有大量的NaCl,以及少量的 、
、 、
、 等离子。为得到纯净的饱和NaCl溶液,进行了如下操作。请补全操作步骤:
等离子。为得到纯净的饱和NaCl溶液,进行了如下操作。请补全操作步骤:
a.向浓缩后的海水中加入过量的氢氧化钠溶液后,过滤;
b.向滤液中_______ ,过滤;
c.向滤液中_______ ,过滤;
d.向滤液中加入足量的稀盐酸;
e.加热煮沸一段时间,得到饱和NaCl溶液。
(4)反应II的化学方程式是_______ 。
(5)制得的纯碱中含有少量NaCl。取5.5g纯碱样品加入足量稀硫酸,得到标准状况下1120mLCO2,则样品中纯碱的质量分数是_______ %(保留1位小数)。

已知反应I为:
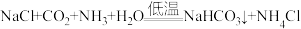
(1)从海水中获取淡水的常用方法实验操作是
(2)从溴水中获得单质溴时,采用的方法是萃取、
A.酒精 B.苯 C.CCl4
(3)海水中含有大量的NaCl,以及少量的
 、
、 、
、 等离子。为得到纯净的饱和NaCl溶液,进行了如下操作。请补全操作步骤:
等离子。为得到纯净的饱和NaCl溶液,进行了如下操作。请补全操作步骤:a.向浓缩后的海水中加入过量的氢氧化钠溶液后,过滤;
b.向滤液中
c.向滤液中
d.向滤液中加入足量的稀盐酸;
e.加热煮沸一段时间,得到饱和NaCl溶液。
(4)反应II的化学方程式是
(5)制得的纯碱中含有少量NaCl。取5.5g纯碱样品加入足量稀硫酸,得到标准状况下1120mLCO2,则样品中纯碱的质量分数是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】I.已知B为碱性氧化物,D为淡黄色固体粉末,F为医疗上治疗胃酸过多的一种药剂;物质的转化关系如图所示,请回答下列问题:
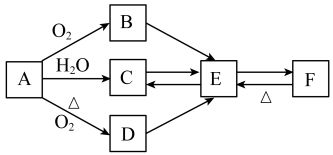
(1)请写出下列化学反应方程式
①A→C:___________ ;
②A→D:___________ ;
③D→E:___________ ;
(2)物质D中阴阳离子个数比为___________ ,其在生活中可用于___________ 。
II.用套管实验装置可以更好地比较E和F的热稳定性,其中甲试管内有沾有无水硫酸铜粉末的棉花球,实验装置如图:
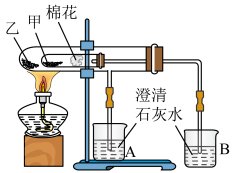
(3)实验时,应将 装进
装进___________ 试管(填“甲”或“乙”);
(4)可观察到到的现象是甲中棉花___________ (填“变白”或“变蓝”),___________ 烧杯中澄清石灰水变浑浊(填“A”或“B”);
(5)由以上实验可得热稳定性
___________  (填“>”或“<”)。
(填“>”或“<”)。

(1)请写出下列化学反应方程式
①A→C:
②A→D:
③D→E:
(2)物质D中阴阳离子个数比为
II.用套管实验装置可以更好地比较E和F的热稳定性,其中甲试管内有沾有无水硫酸铜粉末的棉花球,实验装置如图:

(3)实验时,应将
 装进
装进(4)可观察到到的现象是甲中棉花
(5)由以上实验可得热稳定性

 (填“>”或“<”)。
(填“>”或“<”)。
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】A,B、C.D、E五种物质的焰色试验都呈黄色,其中A为金属单质,B为淡黄色固体,五种物质存在如图所示的转化关系。

回答下列问题:
(1)②对应的化学方程式为___________ 。
(2)⑤对应的化学方程式为___________ 。
(3)2molB与足量的水反应时,转移的电子数目为___________ 。
(4)若D的固体中含有少量的E,则除去E的方法为___________ 。
(5)E溶液与稀HCl反应的离子方程式为___________ 。
(6)上述转化关系中,涉及氧化还原反应的是___________ (填序号)。

回答下列问题:
(1)②对应的化学方程式为
(2)⑤对应的化学方程式为
(3)2molB与足量的水反应时,转移的电子数目为
(4)若D的固体中含有少量的E,则除去E的方法为
(5)E溶液与稀HCl反应的离子方程式为
(6)上述转化关系中,涉及氧化还原反应的是
您最近一年使用:0次



