二氯化二硫( )可用作橡胶的低温硫化剂和粘结剂,在工业上具有重要的应用.某实验室研究小组通过查阅硫与氯气反应的相关资料,得知:
)可用作橡胶的低温硫化剂和粘结剂,在工业上具有重要的应用.某实验室研究小组通过查阅硫与氯气反应的相关资料,得知: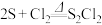 ,纯净的氯气在110~140℃时可以与硫反应得到淡红色的
,纯净的氯气在110~140℃时可以与硫反应得到淡红色的 粗产品.
粗产品.
有关物质的部分性质如下表:
现在需要利用如下仪器和药品制取纯净的氯气,并且进一步与硫反应来制备 .
.
提供的仪器:
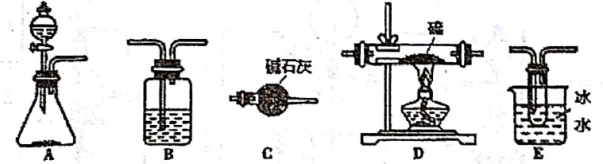
提供的药品:
浓盐酸、浓 、
、 、
、 、饱和
、饱和 溶液、碱石灰、硫磺、
溶液、碱石灰、硫磺、 溶液、冰水、饱和食盐水.
溶液、冰水、饱和食盐水.
(1)现需要使用装置A来制备氯气,写出制备 的离子方程式:
的离子方程式:______
(2)利用所提供的仪器组合实验装置,写出相应的连接顺序(仪器B可使用2次)______ ;第二次装置B中的药品是______ ;
(3) 分子中各原子均达到8电子稳定结构,写出其电子式
分子中各原子均达到8电子稳定结构,写出其电子式_______ ; 遇水剧烈反应,出现黄色浑浊,并生成两种刺激性气味的气体,写出相关化学方程式:
遇水剧烈反应,出现黄色浑浊,并生成两种刺激性气味的气体,写出相关化学方程式:______ .
(4)装置C的作用是______ .
(5)实验过程中需要控制装置D的加热温度,并且需要控制好 的通入量,原因是?
的通入量,原因是?______ .
(6)装置E中收集到的粗产品 呈淡红色,如何进一步提纯?
呈淡红色,如何进一步提纯?______ .
 )可用作橡胶的低温硫化剂和粘结剂,在工业上具有重要的应用.某实验室研究小组通过查阅硫与氯气反应的相关资料,得知:
)可用作橡胶的低温硫化剂和粘结剂,在工业上具有重要的应用.某实验室研究小组通过查阅硫与氯气反应的相关资料,得知: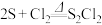 ,纯净的氯气在110~140℃时可以与硫反应得到淡红色的
,纯净的氯气在110~140℃时可以与硫反应得到淡红色的 粗产品.
粗产品.有关物质的部分性质如下表:
| 物质 | 外观(常温下) | 熔点/℃ | 沸点/℃ | 化学性质 |
 | 淡黄色固体 | 112.8 | 444.6 | 略 |
 | 淡黄色液体 |  | 135.6 | ①遇水剧烈反应,出现黄色浑浊,并生成两种刺激性气味的气体 ②能与  反应生成 反应生成 ③温度过高易分解,300℃以上完全分解 |
 | 红色液体 | 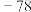 | — | 59.6℃发生完全分解,分解产物为 与 与 |
现在需要利用如下仪器和药品制取纯净的氯气,并且进一步与硫反应来制备
 .
.提供的仪器:

提供的药品:
浓盐酸、浓
 、
、 、
、 、饱和
、饱和 溶液、碱石灰、硫磺、
溶液、碱石灰、硫磺、 溶液、冰水、饱和食盐水.
溶液、冰水、饱和食盐水.(1)现需要使用装置A来制备氯气,写出制备
 的离子方程式:
的离子方程式:(2)利用所提供的仪器组合实验装置,写出相应的连接顺序(仪器B可使用2次)
(3)
 分子中各原子均达到8电子稳定结构,写出其电子式
分子中各原子均达到8电子稳定结构,写出其电子式 遇水剧烈反应,出现黄色浑浊,并生成两种刺激性气味的气体,写出相关化学方程式:
遇水剧烈反应,出现黄色浑浊,并生成两种刺激性气味的气体,写出相关化学方程式:(4)装置C的作用是
(5)实验过程中需要控制装置D的加热温度,并且需要控制好
 的通入量,原因是?
的通入量,原因是?(6)装置E中收集到的粗产品
 呈淡红色,如何进一步提纯?
呈淡红色,如何进一步提纯?
更新时间:2019-01-13 18:08:42
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】下表为元素周期表的一部分,请参照元素①~⑧在表中的位置,用化学用语回答下列问题:
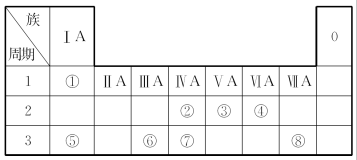
(1)⑧的气态氢化物为_________ (填电子式)
(2)⑤对应的碱为_____ (填电子式);③的最高价含氧酸_____ (填化学式)。
(3)比较⑤、⑥元素的金属性强弱________ ;并写出它们最高价氧化物的水化物反应的化学方程式__________ 。
(4)写出一种由原子序数①、③、⑧三种元素组成化合物的化学式:_______ 。

(1)⑧的气态氢化物为
(2)⑤对应的碱为
(3)比较⑤、⑥元素的金属性强弱
(4)写出一种由原子序数①、③、⑧三种元素组成化合物的化学式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】将地球储量丰富的小分子电催化转化为有高附加值的 、
、 、
、 及
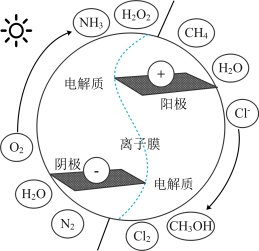
及 (如图所示)等具有巨大的经济效益和环境效益。回答下列问题:
(如图所示)等具有巨大的经济效益和环境效益。回答下列问题:
(1) 是一种绿色氧化剂,它的电子式为
是一种绿色氧化剂,它的电子式为___________ ;目前工业上采用蒽醌法生产 的原理为:
的原理为:
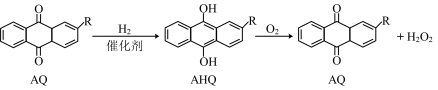 。
。
该总反应的原子利用率为___________ %;测定 的纯度可用酸性高锰酸钾溶液滴定法,该反应的离子方程式为
的纯度可用酸性高锰酸钾溶液滴定法,该反应的离子方程式为___________ 。
(2) 还原
还原 制取X(方程式中部分物质的化学计量数已略)可表示为
制取X(方程式中部分物质的化学计量数已略)可表示为
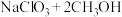


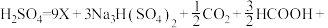

 ,则X为
,则X为___________ (填化学式)。
(3)电催化制取有高附加值物质的方法有很多。
①下列说法错误的是___________ (填标号)。
A. 及
及 电催化制
电催化制 时,
时, 在阴极区生成
在阴极区生成
B. 及
及 电催化制
电催化制 时,
时, 在阳极区生成
在阳极区生成
C.隔膜电解槽电解饱和食盐水制 时,用阴离子交换膜
时,用阴离子交换膜
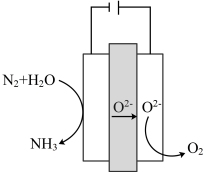
②一种合成氨的装置如图所示,阴极的电极反应式为___________ ,电解总反应为___________ 。
 、
、 、
、 及
及 (如图所示)等具有巨大的经济效益和环境效益。回答下列问题:
(如图所示)等具有巨大的经济效益和环境效益。回答下列问题:
(1)
 是一种绿色氧化剂,它的电子式为
是一种绿色氧化剂,它的电子式为 的原理为:
的原理为: 。
。该总反应的原子利用率为
 的纯度可用酸性高锰酸钾溶液滴定法,该反应的离子方程式为
的纯度可用酸性高锰酸钾溶液滴定法,该反应的离子方程式为(2)
 还原
还原 制取X(方程式中部分物质的化学计量数已略)可表示为
制取X(方程式中部分物质的化学计量数已略)可表示为
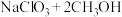


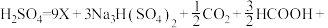

 ,则X为
,则X为(3)电催化制取有高附加值物质的方法有很多。
①下列说法错误的是
A.
 及
及 电催化制
电催化制 时,
时, 在阴极区生成
在阴极区生成B.
 及
及 电催化制
电催化制 时,
时, 在阳极区生成
在阳极区生成C.隔膜电解槽电解饱和食盐水制
 时,用阴离子交换膜
时,用阴离子交换膜②一种合成氨的装置如图所示,阴极的电极反应式为

您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】元素周期表反映了元素之间的内在联系,是研究物质性质的重要工具。如表是元素周期表的一部分。回答下列问题:
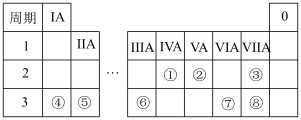
(1)上述元素①~⑧的非金属性最强的是______ (填元素符号);简单离子半径最大的是______ (填离子符号)。
(2)若元素④与⑧形成的化合物为X,用电子式表示X的形成过程:________ ;画出X中阴离子的离子结构示意图:________ 。
(3)⑦⑧两种元素的最高价氧化物的水化物酸性强弱为________ (用化学式表示)。
(4)⑥的单质与强碱反应的离子方程式为_________ 。
(5)已知⑤的单质与①的最高价氧化物Y在点燃条件下能反应生成黑色单质,推测④的单质_____ (填“能”或“不能”)与Y发生类似反应。
(6)已知铷(Rb)是37号元素,与④同主族。下列说法正确的是_______ (填字母)。
a.铷在周期表中的位置为第四周期第ⅠA族
b.铷的熔点比④对应单质的熔点低
c.⑥的简单离子与过量的RbOH反应最终会产生白色沉淀
d.RbOH的碱性比④的最高价氧化物的水化物强

(1)上述元素①~⑧的非金属性最强的是
(2)若元素④与⑧形成的化合物为X,用电子式表示X的形成过程:
(3)⑦⑧两种元素的最高价氧化物的水化物酸性强弱为
(4)⑥的单质与强碱反应的离子方程式为
(5)已知⑤的单质与①的最高价氧化物Y在点燃条件下能反应生成黑色单质,推测④的单质
(6)已知铷(Rb)是37号元素,与④同主族。下列说法正确的是
a.铷在周期表中的位置为第四周期第ⅠA族
b.铷的熔点比④对应单质的熔点低
c.⑥的简单离子与过量的RbOH反应最终会产生白色沉淀
d.RbOH的碱性比④的最高价氧化物的水化物强
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】工业上氯气用途非常广泛,回答下列问题:
(1)实验室制取氯气的化学方程式为_______ 。
(2)下表是某实验研究氯水性质实验的部分活动记录。
(3)“价态—类别”二维图是研究元素的重要方法,下图为氯及其化合物的“价态—类别”二维图。_______ ;B是家庭学校常用的消毒药品,则B是_______ (填化学式);C的焰色试验呈紫色,则C是_______ (填化学式)。
②某同学利用a. b.
b. c.酸性
c.酸性 三种溶液探究盐酸性质,试验前进行如下预测:从物质类别上看,盐酸有酸的通性,可能与
三种溶液探究盐酸性质,试验前进行如下预测:从物质类别上看,盐酸有酸的通性,可能与_______ 发生反应(填序号);从化合价角度看,盐酸的 具有
具有_______ 性,(填“氧化”或“还原”);可能与_______ 发生反应(填序号)。
(4)下图是用强光照射密闭广口瓶中新制氯水时,用数字化传感器采集的图像,下列纵坐标代表的物理量与图像相符的是_______ 。
c.溶液的导电能力 d.溶液的漂白能力
(1)实验室制取氯气的化学方程式为
(2)下表是某实验研究氯水性质实验的部分活动记录。
| 实验内容 | 实验现象 | 解释原因(文字或反应) |
| 观察氯水颜色 | ① | 氯水中含有氯气分子 |
向氯水中滴入 | 有无色气体生成 | ② |
| 用玻璃棒蘸取氯水,点在品红试纸上 | 红色褪去 | ③ |
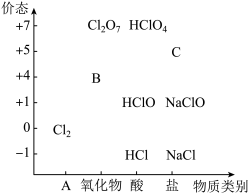
②某同学利用a.
 b.
b. c.酸性
c.酸性 三种溶液探究盐酸性质,试验前进行如下预测:从物质类别上看,盐酸有酸的通性,可能与
三种溶液探究盐酸性质,试验前进行如下预测:从物质类别上看,盐酸有酸的通性,可能与 具有
具有(4)下图是用强光照射密闭广口瓶中新制氯水时,用数字化传感器采集的图像,下列纵坐标代表的物理量与图像相符的是

c.溶液的导电能力 d.溶液的漂白能力
您最近一年使用:0次
【推荐2】请按要求回答下列问题:
(1)实验室二氧化锰和浓盐酸在加热条件下制取Cl2,其中 MnO2 是__________ 剂;反应中氯化氢体现了_____________ 性和 _______________ 性。
(2)室温下KClO3 与浓盐酸反应制取氯气的化学方程式:KClO3+6HCl(浓)=KCl+3Cl2+3H2O请在上式中用单线桥法表示出得失电子的情况。___
(3)用CuCl2作催化剂,在450℃时用空气中的O2 跟 HCl 反应也能制得氯气,其化学方程式:4HCl+O2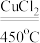 2H2O+2Cl2,从以上3种制备的方法中,可以认为氧化剂的氧化能力从强到弱的顺序为
2H2O+2Cl2,从以上3种制备的方法中,可以认为氧化剂的氧化能力从强到弱的顺序为________ 。
(4)把 Cl2 通入浓氨水中,发生如下反应:3Cl2+8NH3=6NH4Cl+N2请在上式用双线桥表示反应的电子转移方向和数目___ ;反应中氧化剂与还原剂分子数之比为 ___ 。若反应中有 6.8 g NH3 发生氧化反应,则反应中生成的 N2 质量为 __________ g。
(1)实验室二氧化锰和浓盐酸在加热条件下制取Cl2,其中 MnO2 是
(2)室温下KClO3 与浓盐酸反应制取氯气的化学方程式:KClO3+6HCl(浓)=KCl+3Cl2+3H2O请在上式中用单线桥法表示出得失电子的情况。
(3)用CuCl2作催化剂,在450℃时用空气中的O2 跟 HCl 反应也能制得氯气,其化学方程式:4HCl+O2
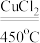 2H2O+2Cl2,从以上3种制备的方法中,可以认为氧化剂的氧化能力从强到弱的顺序为
2H2O+2Cl2,从以上3种制备的方法中,可以认为氧化剂的氧化能力从强到弱的顺序为(4)把 Cl2 通入浓氨水中,发生如下反应:3Cl2+8NH3=6NH4Cl+N2请在上式用双线桥表示反应的电子转移方向和数目
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】海水中含有大量的卤族元素,具有十分巨大的开发利用潜力。
I.氯气是非常重要的化工产品
(1)用浓盐酸和二氧化锰制氯气是实验室常用的方法,写出该反应的化学方程式:_____ 。
(2)也可用浓盐酸和高锰酸钾制氯气,反应方程式如下:2KMnO4+16HCl(浓)=KCl+2MnCl2+5Cl2↑+8H2O,实验室用该方法制氯气时,可选用的发生装置是___________ (写编号)。
(3)为证明氯气与水反应产物具有漂白性,将Cl2缓缓通过下列装置:
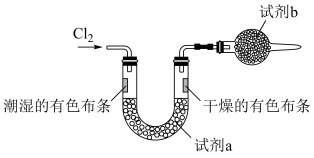
试剂a应选择___________ ;试剂b的作用是___________ ;___________ 。
(4)通常使用84消毒液时需要把消毒对象在其中浸泡一段时间,以提高消毒效果。请结合反应方程式分析原因___________
II.地球上99%的溴元素以Br-形式存在于海水中。海水中Br-含量约为65mg/L,而苦卤(海水晒盐后得到的母液)中Br-含量高很多,苦卤常作海水提溴的主要原料。目前最成熟的“空气吹出法”海水提溴工艺流程如图(已知:溴的沸点为59℃):
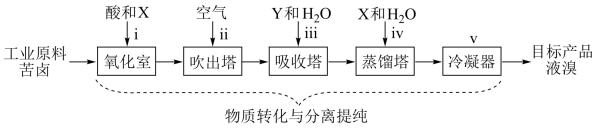
(5)为实现Br-转化为Br2的目的,所加试剂X应必有的化学性质是___________ 。
(6)利用“空气吹出法”将“氧化室”产生的低浓度Br2分离出来的方法利用了溴的___________ 这一物理性质。
(7)将低浓度Br2富集为高浓度Br2历经步骤iii反应的离子方程式为:___________ 。
I.氯气是非常重要的化工产品
(1)用浓盐酸和二氧化锰制氯气是实验室常用的方法,写出该反应的化学方程式:
(2)也可用浓盐酸和高锰酸钾制氯气,反应方程式如下:2KMnO4+16HCl(浓)=KCl+2MnCl2+5Cl2↑+8H2O,实验室用该方法制氯气时,可选用的发生装置是
| 编号 | A | B | C |
| 发生装置 | 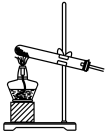 |  | 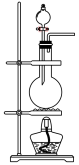 |

试剂a应选择
(4)通常使用84消毒液时需要把消毒对象在其中浸泡一段时间,以提高消毒效果。请结合反应方程式分析原因
II.地球上99%的溴元素以Br-形式存在于海水中。海水中Br-含量约为65mg/L,而苦卤(海水晒盐后得到的母液)中Br-含量高很多,苦卤常作海水提溴的主要原料。目前最成熟的“空气吹出法”海水提溴工艺流程如图(已知:溴的沸点为59℃):

(5)为实现Br-转化为Br2的目的,所加试剂X应必有的化学性质是
(6)利用“空气吹出法”将“氧化室”产生的低浓度Br2分离出来的方法利用了溴的
(7)将低浓度Br2富集为高浓度Br2历经步骤iii反应的离子方程式为:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】以铬铁矿(主要成分为FeO·Cr2O3,还含有Al2O3等杂质)为原料制备金属铬的工艺流程如图所示:
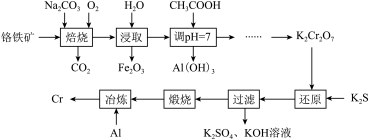
(1)“焙烧”后所得固体为Na2CrO4、Fe2O3和NaAlO2。
①“焙烧”时FeO·Cr2O3发生反应的化学方程式为____ 。
②“焙烧”时Al2O3发生反应的化学方程式为____ 。
(2)“调pH=7”时生成Al(OH)3的离子方程式为____ 。
(3)“过滤”所得滤渣为Cr(OH)3,“还原”反应的离子方程式为____ 。
(4)“冶炼”时的化学方程式为____ 。
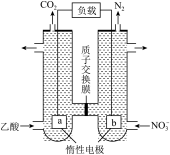
(5)含醋酸的酸性废水可用图2所示方法处理,写出负极的电极反应式:____ 。

(1)“焙烧”后所得固体为Na2CrO4、Fe2O3和NaAlO2。
①“焙烧”时FeO·Cr2O3发生反应的化学方程式为
②“焙烧”时Al2O3发生反应的化学方程式为
(2)“调pH=7”时生成Al(OH)3的离子方程式为
(3)“过滤”所得滤渣为Cr(OH)3,“还原”反应的离子方程式为
(4)“冶炼”时的化学方程式为
(5)含醋酸的酸性废水可用图2所示方法处理,写出负极的电极反应式:

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】Ⅰ.元素的“价—类”二维图体现了化学变化之美。部分含硫、氮物质的类别与硫元素和氮元素化合价的对应关系如图所示。回答下列问题:
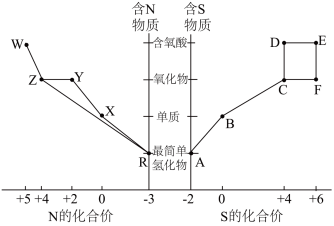
(1)写出实验室利用两种固体物质加热制备物质R的化学方程式_____ 。
(2)物质R→Y是工业制硝酸的重要反应,其化学方程式是_____ 。
(3)写出物质E的浓溶液与碳单质反应的化学方程式:_____ 。
(4)下列有关图中所示含N、S物质的叙述,正确的是_____ (填标号)。
Ⅱ.粗盐中含有泥沙及Ca2+、Mg2+、SO 等杂质,其提纯过程一般经过以下流程:
等杂质,其提纯过程一般经过以下流程:
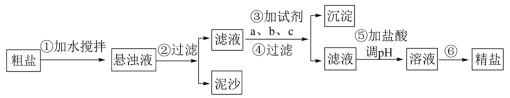
某兴趣小组按上述方案进行粗盐提纯实验,实验室提供了粗盐样品、稀盐酸、NaOH溶液、BaCl2溶液、Na2CO3溶液等药品以及必备的实验仪器若干。请回答下列问题:
(5)操作③按a、b、c顺序依次加入过量的试剂。若a为NaOH溶液,则c为_____ 溶液。
(6)加盐酸调溶液pH的目的是_____ 。
(7)步骤⑥操作名称是_____ 。

(1)写出实验室利用两种固体物质加热制备物质R的化学方程式
(2)物质R→Y是工业制硝酸的重要反应,其化学方程式是
(3)写出物质E的浓溶液与碳单质反应的化学方程式:
(4)下列有关图中所示含N、S物质的叙述,正确的是
| A.在催化剂的作用下,R可将Y、Z还原为X |
| B.图中所示的物质中,只有W、D、E属于电解质 |
| C.用玻璃棒分别蘸取浓的R溶液和浓的W溶液,玻璃棒靠近时有白烟产生 |
| D.Z、C、F均能与NaOH溶液反应,都是酸性氧化物 |
Ⅱ.粗盐中含有泥沙及Ca2+、Mg2+、SO
 等杂质,其提纯过程一般经过以下流程:
等杂质,其提纯过程一般经过以下流程:
某兴趣小组按上述方案进行粗盐提纯实验,实验室提供了粗盐样品、稀盐酸、NaOH溶液、BaCl2溶液、Na2CO3溶液等药品以及必备的实验仪器若干。请回答下列问题:
(5)操作③按a、b、c顺序依次加入过量的试剂。若a为NaOH溶液,则c为
(6)加盐酸调溶液pH的目的是
(7)步骤⑥操作名称是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】2-噻吩乙醇(Mr=128)是抗血栓药物氯吡格雷的重要中间体,其制备方法如下:
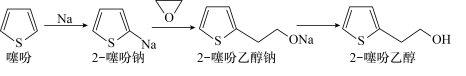
Ⅰ.制钠砂。向烧瓶中加入300mL液体A和4.60g金属钠,加热至钠熔化后,盖紧塞子,振荡至大量微小钠珠出现。
Ⅱ.制噻吩钠。降温至10℃,加入25mL噻吩,反应至钠砂消失。
Ⅲ.制噻吩乙醇钠。降温至-10℃,加入稍过量的环氧乙烷的四氢呋喃溶液,反应30min。
Ⅳ.水解。恢复室温,加入70mL水,搅拌30min;加盐酸调pH至4~6,继续反应2h,分液;用水洗涤有机相,二次分液。
Ⅴ.分离。向有机相中加入无水MgSO4,静置,过滤,对滤液进行蒸馏,蒸出四氢呋喃、噻吩和液体A后,得到产品17.92g。
产品的产率为_______ (用Na计算,精确至0.1%)。

Ⅰ.制钠砂。向烧瓶中加入300mL液体A和4.60g金属钠,加热至钠熔化后,盖紧塞子,振荡至大量微小钠珠出现。
Ⅱ.制噻吩钠。降温至10℃,加入25mL噻吩,反应至钠砂消失。
Ⅲ.制噻吩乙醇钠。降温至-10℃,加入稍过量的环氧乙烷的四氢呋喃溶液,反应30min。
Ⅳ.水解。恢复室温,加入70mL水,搅拌30min;加盐酸调pH至4~6,继续反应2h,分液;用水洗涤有机相,二次分液。
Ⅴ.分离。向有机相中加入无水MgSO4,静置,过滤,对滤液进行蒸馏,蒸出四氢呋喃、噻吩和液体A后,得到产品17.92g。
产品的产率为
您最近一年使用:0次



