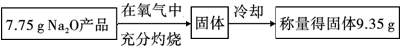
I.(1)氨和硝酸都是重要的工业原料,标准状况下,将640L氨气溶于水形成1L氨水,则此氨水的物质的量浓度为______ mol/L(保留三位有效数字).将体积为12mL的试管充满NO2气体后,倒立于水槽中(保持同温同压),液面稳定后,保持相同条件下再通入O2,若要液面仍在原来的位置,则通入O2的体积为______ mL。
(2)工业中的尾气(假设只有NO和NO2)用烧碱进行吸收,反应的离子方程式为2NO2+2OH- =NO2-+NO3-+H2O和NO+NO2+2OH- =_____ +H2O(配平该方程式)。
Ⅱ.在标准状况下,分别取30mL相同浓度的盐酸依次装入①②③试管中,然后分别慢慢加入组成相同的镁铝混合物,相同条件下,测得有关数据如表所示(反应前后溶液体积不发生变化)。
(1)①组实验中,盐酸__________ ,(填过量或不足);②组实验中,盐酸__________ ,(填过量或不足)。
(2)盐酸的物质的量浓度为__________ mol/L。
(3)混合物中Mg和Al的物质的量之比为__________ 。
(2)工业中的尾气(假设只有NO和NO2)用烧碱进行吸收,反应的离子方程式为2NO2+2OH- =NO2-+NO3-+H2O和NO+NO2+2OH- =
Ⅱ.在标准状况下,分别取30mL相同浓度的盐酸依次装入①②③试管中,然后分别慢慢加入组成相同的镁铝混合物,相同条件下,测得有关数据如表所示(反应前后溶液体积不发生变化)。
| 实验序号 | ① | ② | ③ |
| 混合物质量/mg | 255 | 510 | 1020 |
| 气体体积/mL | 280 | 336 | 336 |
(1)①组实验中,盐酸
(2)盐酸的物质的量浓度为
(3)混合物中Mg和Al的物质的量之比为
更新时间:2019-01-30 08:08:49
|
相似题推荐
计算题
|
适中
(0.65)
【推荐1】硝酸与合成氨工业密切相关,氨氧化法是工业生产中制取硝酸的主要途径。
完成下列计算:
(1)合成氨时,假设100L的氮气与氢气(体积比为1 : 3)的混合气体通过氨合成塔充分反应后,体积变为90L,则氮气的转化率为____________ 。(写出计算过程,计算结果请用百分数表示)
(2)标准状况下,将500L氨气溶于1L水中形成氨水,则此氨水质量分数为____________ 。(写出计算过程,计算结果请用百分数表示,并保留1位小数)
(3)氨氧化法是将氨和空气的混合气通过灼热的铂铑合金网,在合金网的催化下,氨被氧化成一氧化氮(NO)。此时温度很高,水以水蒸气的形式存在,NO也不与O2反应。若氨气与氧气物质的量之比为1:1.7 时,氨的转化率可达95%,计算反应后NO的体积分数____________ 。(设氧气在空气中的体积分数为20%,写出计算过程,计算结果请用百分数表示并保留1位小数)
(4)一氧化氮继续氧化为二氧化氮,二氧化氮溶于水可得硝酸。为测定某18K金样品的组成,将2.832 g样品粉碎后投入足量的浓硝酸中,充分溶解后,收集到NO2和N2O4的混合气体224 mL(折算至标准状况,下同),将该混合气体与84 mL O2混合后缓缓通入水中,恰好被完全吸收。( 已知金不溶于浓硝酸)
填写该18K金的成分表(写出计算过程,计算结果请用百分数表示并保留1位小数,若不含该金属则填0)。
完成下列计算:
(1)合成氨时,假设100L的氮气与氢气(体积比为1 : 3)的混合气体通过氨合成塔充分反应后,体积变为90L,则氮气的转化率为
(2)标准状况下,将500L氨气溶于1L水中形成氨水,则此氨水质量分数为
(3)氨氧化法是将氨和空气的混合气通过灼热的铂铑合金网,在合金网的催化下,氨被氧化成一氧化氮(NO)。此时温度很高,水以水蒸气的形式存在,NO也不与O2反应。若氨气与氧气物质的量之比为1:1.7 时,氨的转化率可达95%,计算反应后NO的体积分数
(4)一氧化氮继续氧化为二氧化氮,二氧化氮溶于水可得硝酸。为测定某18K金样品的组成,将2.832 g样品粉碎后投入足量的浓硝酸中,充分溶解后,收集到NO2和N2O4的混合气体224 mL(折算至标准状况,下同),将该混合气体与84 mL O2混合后缓缓通入水中,恰好被完全吸收。( 已知金不溶于浓硝酸)
填写该18K金的成分表(写出计算过程,计算结果请用百分数表示并保留1位小数,若不含该金属则填0)。
| 18K金成分 | Au | Ag | Cu |
| 含量(质量分数) | 75 % |
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐2】完成下列问题
(1)把盛满 和
和 的混合气体的试管倒立于水中。
的混合气体的试管倒立于水中。
①若一段时间内水上升且充满试管,则原混合气体中 和
和 的体积比是
的体积比是___________ ,若假设生成的溶质不向外扩散,且为标准状况。则所得溶液的物质的量浓度应为___________ 。(保留二位有效数字)
②若一段时间后上升的水只升到试管容积的一半,则剩余的气体为___________ (用化学式表示)。原混合气体中, 和
和 的体积比是
的体积比是___________ 。
(2)二氧化氮和氨气在一定条件下,充分反应,得到非常稳定的产物,其化学方程式为: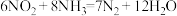 ,若
,若 和
和 的混合气体在一定条件下发生上述反应,已知实际参加反应的
的混合气体在一定条件下发生上述反应,已知实际参加反应的 比
比 少2mL,则原混合气体中
少2mL,则原混合气体中 和
和 的物质的量之比可能为___________。
的物质的量之比可能为___________。
(1)把盛满
 和
和 的混合气体的试管倒立于水中。
的混合气体的试管倒立于水中。①若一段时间内水上升且充满试管,则原混合气体中
 和
和 的体积比是
的体积比是②若一段时间后上升的水只升到试管容积的一半,则剩余的气体为
 和
和 的体积比是
的体积比是(2)二氧化氮和氨气在一定条件下,充分反应,得到非常稳定的产物,其化学方程式为:
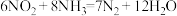 ,若
,若 和
和 的混合气体在一定条件下发生上述反应,已知实际参加反应的
的混合气体在一定条件下发生上述反应,已知实际参加反应的 比
比 少2mL,则原混合气体中
少2mL,则原混合气体中 和
和 的物质的量之比可能为___________。
的物质的量之比可能为___________。| A.3:4 | B.3:2 | C.1:2 | D.3:7。 |
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐3】在浓硝酸中放入铜片,请完成下列各题:
(1)开始时反应的化学方程式为_______ 。
(2)若将6.4g铜与一定量的浓硝酸反应,铜消耗完时,共产生气体5.6L(标准状况下),则所消耗硝酸的物质的量是_______ mol
(3)若另用试管收集满100mLNO和NO2的混合气体,倒立于盛有水的水槽中,并缓慢通入O2,当分别通入V mL或80 mL(V<80)O2时,均剩余20mL气体(均为标准状况)。
①当通入80mLO2时剩余的气体是_______ 。
②混合气体中NO2的体积是_______ mL。
③V的值是_______ 。
④当通入O2使试管中恰好没有气体剩余时,所得溶液的物质的量浓度为(假设溶液不扩散)_______ mol/L(保留到小数点后第三位)
(1)开始时反应的化学方程式为
(2)若将6.4g铜与一定量的浓硝酸反应,铜消耗完时,共产生气体5.6L(标准状况下),则所消耗硝酸的物质的量是
(3)若另用试管收集满100mLNO和NO2的混合气体,倒立于盛有水的水槽中,并缓慢通入O2,当分别通入V mL或80 mL(V<80)O2时,均剩余20mL气体(均为标准状况)。
①当通入80mLO2时剩余的气体是
②混合气体中NO2的体积是
③V的值是
④当通入O2使试管中恰好没有气体剩余时,所得溶液的物质的量浓度为(假设溶液不扩散)
您最近一年使用:0次
【推荐1】标准状况下,进行甲、乙、丙三组实验,各取30.0 mL相同浓度的盐酸溶液,然后分别慢慢地加入不同质量的的同一种镁铝合金粉末,得下列有关数据:(假设反应前后溶液的体积不发生变化)请回答:
(1)根据所给数据,计算盐酸的物质的量浓度为__________ mol/L。
(2)根据所给数据,计算镁铝的物质的量之比为___________ 。
(3)甲组实验后,向容器中加入一定量1 mol/L的NaOH溶液,恰好使铝元素全部以AlO2—形式存在,并使Mg2+刚好沉淀完全,所需NaOH体积为______ 升。
(4)取一定量的Al2O3投入到NaOH溶液中,全部溶解,再通入CO2气体,当通入CO2气体2.24L时,生成11.7克的沉淀,如果通入CO2气体1.12L时,生成的沉淀是多少克?_________
| 甲 | 乙 | 丙 | |
| 合金质量/mg | 255 | 385 | 459 |
| 气体体积/mL | 280 | 336 | 336 |
(1)根据所给数据,计算盐酸的物质的量浓度为
(2)根据所给数据,计算镁铝的物质的量之比为
(3)甲组实验后,向容器中加入一定量1 mol/L的NaOH溶液,恰好使铝元素全部以AlO2—形式存在,并使Mg2+刚好沉淀完全,所需NaOH体积为
(4)取一定量的Al2O3投入到NaOH溶液中,全部溶解,再通入CO2气体,当通入CO2气体2.24L时,生成11.7克的沉淀,如果通入CO2气体1.12L时,生成的沉淀是多少克?
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】把5.1 g镁铝合金的粉末放入500 mL1 mol/L盐酸中,恰好完全反应。试计算:
(1)该合金中镁和铝的物质的量:n(Mg)______________ ;n(Al)______________
(2)将等质量的该合金投入到足量的氢氧化钠溶液中,求标况下放出气体的体积。__________ 。
(1)该合金中镁和铝的物质的量:n(Mg)
(2)将等质量的该合金投入到足量的氢氧化钠溶液中,求标况下放出气体的体积。
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐1】完成下列计算:
(1)某无土栽培用的营养液,要求KCl、K2SO4和NH4Cl三种固体原料的物质的量之比为1:4:8。若配制该营养液,取428gNH4Cl,则需KCl的质量为________ g。
(2)在K2SO4和Al2(SO4)3的混合溶液中,测得Al3+的浓度为0.2mol•L﹣1,加入等体积0.6mol•L﹣1的BaCl2溶液恰好使SO42-完全沉淀,则混合溶液中K+的浓度为_____ mol•L﹣1。
(3)某固态化合物X受热分解的反应为:X=A↑+B↑+C↑,在一定的温度和压强下测得反应生成的混合气体对氢气的相对密度为15,则X的摩尔质量是___________ 。
(4)标准状况下,将V L A气体(摩尔质量为M mol•L﹣1)溶于0.1L水(密度1g/cm3)中,所得溶液的密度为dg/mL,则此溶液的物质的量浓度为____________ mol•L﹣1。
(1)某无土栽培用的营养液,要求KCl、K2SO4和NH4Cl三种固体原料的物质的量之比为1:4:8。若配制该营养液,取428gNH4Cl,则需KCl的质量为
(2)在K2SO4和Al2(SO4)3的混合溶液中,测得Al3+的浓度为0.2mol•L﹣1,加入等体积0.6mol•L﹣1的BaCl2溶液恰好使SO42-完全沉淀,则混合溶液中K+的浓度为
(3)某固态化合物X受热分解的反应为:X=A↑+B↑+C↑,在一定的温度和压强下测得反应生成的混合气体对氢气的相对密度为15,则X的摩尔质量是
(4)标准状况下,将V L A气体(摩尔质量为M mol•L﹣1)溶于0.1L水(密度1g/cm3)中,所得溶液的密度为dg/mL,则此溶液的物质的量浓度为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐2】铁、铜混合粉末20.0 g加入到100 mL5.0 mol·L-1FeCl3溶液中,剩余固体质量为5.2 g(忽略反应前后溶液体积变化)。计算:还原剂失去电子的物质的量_____ ;反应后溶液中FeCl2的物质的量浓度_____ mol·L-1。
您最近一年使用:0次