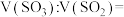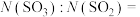现有五种物质A、B、C、D、E,其中有一种是碱,四种是盐,它们分别由下表中的离子组成:
为鉴别它们,分别完成以下实验,其结果如下:①A溶液与B溶液反应生成无色气体X,气体X可以与C溶液反应生成沉淀E,沉淀E可与B溶液反应;②B溶液与C溶液反应生成白色沉淀D,沉淀D不溶于稀硝酸。请根据上述实验结果,填空:
(1)写出下列物质的化学式:A________ ,X________ 。
(2)B溶于水后的电离方程式为________ 。鉴别B中阴离子的实验操作方法是________ 。
(3)写出A溶液与B溶液反应的离子方程式:________ 。
(4)D与E的混合物a g,加入足量盐酸,反应完毕生成标准状况下的气体b L,则D在混合物中的质量分数为________ (列出算式即可)。
| 阳离子 | Na+ H+ Ba2+ |
| 阴离子 | OH- CO32- SO42- |
(1)写出下列物质的化学式:A
(2)B溶于水后的电离方程式为
(3)写出A溶液与B溶液反应的离子方程式:
(4)D与E的混合物a g,加入足量盐酸,反应完毕生成标准状况下的气体b L,则D在混合物中的质量分数为
更新时间:2019-02-01 18:01:03
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】我国化工专家侯德榜改革国外的纯碱生产工艺,他设计的生产流程可用下图表示。

(1)上述生产纯碱的方法被称为___________ 。
(2)食盐水中若含有MgCl2杂质,可滴加适量___________ 进行除杂。
(3)流程中的副产品为NH4Cl,是一种重要的氮肥,该物质在水溶液中的电离方程式为_____ 。
(4)上述流程中物质X的分子式为___________ 。
(5)沉淀池中发生反应的化学方程式是___________ 。从沉淀池中分离出沉淀的操作名称是___________ 。
(6)为检验产品碳酸钠中是否含有氯化钠,可取少量试样溶于水后,然后___________ 。

(1)上述生产纯碱的方法被称为
(2)食盐水中若含有MgCl2杂质,可滴加适量
(3)流程中的副产品为NH4Cl,是一种重要的氮肥,该物质在水溶液中的电离方程式为
(4)上述流程中物质X的分子式为
(5)沉淀池中发生反应的化学方程式是
(6)为检验产品碳酸钠中是否含有氯化钠,可取少量试样溶于水后,然后
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】铅酸蓄电池在生产、生活中使用广泛,其放电过程中,发生反应的化学方程式为 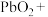
 废铅酸蓄电池中回收铅的一种工艺流程如图。
废铅酸蓄电池中回收铅的一种工艺流程如图。

回答下列问题:
(1)对于反应 该反应中Pb体现了
该反应中Pb体现了_______ (填“还原性”或“氧化性”)。
(2)Na2CO3在水中的电离方程式为_______ 。
(3)废硫酸直接排放会污染环境:
①可用氟磷灰石[Ca5(PO4)3F]进行处理,反应的化学方程式为
 相对分子质量:H2SO4
相对分子质量:H2SO4_______ (填“>”或“<”)HF。
②也可用烧碱溶液来处理废硫酸,发生反应的离子方程式为_______ ,该反应的基本反应类型为_______ 。
(4)若滤渣的主要成分为PbCO3,则PbCO3与焦炭反应的化学方程式为_______ (假设杂质不参与反应)。
(5)写出铅在生活中的一种用途:_______ 。
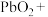
 废铅酸蓄电池中回收铅的一种工艺流程如图。
废铅酸蓄电池中回收铅的一种工艺流程如图。
回答下列问题:
(1)对于反应
 该反应中Pb体现了
该反应中Pb体现了(2)Na2CO3在水中的电离方程式为
(3)废硫酸直接排放会污染环境:
①可用氟磷灰石[Ca5(PO4)3F]进行处理,反应的化学方程式为

 相对分子质量:H2SO4
相对分子质量:H2SO4②也可用烧碱溶液来处理废硫酸,发生反应的离子方程式为
(4)若滤渣的主要成分为PbCO3,则PbCO3与焦炭反应的化学方程式为
(5)写出铅在生活中的一种用途:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】某无色透明溶液中可能大量存在Ag+、Mg2+、Cu2+、Fe3+、Na+中的几种。请填写下列空白:
(1)不做任何实验就可以肯定原溶液中不存在 的离子是______ 。
(2)取少量原溶液,加入过量稀盐酸,有白色沉淀生成。说明原溶液中,肯定存在的离子是______ ,有关离子方程式为______ 。
(3)取(2)中的滤液,加入过量的NaOH,出现白色沉淀,说明原溶液中肯定有______ ,有关的离子方程式为______ 。
(4)原溶液可能大量存在的阴离子是下列的______(填选项)。
(1)不做任何实验就可以肯定原溶液中
(2)取少量原溶液,加入过量稀盐酸,有白色沉淀生成。说明原溶液中,肯定存在的离子是
(3)取(2)中的滤液,加入过量的NaOH,出现白色沉淀,说明原溶液中肯定有
(4)原溶液可能大量存在的阴离子是下列的______(填选项)。
A. | B. | C. | D. |
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】已知A和B两支试管所盛的溶液中共含有K+、Ag+、Mg2+、Cl-、OH-、NO3-六种离子,向试管A的溶液中滴入酚酞试液呈粉红色。请回答下列问题:
(1)试管A的溶液中所含上述离子共有___________ 种。
(2)若向某试管中滴入稀盐酸产生沉淀,则该试管为_______ (填“A”或“B”)。
(3)若向试管B的溶液中加入合适的药品,过滤后可以得到相应的金属和仅含一种溶质的溶液,则加入的药品是________________ (填化学式)。
(4)若将试管A和试管B中的溶液按一定体积比混合过滤后,蒸干滤液可得到一种纯净物,则混合过程中发生反应的离子方程式为_________________________ , _________________________ 。
(5)若试管A和试管B中的溶液是由等物质的量的四种物质配成的溶液,将两试管中溶液混合后过滤,所得滤液中各种离子的物质的量之比为__________________ 。
(6)若向由试管A溶液中的阳离子组成的碳酸氢盐溶液中,滴入少量Ba(OH)2溶液,则发生反应的离子方程式为_____________________________________
(1)试管A的溶液中所含上述离子共有
(2)若向某试管中滴入稀盐酸产生沉淀,则该试管为
(3)若向试管B的溶液中加入合适的药品,过滤后可以得到相应的金属和仅含一种溶质的溶液,则加入的药品是
(4)若将试管A和试管B中的溶液按一定体积比混合过滤后,蒸干滤液可得到一种纯净物,则混合过程中发生反应的离子方程式为
(5)若试管A和试管B中的溶液是由等物质的量的四种物质配成的溶液,将两试管中溶液混合后过滤,所得滤液中各种离子的物质的量之比为
(6)若向由试管A溶液中的阳离子组成的碳酸氢盐溶液中,滴入少量Ba(OH)2溶液,则发生反应的离子方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】有一透明溶液,可能含有较大量的Mg2+、Fe3+、Al3+、Cu2+、Na+、H+、SO42-、CO32-中的一种或几种,取此溶液做下列实验:
①取少量溶液加入用盐酸酸化的BaCl2溶液,有白色沉淀生成;
②取少量溶液加入过氧化钠粉末,溶液中有白色沉淀产生并逸出无色无味的气体,加入Na2O2的物质的量与析出沉淀的物质的量如图所示。

试推断并完成作答:
(1)溶液中一定含有的离子是___________ ;
(2)溶液中肯定不含有的离子是_________ ;
(3)检验可能含有的离子的方法是____________ 。
(4)图示中a点沉淀的成分是______________ 。
①取少量溶液加入用盐酸酸化的BaCl2溶液,有白色沉淀生成;
②取少量溶液加入过氧化钠粉末,溶液中有白色沉淀产生并逸出无色无味的气体,加入Na2O2的物质的量与析出沉淀的物质的量如图所示。

试推断并完成作答:
(1)溶液中一定含有的离子是
(2)溶液中肯定不含有的离子是
(3)检验可能含有的离子的方法是
(4)图示中a点沉淀的成分是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】某白色粉末,可能含有硫酸钠、硫酸铜、氯化钠、硝酸钡、碳酸钙中的一种或几种。某科学兴趣小组为探究其成分,设计了如下实验流程(所加试剂均足量)。
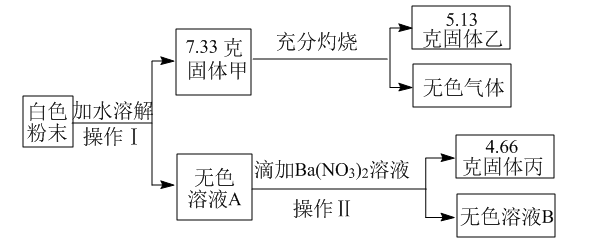
(1)操作I的名称是_____ 。
(2)生成无色气体的质量是___________ 克,所涉及的化学反应方程式_____
(3)固体甲的成分是___________ ,所涉及的离子反应方程式_____
(4)这种白色粉末中一定不含有___________ 。
(5)求白色粉末中肯定含有的物质总质量___________ 。

(1)操作I的名称是
(2)生成无色气体的质量是
(3)固体甲的成分是
(4)这种白色粉末中一定不含有
(5)求白色粉末中肯定含有的物质总质量
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】化合物X由三种前四周期常见元素组成,某学习小组按如下流程进行实验:

请回答:
(1)E的电子式是_______ ,X的化学式是_______ 。
(2)写出X与足量浓 反应的化学方程式
反应的化学方程式_______ 。
(3)写出气体D与酸性 溶液反应的离子反应方程式
溶液反应的离子反应方程式_______ 。
(4)设计实验检验溶液G中的阳离子_______ 。

请回答:
(1)E的电子式是
(2)写出X与足量浓
 反应的化学方程式
反应的化学方程式(3)写出气体D与酸性
 溶液反应的离子反应方程式
溶液反应的离子反应方程式(4)设计实验检验溶液G中的阳离子
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】溶液X中可能含有 、
、 、
、 、
、 ,
, ,
, 、
、 中的几种离子(不考虑水的电离)。回答下列问题:
中的几种离子(不考虑水的电离)。回答下列问题:
(1)取少量溶液X于试管中,滴加稀盐酸,先无明显现象,随后有气泡生成,说明溶液X中一定不含______ (填离子符号,下同),一定含有______ ;向反应后的溶液中加入硝酸酸化的 溶液有白色沉淀生成,能否说明溶液X中含有Cl,并阐明原因:
溶液有白色沉淀生成,能否说明溶液X中含有Cl,并阐明原因:____________ 。
(2)为确定溶液组成,设计如图1所示的实验装置进行探究。
Ⅰ.取50 mL溶液X于锥形瓶中,逐滴加入稀硝酸,并用压强传感器测定锥形瓶内的压强变化,压强传感器所示数据如图2所示。
Ⅱ.另取100 mL溶液X于试管中,加入足量稀硝酸和 溶液,有白色沉淀生成,经过滤、洗涤、干燥后,称得沉淀质量为2.87 g。
溶液,有白色沉淀生成,经过滤、洗涤、干燥后,称得沉淀质量为2.87 g。

①对图1装置检查气密性的操作为____________ 。
②图2中G→M点压强增大的主要原因是____________ 。
③已知N点消耗50 mL 1 mol⋅L 的稀硝酸,则步骤Ⅰ中产生
的稀硝酸,则步骤Ⅰ中产生 的总质量为
的总质量为______ g;结合步骤Ⅱ可以得出溶液X中各离子的物质的量之比为______ [用 的格式表示]。
的格式表示]。
 、
、 、
、 、
、 ,
, ,
, 、
、 中的几种离子(不考虑水的电离)。回答下列问题:
中的几种离子(不考虑水的电离)。回答下列问题:(1)取少量溶液X于试管中,滴加稀盐酸,先无明显现象,随后有气泡生成,说明溶液X中一定不含
 溶液有白色沉淀生成,能否说明溶液X中含有Cl,并阐明原因:
溶液有白色沉淀生成,能否说明溶液X中含有Cl,并阐明原因:(2)为确定溶液组成,设计如图1所示的实验装置进行探究。
Ⅰ.取50 mL溶液X于锥形瓶中,逐滴加入稀硝酸,并用压强传感器测定锥形瓶内的压强变化,压强传感器所示数据如图2所示。
Ⅱ.另取100 mL溶液X于试管中,加入足量稀硝酸和
 溶液,有白色沉淀生成,经过滤、洗涤、干燥后,称得沉淀质量为2.87 g。
溶液,有白色沉淀生成,经过滤、洗涤、干燥后,称得沉淀质量为2.87 g。
①对图1装置检查气密性的操作为
②图2中G→M点压强增大的主要原因是
③已知N点消耗50 mL 1 mol⋅L
 的稀硝酸,则步骤Ⅰ中产生
的稀硝酸,则步骤Ⅰ中产生 的总质量为
的总质量为 的格式表示]。
的格式表示]。
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】碳酸亚铁在空气中灼烧得到铁的氧化物A和一种气体。某学习小组为了探究该氧化物A的组成设计了两种实验方案:
方案Ⅰ

(1)若该方案中①通入Cl2不足量,小组成员认为可以通过在空气中充分搅拌D而最终实现准确测定,他的依据是_____ (用化学方程式表示)
(2)若氧化物A的质量是7.8400g,E的质量为8.0000g根据数据计算化合物A的化学式为_____ 。
方案Ⅱ
①称取ag氧化物A样品溶于足量稀硫酸,并配成100mL溶液。
②取20.00 mL该溶液于锥形瓶中,滴加几滴KSCN溶液,溶液变红色;再滴加双氧水至红色刚好褪去,同时产生少量气泡(资料显示SCN-可被H2O2氧化,产物为N2、CO2、SO42﹣)
③待气泡消失后,用 b mol/LKI标准溶液滴定锥形瓶中的Fe3+,滴定终点时消耗cmL KI标准溶液。
(3)该方案用到的定量仪器有量筒、分析天平、酸式滴定管、_____ 。
(4)步骤②中滴加KSCN溶液的目的是_____ 。
(5)补充完整该实验步骤③用到的酸式滴定管的润洗操作:关闭滴定管旋塞,从上口注入3﹣5mL待装液,_____ ,重复2﹣3次。
(6)步骤③能否选用淀粉作指示剂_____ 。(填“能”或“否”)
(7)有的同学通过查阅相关资料对该小组的实验设计进行了评价,以下说法合理的是_____
A.资料显示:HSCN有剧毒,易挥发。因此该方案步骤②可能因产生HSCN而不符合实验安全性的要求。
B.步骤②若加入H2O2过量,后续步骤不加以处理也不会对实验结果造成任何影响。
C.资料显示:Fe3+和I﹣之间的反应是明显的可逆反应,这样步骤③就会造成滴定测定不准确
(8)有的同学对碳酸亚铁的获得产生了兴趣。通过查阅资料发现碳酸亚铁可通过碳酸氢钠和硫酸亚铁发生Fe2++2HCO3﹣⇌FeCO3↓+H2CO3制得,请计算该反应的平衡常数K=_____ (mol/L)﹣2可能用到的数据如下:Ksp(FeCO3)=3.20×10﹣11,H2CO3的Ka1=4.30×10﹣7,Ka2=5.61×10﹣11。
方案Ⅰ

(1)若该方案中①通入Cl2不足量,小组成员认为可以通过在空气中充分搅拌D而最终实现准确测定,他的依据是
(2)若氧化物A的质量是7.8400g,E的质量为8.0000g根据数据计算化合物A的化学式为
方案Ⅱ
①称取ag氧化物A样品溶于足量稀硫酸,并配成100mL溶液。
②取20.00 mL该溶液于锥形瓶中,滴加几滴KSCN溶液,溶液变红色;再滴加双氧水至红色刚好褪去,同时产生少量气泡(资料显示SCN-可被H2O2氧化,产物为N2、CO2、SO42﹣)
③待气泡消失后,用 b mol/LKI标准溶液滴定锥形瓶中的Fe3+,滴定终点时消耗cmL KI标准溶液。
(3)该方案用到的定量仪器有量筒、分析天平、酸式滴定管、
(4)步骤②中滴加KSCN溶液的目的是
(5)补充完整该实验步骤③用到的酸式滴定管的润洗操作:关闭滴定管旋塞,从上口注入3﹣5mL待装液,
(6)步骤③能否选用淀粉作指示剂
(7)有的同学通过查阅相关资料对该小组的实验设计进行了评价,以下说法合理的是
A.资料显示:HSCN有剧毒,易挥发。因此该方案步骤②可能因产生HSCN而不符合实验安全性的要求。
B.步骤②若加入H2O2过量,后续步骤不加以处理也不会对实验结果造成任何影响。
C.资料显示:Fe3+和I﹣之间的反应是明显的可逆反应,这样步骤③就会造成滴定测定不准确
(8)有的同学对碳酸亚铁的获得产生了兴趣。通过查阅资料发现碳酸亚铁可通过碳酸氢钠和硫酸亚铁发生Fe2++2HCO3﹣⇌FeCO3↓+H2CO3制得,请计算该反应的平衡常数K=
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】草酸亚铁,在形成晶体时会结晶一定量的水;在工农业生产中具有重要用途,如照相的显影剂,生产磷酸铁锂电池的原料等。
已知:①草酸亚铁不溶于水,可溶于酸;②Fe(SCN)63-+3C2O42-=Fe(C2O4)33-+6SCN-。
回答下列问题:
Ⅰ.甲同学检查药品发现该晶体显浅黄色,认为晶体不纯,可能是因为部分的铁被氧化。为验证自己的猜想,进行实验验证。取少量的晶体样品溶于稀硫酸,滴加KSCN溶液,溶液无明显变化。由此认为晶体中不存在+3价的铁。你认为_______ (填“正确”或“不正确”),理由是___________________________________ 。
Ⅱ.乙同学为测定草酸亚铁晶体FeC2O4﹒xH2O中的结晶水含量,利用如下装置:

①做实验前首先要_____________________________ ;
②称取一定质量的晶体,装好药品,开始实验接下来的实验步骤依次为____________________ ,重复实验直至B中恒重。
a.点燃酒精灯,加热 b.熄灭酒精灯 c.关闭K d.打开K,缓缓通入空气 e.冷却至室温 f.称量
Ⅲ.丙同学用滴定的方法也可以测定草酸亚铁晶体中结晶水的含量。取a克草酸亚铁晶体溶入稀硫酸,再把所得溶液稀释成500mL,取出50mL放入锥形瓶,向其中逐滴滴入未知浓度的酸性KMnO4溶液,振荡,发现溶液颜色逐渐变为棕黄色,且有气泡冒出,当溶液颜色突变成浅紫色,停止滴加。接着向溶液中加入稍过量的KI溶液和几滴淀粉溶液,然后再用c mol/L的Na2S2O3溶液滴至终点。几次实验平均耗用Na2S2O3溶液VmL。(2Na2S2O3+I2=Na2S4O6+2NaI)
(1)写出向溶液中滴加酸性KMnO4溶液发生反应的离子方程式_____________________
(2)上述试验中稀释草酸亚铁溶液时除烧杯和玻璃棒外,还必需的玻璃仪器有__________
(3)x=_______________
(4)若实验中滴入KMnO4溶液过多,则所得x值___________ (填偏大、偏小或无影响)
已知:①草酸亚铁不溶于水,可溶于酸;②Fe(SCN)63-+3C2O42-=Fe(C2O4)33-+6SCN-。
回答下列问题:
Ⅰ.甲同学检查药品发现该晶体显浅黄色,认为晶体不纯,可能是因为部分的铁被氧化。为验证自己的猜想,进行实验验证。取少量的晶体样品溶于稀硫酸,滴加KSCN溶液,溶液无明显变化。由此认为晶体中不存在+3价的铁。你认为
Ⅱ.乙同学为测定草酸亚铁晶体FeC2O4﹒xH2O中的结晶水含量,利用如下装置:

①做实验前首先要
②称取一定质量的晶体,装好药品,开始实验接下来的实验步骤依次为
a.点燃酒精灯,加热 b.熄灭酒精灯 c.关闭K d.打开K,缓缓通入空气 e.冷却至室温 f.称量
Ⅲ.丙同学用滴定的方法也可以测定草酸亚铁晶体中结晶水的含量。取a克草酸亚铁晶体溶入稀硫酸,再把所得溶液稀释成500mL,取出50mL放入锥形瓶,向其中逐滴滴入未知浓度的酸性KMnO4溶液,振荡,发现溶液颜色逐渐变为棕黄色,且有气泡冒出,当溶液颜色突变成浅紫色,停止滴加。接着向溶液中加入稍过量的KI溶液和几滴淀粉溶液,然后再用c mol/L的Na2S2O3溶液滴至终点。几次实验平均耗用Na2S2O3溶液VmL。(2Na2S2O3+I2=Na2S4O6+2NaI)
(1)写出向溶液中滴加酸性KMnO4溶液发生反应的离子方程式
(2)上述试验中稀释草酸亚铁溶液时除烧杯和玻璃棒外,还必需的玻璃仪器有
(3)x=
(4)若实验中滴入KMnO4溶液过多,则所得x值
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐3】为更有效处理工业废气中排放的氮氧化物(NOx)、SO2等,减少大气污染。科学家不断对相关反应进行研究尝试。
(1)按每年全国发电燃煤8亿吨,煤中含硫质量分数以2%计,若不经过脱硫处理,则会有_______ 亿吨SO2排放到大气中(假设S全部转化为SO2)。
(2)下列物质中,能吸收SO2的有_______ (填序号)。
a.氨水 b.酸性KMnO4溶液 c.生石灰 d.Na2CO3溶液
(3)某工厂采用(NH4)2SO3和NH4HSO3的混合溶液A吸收废气中的SO2并制备(NH4)2SO3·H2O,过程如下:

①“吸收”过程中,溶液中(NH4)2SO3和NH4HSO3物质的量之比变_____ (填“大”或“小”)。
②“制备”过程中,溶液B中发生反应的化学方程式是_____________________ 。
③检验产品(NH4)2SO3·H2O中含有少量SO42-的方法如下:取少量产品加水溶解,(将实验操作和现象补充完整)___________________________________ 。
(4)选择性催化还原技术(SCR)是目前较为成熟的烟气脱硝技术,其反应原理主要为:4NH3(g)+4NO(g)+O2(g) 4N2(g)+6H2O(g) ΔH= -1627 kJ•mol-1
4N2(g)+6H2O(g) ΔH= -1627 kJ•mol-1
①被NO氧化的NH3和被O2氧化的NH3的物质的量之比为________________ 。

②氨氮比 会直接影响该方法的脱硝率如图为350 ℃时只改变氨气的投放量,NO的百分含量与氨氮比的关系图。当
会直接影响该方法的脱硝率如图为350 ℃时只改变氨气的投放量,NO的百分含量与氨氮比的关系图。当 >1.0时,烟气中NO含量反而增大,主要原因是
>1.0时,烟气中NO含量反而增大,主要原因是__________________ 。
(1)按每年全国发电燃煤8亿吨,煤中含硫质量分数以2%计,若不经过脱硫处理,则会有
(2)下列物质中,能吸收SO2的有
a.氨水 b.酸性KMnO4溶液 c.生石灰 d.Na2CO3溶液
(3)某工厂采用(NH4)2SO3和NH4HSO3的混合溶液A吸收废气中的SO2并制备(NH4)2SO3·H2O,过程如下:

①“吸收”过程中,溶液中(NH4)2SO3和NH4HSO3物质的量之比变
②“制备”过程中,溶液B中发生反应的化学方程式是
③检验产品(NH4)2SO3·H2O中含有少量SO42-的方法如下:取少量产品加水溶解,(将实验操作和现象补充完整)
(4)选择性催化还原技术(SCR)是目前较为成熟的烟气脱硝技术,其反应原理主要为:4NH3(g)+4NO(g)+O2(g)
 4N2(g)+6H2O(g) ΔH= -1627 kJ•mol-1
4N2(g)+6H2O(g) ΔH= -1627 kJ•mol-1①被NO氧化的NH3和被O2氧化的NH3的物质的量之比为

②氨氮比
 会直接影响该方法的脱硝率如图为350 ℃时只改变氨气的投放量,NO的百分含量与氨氮比的关系图。当
会直接影响该方法的脱硝率如图为350 ℃时只改变氨气的投放量,NO的百分含量与氨氮比的关系图。当 >1.0时,烟气中NO含量反而增大,主要原因是
>1.0时,烟气中NO含量反而增大,主要原因是
您最近一年使用:0次

 气体和
气体和 气体的体积之比
气体的体积之比