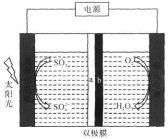
高温时通过以下反应制备金属铝。用铝制作的“快速放电铝离子二次电池”的原理如下图所示(EMI+为有机阳离子)。
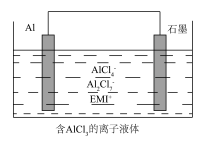
①Al2O3(s)+AlCl3(g)+3C(s)===3AlCl(g)+3CO(g) △H1=a kJ·mol-1
②3AlCl(g)===2A1(1)+AlCl3(g) △H2=b kJ·mol-1
③Al2O3(s)+3C(s)===2A1(1)+3CO(g) △H3
下列说法正确的是

①Al2O3(s)+AlCl3(g)+3C(s)===3AlCl(g)+3CO(g) △H1=a kJ·mol-1
②3AlCl(g)===2A1(1)+AlCl3(g) △H2=b kJ·mol-1
③Al2O3(s)+3C(s)===2A1(1)+3CO(g) △H3
下列说法正确的是
| A.该电池放电时的负极反应方程式为A1-3e-+7AlCl4-===4A12C17- |
| B.ΔH2<0 |
| C.该电池充电时石墨电极与电源负极相连 |
| D.A12O3(s)+3C(s)===2A1(1)+3CO(g) ΔH3=(a-b) kJ·mol-1 |
更新时间:2019-02-20 13:37:04
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】Mg−AgCl电池是一种以海水为电解质溶液的水激活电池,以下说法错误的是
| A.放电时Cl−由负极向正极迁移 |
| B.正极反应式为:AgCl+e−=Ag+Cl− |
| C.Mg作电池负极,发生氧化反应 |
| D.当负极质量减轻4.8 g,电路中通过0.4 mol电子 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】如图所示,装置Ⅰ是可充电电池,装置Ⅱ为电解池。离子交换膜只允许Na+通过,充放电的化学方程式为2Na2S2+NaBr3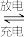 Na2S4+3NaBr。闭合开关K时,b极附近先变红色。下列说法正确的是
Na2S4+3NaBr。闭合开关K时,b极附近先变红色。下列说法正确的是
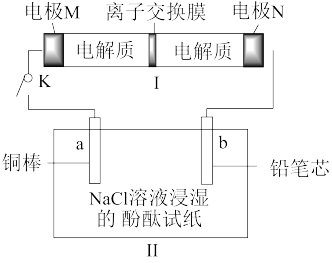
 Na2S4+3NaBr。闭合开关K时,b极附近先变红色。下列说法正确的是
Na2S4+3NaBr。闭合开关K时,b极附近先变红色。下列说法正确的是
A.闭合 后,b电极附近的pH变小 后,b电极附近的pH变小 |
| B.当有0.01molNa+通过离子交换膜时,b电极上析出气体体积为112mL |
C. 极是负极,电极反应为2Na2S2-2e-=2Na++Na2S4 极是负极,电极反应为2Na2S2-2e-=2Na++Na2S4 |
| D.闭合K后,a电极上产生的气体具有漂白性 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】以锂硫电池(电池的总反应为2Li + xS= Li2Sx )为电源,电解含(NH4)2SO4的废水制备硫酸和化肥的原理如图(不考虑其他杂质离子的反应)。下列说法正确的是
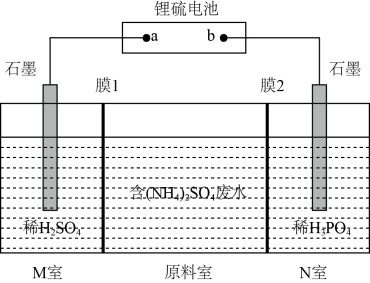

| A.膜1是阳离子交换膜,膜2是阴离子交换膜 |
| B.电解一段时间后,原料室中溶液的pH会增大 |
| C.N室的电极反应式为2H2O-4e-=O2↑+4H+ |
| D.锂硫电池每消耗2.8g锂,理论上M室产生2.24L气体 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】目前,光电催化反应器(PEC)可以有效地进行能源的转换和储存,一种PEC装置如图所示,通过光解水可由CO2制得主要产物异丙醇。下列说法错误的是
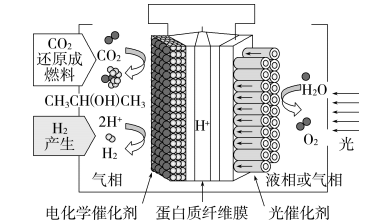

| A.该装置的能量来源为光能 |
B.光催化剂电极反应为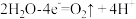 |
| C.H+从电化学催化剂电极一侧向右移动 |
| D.每生成60g异丙醇,电路中转移电子数日不一定为18NA |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列反应的离子方程式不正确的是
A.铅酸蓄电池充电时的阴极反应: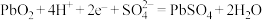 |
B.少量氯水滴入到碳酸钠溶液中: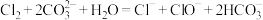 |
C.普通锌锰干电池(电解质主要成分为氯化铵)的正极反应: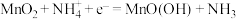 |
D.氯化铝溶液逐滴加入到过量的碳酸钠溶液中,并边加边振荡: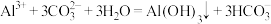 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列反应的离子方程式书写正确的是
A.用氨水吸收足量的 气体: 气体: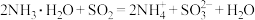 |
B.向 溶液中通入与 溶液中通入与 等物质的量的 等物质的量的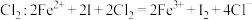 |
C.向 酸性溶液中滴入 酸性溶液中滴入 溶液: 溶液: |
D.用惰性电极电解饱和 溶液: 溶液: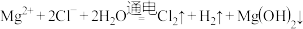 |
您最近一年使用:0次

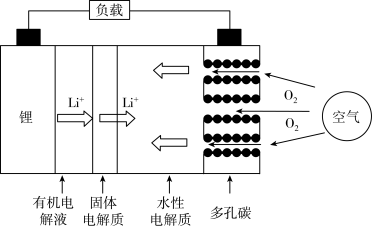
 的废水。下列说法正确的是
的废水。下列说法正确的是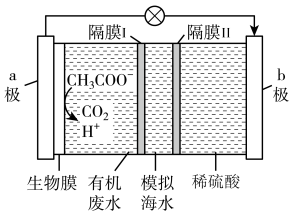
 通过隔膜II进入右室
通过隔膜II进入右室