回答下列问题
(1)联氨(又称肼,N2H4,无色液体)分子的电子式为____ ,其中氮的化合价为____ 。
(2)HClO的电子式为____ 。
(3)该气体(H2S)分子的电子式为____ 。
(4)以硼酸为原料可制得硼氢化钠(NaBH4),它是有机合成中的重要还原剂,其电子式为___________ 。
(5)H、C、N、O、Na、Al、S、Cl中任选元素组成一种四原子共价化合物,写出其电子式:____________ 。
(1)联氨(又称肼,N2H4,无色液体)分子的电子式为
(2)HClO的电子式为
(3)该气体(H2S)分子的电子式为
(4)以硼酸为原料可制得硼氢化钠(NaBH4),它是有机合成中的重要还原剂,其电子式为
(5)H、C、N、O、Na、Al、S、Cl中任选元素组成一种四原子共价化合物,写出其电子式:
2019高三·浙江·专题练习 查看更多[1]
(已下线)考点06 原子结构 化学键——备战2019年浙江新高考化学考点
更新时间:2019-03-04 15:20:47
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】我国在 催化加氢制取汽油方面取得突破性进展,
催化加氢制取汽油方面取得突破性进展, 转化过程如图所示:
转化过程如图所示:
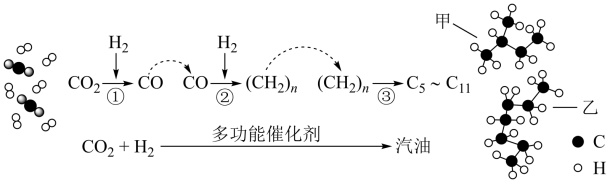
(1)二氧化碳分子的电子式为_______ 。
(2)图中有机物甲是汽油的成分之一,其名称为_______ ,其同分异构体有_______ 种。
(3)实验室常用纯净的碳酸钙与稀盐酸反应制取二氧化碳气体,反应过程中产生二氧化碳的体积(V)与时间(t)的关系如图所示:
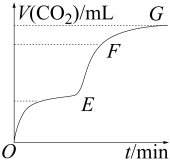
①由图象分析,化学反应速宰最快的是_______ (填字母)段。
②为了增大上述反应的速率。下列操作可行的是_______ (填字母)。
a.加蒸馏水 b.加氯化钠溶液 c.加浓盐酸 d.加热
(4)下面列出了几组物质,请将物质的合适组号填写在空格上。
同位素_______ ,同系物_______ ,同素异形体_______ ,同分异构体_______ 。
①金刚石与“足球烯”C60;②D与T;③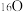 、
、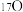 和
和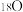 ;④氧气(
;④氧气( )与臭氧(
)与臭氧( );⑤
);⑤ 和癸烷;⑥
和癸烷;⑥ 和
和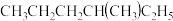 ;⑦
;⑦ 和
和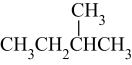
 催化加氢制取汽油方面取得突破性进展,
催化加氢制取汽油方面取得突破性进展, 转化过程如图所示:
转化过程如图所示:
(1)二氧化碳分子的电子式为
(2)图中有机物甲是汽油的成分之一,其名称为
(3)实验室常用纯净的碳酸钙与稀盐酸反应制取二氧化碳气体,反应过程中产生二氧化碳的体积(V)与时间(t)的关系如图所示:

①由图象分析,化学反应速宰最快的是
②为了增大上述反应的速率。下列操作可行的是
a.加蒸馏水 b.加氯化钠溶液 c.加浓盐酸 d.加热
(4)下面列出了几组物质,请将物质的合适组号填写在空格上。
同位素
①金刚石与“足球烯”C60;②D与T;③
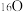 、
、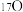 和
和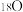 ;④氧气(
;④氧气( )与臭氧(
)与臭氧( );⑤
);⑤ 和癸烷;⑥
和癸烷;⑥ 和
和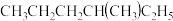 ;⑦
;⑦ 和
和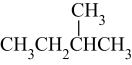
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】按要求回答下列问题:
(1)钡餐的化学式_______ ,氨气的电子式_______ 。
(2)写出工业制粗硅的化学反应方程式_______ 。
(3)工业制乙醇的化学方程式_______ 。
(4)已知 有两种结构,其中一种是
有两种结构,其中一种是 ,另一种结构简式是
,另一种结构简式是_______ 。
(1)钡餐的化学式
(2)写出工业制粗硅的化学反应方程式
(3)工业制乙醇的化学方程式
(4)已知
 有两种结构,其中一种是
有两种结构,其中一种是 ,另一种结构简式是
,另一种结构简式是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】按要求填空
(1)写出下列物质的电子式:
①KCl___________ ②MgCl2 ___________ ③Cl2___________
④N2___________ ⑤H2O___________ ⑥CH4___________
(2)写出下列反应的化学方程式。
①锂在空气中燃烧:___________ ;
②钾与水反应:___________ ;
③溴与碘化钾反应:___________ ;
④氯化亚铁与氯气反应:___________ ;
(1)写出下列物质的电子式:
①KCl
④N2
(2)写出下列反应的化学方程式。
①锂在空气中燃烧:
②钾与水反应:
③溴与碘化钾反应:
④氯化亚铁与氯气反应:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】如表是元素周期表的一部分。回答下列问题:
(1)地球上99%的溴元素存在于海水中,因此溴被称为“海洋元素”。
①该表中溴在元素周期表中的位置为____________ 。
②该表中最高价氧化物对应的水化物酸性最强的是______ (填化学式),该元素形成化合物HXO的结构式为______ (X用对应元素符号表示)。
③卤素互化物(如IBr)与卤素单质性质相似。已知IBr能与水发生非氧化还原反应,写出IBr与水反应的化学方程式____________ ,IBr中含有的化学键是______ (填“离子键”、“极性键”或“非极性键”)。
(2) 溶于水形成
溶于水形成 溶液,向所得溶液中通入
溶液,向所得溶液中通入 气体,反应生成Se和
气体,反应生成Se和 。写出
。写出 与
与 反应的化学方程式
反应的化学方程式____________ 。
(3)已知某主族元素离子结构示意图为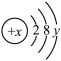 ,其中
,其中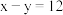 ,此元素与氯元素组成化合物的电子式为
,此元素与氯元素组成化合物的电子式为______ 。
16 S 硫 32.06 | 17 Cl 氯 35.45 |
34 Se 硒 78.96 | 35 Br 溴 79.90 |
53 I 碘 126.9 |
(1)地球上99%的溴元素存在于海水中,因此溴被称为“海洋元素”。
①该表中溴在元素周期表中的位置为
②该表中最高价氧化物对应的水化物酸性最强的是
③卤素互化物(如IBr)与卤素单质性质相似。已知IBr能与水发生非氧化还原反应,写出IBr与水反应的化学方程式
(2)
 溶于水形成
溶于水形成 溶液,向所得溶液中通入
溶液,向所得溶液中通入 气体,反应生成Se和
气体,反应生成Se和 。写出
。写出 与
与 反应的化学方程式
反应的化学方程式(3)已知某主族元素离子结构示意图为
 ,其中
,其中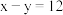 ,此元素与氯元素组成化合物的电子式为
,此元素与氯元素组成化合物的电子式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】如表为元素周期表的一部分,标出了A~K共十种元素所在位置。请用元素符号或化学式 回答下列问题。
(1)10种元素中,化学性质最不活泼的是______ ,最活泼的金属是_____ 。
(2)C、E、F三种元素形成的简单离子半径最小的是_______ 。
(3)化合物C2B2的电子式为__________________ ;该化合物和AB2反应的化学方程式为__________________________________________ 。
(4)E的最高价氧化物属于________________ 性氧化物,它与氢氧化钠溶液反应的离子方程式为____________________________________________ 。
(5)D的单质在A、B形成化合物中燃烧的化学方程式为________________________ 。
(6)用电子式表示H与B组成的H2B型化合物的形成过程_____________________ 。
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | A | B | ||||||
| 3 | C | D | E | F | G | |||
| 4 | H | I | K |
(1)10种元素中,化学性质最不活泼的是
(2)C、E、F三种元素形成的简单离子半径最小的是
(3)化合物C2B2的电子式为
(4)E的最高价氧化物属于
(5)D的单质在A、B形成化合物中燃烧的化学方程式为
(6)用电子式表示H与B组成的H2B型化合物的形成过程
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】(1)比较给出 能力的相对强弱:
能力的相对强弱:
___________ (填 “>”“<”或“=”) ;用一个化学方程式说明
;用一个化学方程式说明 和
和 结合
结合 能力的相对强弱:
能力的相对强弱:_________ 。
(2)草酸钙( )是离子化合物,各原子均满足8电子稳定结构。写出
)是离子化合物,各原子均满足8电子稳定结构。写出 的电子式:
的电子式:____________ 。
(3)甘油、乙二醇等多羟基化合物,这些物质通常为黏稠状液体,主要原因是____________ 。
 能力的相对强弱:
能力的相对强弱:
 ;用一个化学方程式说明
;用一个化学方程式说明 和
和 结合
结合 能力的相对强弱:
能力的相对强弱:(2)草酸钙(
 )是离子化合物,各原子均满足8电子稳定结构。写出
)是离子化合物,各原子均满足8电子稳定结构。写出 的电子式:
的电子式:(3)甘油、乙二醇等多羟基化合物,这些物质通常为黏稠状液体,主要原因是
您最近一年使用:0次



