按要求填空
(1)写出下列物质的电子式:
①KCl___________ ②MgCl2 ___________ ③Cl2___________
④N2___________ ⑤H2O___________ ⑥CH4___________
(2)写出下列反应的化学方程式。
①锂在空气中燃烧:___________ ;
②钾与水反应:___________ ;
③溴与碘化钾反应:___________ ;
④氯化亚铁与氯气反应:___________ ;
(1)写出下列物质的电子式:
①KCl
④N2
(2)写出下列反应的化学方程式。
①锂在空气中燃烧:
②钾与水反应:
③溴与碘化钾反应:
④氯化亚铁与氯气反应:
更新时间:2022-05-23 07:56:53
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】现有以下物质:①N2②KBr ③MgCl2④H2O ⑤CaF2 ⑥NH4Cl ⑦NaOH ⑧CO2⑨HClO
(1)既含有共价键又含有离子键的化合物是_______ ;属于共价化合物的是_______ ;属于离子化合物的是_______ 。
(2)将物质②溶于水,破坏了②中的_______ (填化学键类型),物质②熔融状态_______ (填“能”或“不能”)导电。
(3)请写出①和⑤的电子式:①_______ ,⑤_______ 。
(4)请用电子式表示④的形成过程_______ 。
(1)既含有共价键又含有离子键的化合物是
(2)将物质②溶于水,破坏了②中的
(3)请写出①和⑤的电子式:①
(4)请用电子式表示④的形成过程
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】完成下列问题
(1)请用下列10种物质的序号填空:①O2 ②H2 ③NH4NO3 ④K2O2 ⑤Ba(OH)2 ⑥CH4 ⑦CO2 ⑧NaF ⑨NH3 ⑩I2,只含有极性键的是_______ ,既有离子键又有非极性键的是_______ ,既有离子键又有极性键的是_______ 。
(2)X、Y两种主族元素能形成XY2型化合物,已知XY2中共有38个电子,若XY2为常见元素形成的离子化合物,其电子式为:_______ ;若XY2为共价化合物时,其结构式为:_______ 。
(1)请用下列10种物质的序号填空:①O2 ②H2 ③NH4NO3 ④K2O2 ⑤Ba(OH)2 ⑥CH4 ⑦CO2 ⑧NaF ⑨NH3 ⑩I2,只含有极性键的是
(2)X、Y两种主族元素能形成XY2型化合物,已知XY2中共有38个电子,若XY2为常见元素形成的离子化合物,其电子式为:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】I.下表是元素周期表的一部分,针对表中的①~⑩种元素,填写下列空白:
(1)在这些元素中,化学性质最不活泼的是:________ (填元素符号),
(2)在最高价氧化物对应的水化物中,碱性最强的化合物是________ (填化学式),在常温下该化合物和元素⑦的单质反应的离子方程式__________ 。
(3)用电子式表示元素④与⑥的化合物的形成过程:__________ 。
(4)表示①与⑦的化合物的电子式_______ ,该化合物是由______ (填“极性”或“非极性”)键形成的。
(5)③、⑥、⑦三种元素形成的离子,离子半径由大到小的顺序是____________ (用化学式表示)。
II.①CaBr2;②H2O;③NH4Cl;④H2O2;⑤Na2O2;⑥Ca(OH)2;⑦HClO;⑧I2;⑨He
只含有离子键的是(用序号回答)_____ ,即含离子键又含共价键是(用序号回答)_____ ,其中含有非极性共价键的共价化合物是(用序号回答)_____ ,常温时为固体,当其熔化时,不破坏化学键的是(用序号回答)_____ 。
| 主族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0族 |
| 第二周期 | ① | ② | ③ | |||||
| 第三周期 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 第四周期 | ⑨ | ⑩ |
(1)在这些元素中,化学性质最不活泼的是:
(2)在最高价氧化物对应的水化物中,碱性最强的化合物是
(3)用电子式表示元素④与⑥的化合物的形成过程:
(4)表示①与⑦的化合物的电子式
(5)③、⑥、⑦三种元素形成的离子,离子半径由大到小的顺序是
II.①CaBr2;②H2O;③NH4Cl;④H2O2;⑤Na2O2;⑥Ca(OH)2;⑦HClO;⑧I2;⑨He
只含有离子键的是(用序号回答)
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】叠氮化钠(NaN3)可用于汽车安全气囊的产气药。一种由氨基化钠(NaNH2)制备NaN3的工艺流程如图。
①钠元素位于周期表第_____ 周期_____ 族。
②NaNH2中氮元素的化合价为_____ 。
③用单线桥 标出该反应电子转移的方向和数目_____ 。
(2)NaOH的电子式为_____ ,流程中“反应”的化学方程式为_____ 。
(3)NaN3在撞击时能发生分解反应生成两种单质。计算理论上65gNaN3完全分解,释放出标准状况下的气体体积为_____ L。
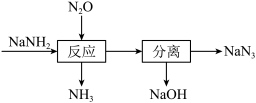
①钠元素位于周期表第
②NaNH2中氮元素的化合价为
③用
(2)NaOH的电子式为
(3)NaN3在撞击时能发生分解反应生成两种单质。计算理论上65gNaN3完全分解,释放出标准状况下的气体体积为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】氮肥的大量使用排出的废水是造成河流及湖泊富营养化的主要因素之一、氨氮废水中的氮元素多以 和
和 等形式存在。电解法处理氨氮酸性废水已引起广泛关注。研究表明,当以碳为阴极,
等形式存在。电解法处理氨氮酸性废水已引起广泛关注。研究表明,当以碳为阴极, 可在阴极生成
可在阴极生成 ,并进一步生成电中性且氧化性极强的羟基自由基(・OH),
,并进一步生成电中性且氧化性极强的羟基自由基(・OH), 可以将氨氮氧化为N2。
可以将氨氮氧化为N2。
1.写出 的电子式
的电子式___________ 。
2.阴极生成H2O2的电极反应为:___________ 。氨氮氧化生成2.24LN2(标准状况),转移电子数为:___________ 。
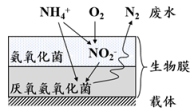
3.生物膜式厌氧氨氧化是一种较先进的氨氮废水处理工艺,通过在填料上附着不同菌种的生物膜来实现低能耗脱氨氮,其过程如图所示。___________ 。
 和
和 等形式存在。电解法处理氨氮酸性废水已引起广泛关注。研究表明,当以碳为阴极,
等形式存在。电解法处理氨氮酸性废水已引起广泛关注。研究表明,当以碳为阴极, 可在阴极生成
可在阴极生成 ,并进一步生成电中性且氧化性极强的羟基自由基(・OH),
,并进一步生成电中性且氧化性极强的羟基自由基(・OH), 可以将氨氮氧化为N2。
可以将氨氮氧化为N2。1.写出
 的电子式
的电子式2.阴极生成H2O2的电极反应为:
3.生物膜式厌氧氨氧化是一种较先进的氨氮废水处理工艺,通过在填料上附着不同菌种的生物膜来实现低能耗脱氨氮,其过程如图所示。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】氯是一种生产生活中常见的元素,下图是几种含氯产品。

(1)Cl2是有毒气体,为了防止多余Cl2污染空气,需要上图装置进行尾气处理,用化学方程式表示该原理___________ 。气体应该由___________ (填a或b)管通入。若要吸收标准状况下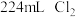 ,至少需要1mol/L的上述溶液
,至少需要1mol/L的上述溶液___________ mL。
(2)工业上制取漂白粉的化学方程式是___________ 。
(3)抗击新冠肺炎的战役中使用了大量的84消毒液。同学们探究84消毒液在不同pH下使红纸褪色的情况,做了如下实验。将5mL市售84消毒液稀释100倍,测得稀释后溶液的 ,将稀释后溶液各20mL分别加入a、b、c三个洁净的烧杯中:
,将稀释后溶液各20mL分别加入a、b、c三个洁净的烧杯中:
已知溶液中 、HClO和
、HClO和 的物质的量分数(a)随溶液pH变化的关系如图所示:
的物质的量分数(a)随溶液pH变化的关系如图所示:
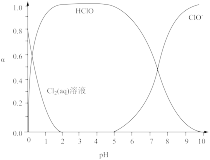
①由实验现象可获得结论:溶液的pH在4~10范围内,pH越大,红纸褪色___________ (填“越快”或“越慢”)。
②结合图象进行分析,b、c两烧杯中实验现象出现差异的原因是___________ 。

(1)Cl2是有毒气体,为了防止多余Cl2污染空气,需要上图装置进行尾气处理,用化学方程式表示该原理
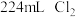 ,至少需要1mol/L的上述溶液
,至少需要1mol/L的上述溶液(2)工业上制取漂白粉的化学方程式是
(3)抗击新冠肺炎的战役中使用了大量的84消毒液。同学们探究84消毒液在不同pH下使红纸褪色的情况,做了如下实验。将5mL市售84消毒液稀释100倍,测得稀释后溶液的
 ,将稀释后溶液各20mL分别加入a、b、c三个洁净的烧杯中:
,将稀释后溶液各20mL分别加入a、b、c三个洁净的烧杯中:| 烧杯 | 溶液pH | 现象 |
| a | 10 | 10min后,红纸基本不褪色;4h后红纸褪色 |
| b | 7 | 10min后,红纸颜色变浅;4h后红纸褪色 |
| c | 4 | 10min后,红纸颜色比b烧杯中10min后的浅;4h后红纸褪色 |
 、HClO和
、HClO和 的物质的量分数(a)随溶液pH变化的关系如图所示:
的物质的量分数(a)随溶液pH变化的关系如图所示:
①由实验现象可获得结论:溶液的pH在4~10范围内,pH越大,红纸褪色
②结合图象进行分析,b、c两烧杯中实验现象出现差异的原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】工业上,我们用电解饱和食盐水制取氯气,请写出其中的化学方程式:_______ ,阳极产物是_______ 。实验室制备氯气时,为防止氯气污染空气,通常将氯气通入氢氧化钠溶液中,写出化学方程式:_______ ;对应的离子方程式_______ 。
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】 溶液和84消毒液是生活中常用的两种消毒剂。请回答下列问题:
溶液和84消毒液是生活中常用的两种消毒剂。请回答下列问题:
(1)某同学设计如下实验研究 的性质:
的性质:
①理论上 既有氧化性又有还原性,具有还原性的原因是
既有氧化性又有还原性,具有还原性的原因是_______ 。
②能证明 具有还原性的是实验
具有还原性的是实验_______ (填序号)。
(2)84消毒液的有效成分为 。
。
①NaClO中Cl元素的化合价是_______ 。
②84消毒液不能用于钢制器具的消毒,原因是 具有
具有_______ 性。
③84消毒液吸收空气中的 ,其消毒杀菌能力增强,该过程中发生反应的化学方程式为
,其消毒杀菌能力增强,该过程中发生反应的化学方程式为_______ 。
(3)漂白粉在社会生活、工业生产中用途广泛。漂白粉除了具有漂白作用外,还能杀菌、消毒。
已知漂白粉溶于水后加入少量的酸能增强漂白效果。某同学据此将少量漂白粉溶于水后,再加入浓盐酸,观察到有黄绿色气体生成。回答下列问题:
①生成黄绿色气体的化学方程式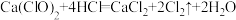 ,用双线桥表示反应电子转移方向和数目:
,用双线桥表示反应电子转移方向和数目:_______ 。
②家庭生活中常使用“84”消毒液进行消毒。这种消毒液和某品牌洁厕净(主要成分为盐酸)_______ (填“能”或“不能”)同时使用,其原因是_______ 。
 溶液和84消毒液是生活中常用的两种消毒剂。请回答下列问题:
溶液和84消毒液是生活中常用的两种消毒剂。请回答下列问题:(1)某同学设计如下实验研究
 的性质:
的性质:| 实验 | 操作 | 现象 |
| i | 向5% 溶液中滴加酸性 溶液中滴加酸性 溶液 溶液 | a.溶液紫色褪去 b.有大量气泡产生 |
| ii | 向5% 溶液中滴加淀粉碘化钾溶液 溶液中滴加淀粉碘化钾溶液 | c.溶液变蓝 |
 既有氧化性又有还原性,具有还原性的原因是
既有氧化性又有还原性,具有还原性的原因是②能证明
 具有还原性的是实验
具有还原性的是实验(2)84消毒液的有效成分为
 。
。①NaClO中Cl元素的化合价是
②84消毒液不能用于钢制器具的消毒,原因是
 具有
具有③84消毒液吸收空气中的
 ,其消毒杀菌能力增强,该过程中发生反应的化学方程式为
,其消毒杀菌能力增强,该过程中发生反应的化学方程式为(3)漂白粉在社会生活、工业生产中用途广泛。漂白粉除了具有漂白作用外,还能杀菌、消毒。
已知漂白粉溶于水后加入少量的酸能增强漂白效果。某同学据此将少量漂白粉溶于水后,再加入浓盐酸,观察到有黄绿色气体生成。回答下列问题:
①生成黄绿色气体的化学方程式
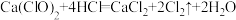 ,用双线桥表示反应电子转移方向和数目:
,用双线桥表示反应电子转移方向和数目:②家庭生活中常使用“84”消毒液进行消毒。这种消毒液和某品牌洁厕净(主要成分为盐酸)
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】物质类别和核心元素的价态是学习元素及其化合物性质的两个重要认识视角。图为钠及其化合物的“价-类”二维图,请回答下列问题:
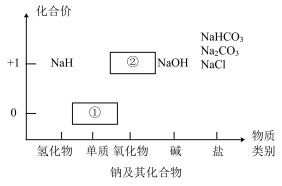
(1)物质①与水反应的离子方程式为_____________________________ 。
(2)写出淡黄色固体②与二氧化碳反应的化学方程式并用双线桥表示出电子转移的方向和数目_____________________________ 。
(3)从核心元素价态的视角看, 中H元素的化合价为
中H元素的化合价为_________ ,从H元素的价态分析, 常用作
常用作_________ (填“氧化剂”或“还原剂”)。
(4)某化学小组设计了下列实验方案鉴别 和
和 两种白色粉末,其中不能达到预期目的的是
两种白色粉末,其中不能达到预期目的的是_________ (填编号)。
①分别向等质量的白色粉末中加等体积、等浓度的稀盐酸,比较生成气体的快慢
②分别向等质量的白色粉末中加少量等体积的水,比较固体温度的变化
③分别将等质量的白色粉末配成溶液,然后加入澄清石灰水,比较是否有沉淀生成
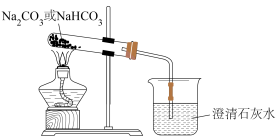
④分别将等质量的白色粉末加热(如图所示),比较澄清石灰水是否变浑浊
(5)纯碱是人类最早制取和使用的化学物质之一,其属于_________ (填“酸”、“碱”、“盐”或“氧化物”)。我国化学家侯德榜发明了联合制碱法,制取方法是向饱和食盐水先通入足量 ,再通入过量
,再通入过量 ,析出
,析出_____________ (填化学式)晶体。

(1)物质①与水反应的离子方程式为
(2)写出淡黄色固体②与二氧化碳反应的化学方程式并用双线桥表示出电子转移的方向和数目
(3)从核心元素价态的视角看,
 中H元素的化合价为
中H元素的化合价为 常用作
常用作(4)某化学小组设计了下列实验方案鉴别
 和
和 两种白色粉末,其中不能达到预期目的的是
两种白色粉末,其中不能达到预期目的的是①分别向等质量的白色粉末中加等体积、等浓度的稀盐酸,比较生成气体的快慢
②分别向等质量的白色粉末中加少量等体积的水,比较固体温度的变化
③分别将等质量的白色粉末配成溶液,然后加入澄清石灰水,比较是否有沉淀生成
④分别将等质量的白色粉末加热(如图所示),比较澄清石灰水是否变浑浊

(5)纯碱是人类最早制取和使用的化学物质之一,其属于
 ,再通入过量
,再通入过量 ,析出
,析出
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】回答下列问题
(1)补齐物质及其用途的连线。______
(2)金属钠可以去除某些有机溶剂中的水分,用离子反应方程式解释其原因:______ 。
(1)补齐物质及其用途的连线。
| 物质 | 用途 |
| A.过氧化钠 | a.作消毒剂 |
| B.金属钠 | b.供氧剂 |
| C.碳酸钠 | c.去除某些有机溶剂中的水分 |
| D.次氯酸钠 | d.作食用碱 |
您最近一年使用:0次

 是N2的等电子体,写出CO、
是N2的等电子体,写出CO、 、CH
、CH


