化学计量在化学中占有重要地位。请回答下列问题:
(1)0.3 mol NH3分子中所含原子数与约__________ 个H2O分子中所含原子数相等。
(2)V mL含a g Al3+的Al2(SO4)3溶液中所含SO42−的物质的量浓度为_____ mol·L−1。
(3)在一定温度和压强下,1体积气体X2与3体积Y2化合生成2体积气态化合物,该化合物的化学式为_________ 。
(4)将各0.3 mol的钠、镁、铝分别放入100 mL 1 mol·L−1的盐酸中,同温同压下产生气体的体积比为_____________ 。
(5)锌与很稀的硝酸反应生成硝酸锌、硝酸铵和水,当生成1 mol硝酸锌时,参加反应的硝酸的物质的量为_________ mol。
(1)0.3 mol NH3分子中所含原子数与约
(2)V mL含a g Al3+的Al2(SO4)3溶液中所含SO42−的物质的量浓度为
(3)在一定温度和压强下,1体积气体X2与3体积Y2化合生成2体积气态化合物,该化合物的化学式为
(4)将各0.3 mol的钠、镁、铝分别放入100 mL 1 mol·L−1的盐酸中,同温同压下产生气体的体积比为
(5)锌与很稀的硝酸反应生成硝酸锌、硝酸铵和水,当生成1 mol硝酸锌时,参加反应的硝酸的物质的量为
更新时间:2019/03/05 14:50:24
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】计算
(1)2.33gBaSO4的物质的量________ mol。
(2)标准状况下6.72L N2的物质的量________ mol。
(3)等质量的O2与O3在同温同压下的体积之比_______ 。
(4)同温同压同体积的CO2与SO2的质量之比________ 。
(5)同温同压下条件下CO与CO2的密度之比_________ 。
(1)2.33gBaSO4的物质的量
(2)标准状况下6.72L N2的物质的量
(3)等质量的O2与O3在同温同压下的体积之比
(4)同温同压同体积的CO2与SO2的质量之比
(5)同温同压下条件下CO与CO2的密度之比
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】回答下列问题
(1)等质量的 和
和 ,
, 与
与 的物质的量之比是
的物质的量之比是_______ ,所含氧原子个数之比是_______ ;
(2)等质量的下列四种气体 、
、 、
、 、
、 ,在相同温度和压强条件下,体积最大的是
,在相同温度和压强条件下,体积最大的是_______ ;
(3)标准状况下,体积为 的
的 所含质子数目为
所含质子数目为_______ ;
(4)设 为阿伏加德罗常数的数值,如果ag某未知气体中含有的分子数为b,则cg该气体在标准状况下的体积约为
为阿伏加德罗常数的数值,如果ag某未知气体中含有的分子数为b,则cg该气体在标准状况下的体积约为_______ 
(1)等质量的
 和
和 ,
, 与
与 的物质的量之比是
的物质的量之比是(2)等质量的下列四种气体
 、
、 、
、 、
、 ,在相同温度和压强条件下,体积最大的是
,在相同温度和压强条件下,体积最大的是(3)标准状况下,体积为
 的
的 所含质子数目为
所含质子数目为(4)设
 为阿伏加德罗常数的数值,如果ag某未知气体中含有的分子数为b,则cg该气体在标准状况下的体积约为
为阿伏加德罗常数的数值,如果ag某未知气体中含有的分子数为b,则cg该气体在标准状况下的体积约为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】完成下列问题
(1)相同物质量的 和
和 的质量比为
的质量比为_______ 。
(2)2.5mol NaOH中含有_______ 个 ,2.5mol NaOH的质量是
,2.5mol NaOH的质量是_______ g。
(3)在标准状况下,1.7g氨气所占的体积约为_______ L,它与标准状况_______ L硫化氢含有相同数目的氢原子。
(4)已知硫酸钠晶体( )的物质的量为1.5mol,所含钠离子的物质的量是
)的物质的量为1.5mol,所含钠离子的物质的量是_______ ,钠离子的数目是_______ 。
(5)在某气态氧化物化学式为 ,在标准状况下,1.28g该氧化物的体积为448mL,则该氧化物的摩尔质量为
,在标准状况下,1.28g该氧化物的体积为448mL,则该氧化物的摩尔质量为_______ 。
(1)相同物质量的
 和
和 的质量比为
的质量比为(2)2.5mol NaOH中含有
 ,2.5mol NaOH的质量是
,2.5mol NaOH的质量是(3)在标准状况下,1.7g氨气所占的体积约为
(4)已知硫酸钠晶体(
 )的物质的量为1.5mol,所含钠离子的物质的量是
)的物质的量为1.5mol,所含钠离子的物质的量是(5)在某气态氧化物化学式为
 ,在标准状况下,1.28g该氧化物的体积为448mL,则该氧化物的摩尔质量为
,在标准状况下,1.28g该氧化物的体积为448mL,则该氧化物的摩尔质量为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】2019年,为纪念元素周期表脠生150周年,IUPAC等向世界介绍118位优秀青年化学家,中国学者雷晓光、姜雪峰、刘庄分别成为“N、S、Hg”元素的代言人。回答下列问题:
(1)合成氨工业化,对人类影响深远。工业上合成氨的化学方程式为______ 。
(2)①叠氮化钠(NaN3)可用于汽车安全气囊的产气药,NaN3在撞击时能发生分解反应生成两种单质。计算理论上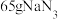 完全分解,释放出标准状况下的气体体积
完全分解,释放出标准状况下的气体体积______ L。
②氮化铝(AlN)具有耐高温、抗冲击、导热性好等优良性质,工业将氧化铝、氮气和碳在一定条件下反应制得AlN和 ,请写出该反应的方程式:
,请写出该反应的方程式:______ 。
(3)利用元素的化合价推测物质的性质是化学研究的重要手段。如图是硫元素的“价一类”二维图:
①从硫元素化合价变化的角度分析,图中既有氧化性又有还原性的化合物有______ (填化学式)。
② 的浓溶液与铝单质在加热条件下可以发生化学反应生成
的浓溶液与铝单质在加热条件下可以发生化学反应生成 ,该反应的化学方程式为
,该反应的化学方程式为______ ,可用______ 法收集Y。(填序号)

A.向上排空气 B.向下排空气 C.排饱和食盐水 D.排饱和 溶液
溶液
③ 和
和 均能使品红溶液褪色,但两种气体按一定比例同时通入品红溶液中无明显现象。请用离子方程式解释原因
均能使品红溶液褪色,但两种气体按一定比例同时通入品红溶液中无明显现象。请用离子方程式解释原因______ 。
(1)合成氨工业化,对人类影响深远。工业上合成氨的化学方程式为
(2)①叠氮化钠(NaN3)可用于汽车安全气囊的产气药,NaN3在撞击时能发生分解反应生成两种单质。计算理论上
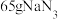 完全分解,释放出标准状况下的气体体积
完全分解,释放出标准状况下的气体体积②氮化铝(AlN)具有耐高温、抗冲击、导热性好等优良性质,工业将氧化铝、氮气和碳在一定条件下反应制得AlN和
 ,请写出该反应的方程式:
,请写出该反应的方程式:(3)利用元素的化合价推测物质的性质是化学研究的重要手段。如图是硫元素的“价一类”二维图:
①从硫元素化合价变化的角度分析,图中既有氧化性又有还原性的化合物有
②
 的浓溶液与铝单质在加热条件下可以发生化学反应生成
的浓溶液与铝单质在加热条件下可以发生化学反应生成 ,该反应的化学方程式为
,该反应的化学方程式为
A.向上排空气 B.向下排空气 C.排饱和食盐水 D.排饱和
 溶液
溶液③
 和
和 均能使品红溶液褪色,但两种气体按一定比例同时通入品红溶液中无明显现象。请用离子方程式解释原因
均能使品红溶液褪色,但两种气体按一定比例同时通入品红溶液中无明显现象。请用离子方程式解释原因
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】(1)工业尾气中 和
和 ,可被吸收制备
,可被吸收制备 和
和 ,其流程图如下:
,其流程图如下:
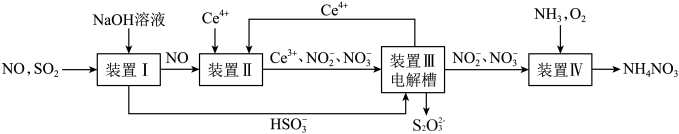
①装置Ⅰ中的主要反应的离子方程式为__________________ .
②经过装置Ⅲ后的 与
与 的物质的量的比值为
的物质的量的比值为___________ .
(2) 催化还原是烟气中氮氧化物脱除最佳技术,反应原理如图1左所示.
催化还原是烟气中氮氧化物脱除最佳技术,反应原理如图1左所示.
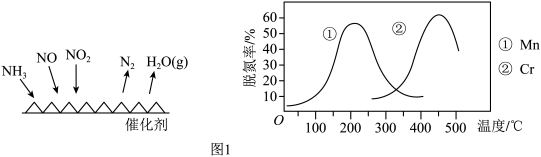
①图1右是不同催化剂 和
和 不同温度下对应的脱氮率,由图综合考虑可知最佳的催化剂和相应的温度分别为:
不同温度下对应的脱氮率,由图综合考虑可知最佳的催化剂和相应的温度分别为:_______ (填序号).
a. ,200℃左右 b.
,200℃左右 b. ,450℃左右 c.
,450℃左右 c. 和
和 混合,300℃左右
混合,300℃左右
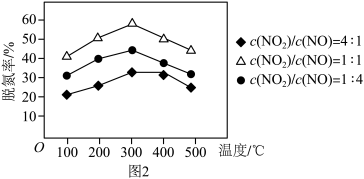
②图2是 做催化剂时的脱氮率,写出最佳脱氮率时发生反应的化学方程式
做催化剂时的脱氮率,写出最佳脱氮率时发生反应的化学方程式_________________ .
 和
和 ,可被吸收制备
,可被吸收制备 和
和 ,其流程图如下:
,其流程图如下:
①装置Ⅰ中的主要反应的离子方程式为
②经过装置Ⅲ后的
 与
与 的物质的量的比值为
的物质的量的比值为(2)
 催化还原是烟气中氮氧化物脱除最佳技术,反应原理如图1左所示.
催化还原是烟气中氮氧化物脱除最佳技术,反应原理如图1左所示.
①图1右是不同催化剂
 和
和 不同温度下对应的脱氮率,由图综合考虑可知最佳的催化剂和相应的温度分别为:
不同温度下对应的脱氮率,由图综合考虑可知最佳的催化剂和相应的温度分别为:a.
 ,200℃左右 b.
,200℃左右 b. ,450℃左右 c.
,450℃左右 c. 和
和 混合,300℃左右
混合,300℃左右②图2是
 做催化剂时的脱氮率,写出最佳脱氮率时发生反应的化学方程式
做催化剂时的脱氮率,写出最佳脱氮率时发生反应的化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】金属钠及其化合物在材料和工业生产方面有着重要作用。
Ⅰ.Na的生产和性质。
(1) 的熔点为
的熔点为 ,但加入
,但加入 形成混合盐后
形成混合盐后 的熔点降低到580℃,故工业上,采用电解熔融的混合盐来制备金属
的熔点降低到580℃,故工业上,采用电解熔融的混合盐来制备金属 ,电解的化学方程式为:
,电解的化学方程式为: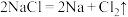 ,加入
,加入 的目的是
的目的是___________ 。
(2)将金属钠放入盛有下列溶液的小烧杯中,既有气体产生,又有沉淀产生的是___________ (填序号)。
① 溶液 ②
溶液 ② 溶液 ③
溶液 ③ 溶液 ④饱和的澄清石灰水 ⑤
溶液 ④饱和的澄清石灰水 ⑤ 溶液 ⑥
溶液 ⑥ 溶液 ⑦
溶液 ⑦ 溶液
溶液
Ⅱ. 是
是 的重要氧化物。
的重要氧化物。
(3) 的电子式是
的电子式是___________ 。
(4)向酸性 溶液中加入
溶液中加入 粉末,观察到溶液褪色,配平下述反应方程式
粉末,观察到溶液褪色,配平下述反应方程式____________
 →
→
(5)200℃时,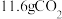 和
和 的混合气体与足量的
的混合气体与足量的 反应,反应后固体增加了
反应,反应后固体增加了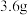 ,则原混合气体的平均摩尔质量为
,则原混合气体的平均摩尔质量为___________  。
。
Ⅲ.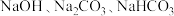 之间在一定条件下能相互转化。
之间在一定条件下能相互转化。
(6)向 中通入一定量的
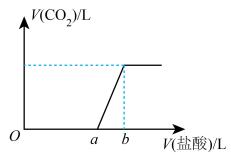
中通入一定量的 气体,充分反应得到溶液X后,再向所得溶液X中逐滴加入稀盐酸。产生
气体,充分反应得到溶液X后,再向所得溶液X中逐滴加入稀盐酸。产生 的体积与所加盐酸体积之间的关系如图所示,完成下列表格:
的体积与所加盐酸体积之间的关系如图所示,完成下列表格:
Ⅰ.Na的生产和性质。
(1)
 的熔点为
的熔点为 ,但加入
,但加入 形成混合盐后
形成混合盐后 的熔点降低到580℃,故工业上,采用电解熔融的混合盐来制备金属
的熔点降低到580℃,故工业上,采用电解熔融的混合盐来制备金属 ,电解的化学方程式为:
,电解的化学方程式为: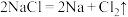 ,加入
,加入 的目的是
的目的是(2)将金属钠放入盛有下列溶液的小烧杯中,既有气体产生,又有沉淀产生的是
①
 溶液 ②
溶液 ② 溶液 ③
溶液 ③ 溶液 ④饱和的澄清石灰水 ⑤
溶液 ④饱和的澄清石灰水 ⑤ 溶液 ⑥
溶液 ⑥ 溶液 ⑦
溶液 ⑦ 溶液
溶液Ⅱ.
 是
是 的重要氧化物。
的重要氧化物。(3)
 的电子式是
的电子式是(4)向酸性
 溶液中加入
溶液中加入 粉末,观察到溶液褪色,配平下述反应方程式
粉末,观察到溶液褪色,配平下述反应方程式 →
→
(5)200℃时,
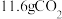 和
和 的混合气体与足量的
的混合气体与足量的 反应,反应后固体增加了
反应,反应后固体增加了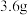 ,则原混合气体的平均摩尔质量为
,则原混合气体的平均摩尔质量为 。
。Ⅲ.
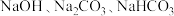 之间在一定条件下能相互转化。
之间在一定条件下能相互转化。(6)向
 中通入一定量的
中通入一定量的 气体,充分反应得到溶液X后,再向所得溶液X中逐滴加入稀盐酸。产生
气体,充分反应得到溶液X后,再向所得溶液X中逐滴加入稀盐酸。产生 的体积与所加盐酸体积之间的关系如图所示,完成下列表格:
的体积与所加盐酸体积之间的关系如图所示,完成下列表格:
| V(盐酸)/L | 溶液X溶质 | 通入 得到溶液X的离子方程式 得到溶液X的离子方程式 |
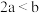 | ① | |
 | ② | |
 | ③ | ④ |
您最近一年使用:0次



