(1)某无色透明溶液可能存在Na+、Fe3+、Ba2+、NO3-、CO32-、HCO3-、SO42-中的几种离子,现有如下操作:
Ⅰ.取适量该溶液加入CaCl2溶液无沉淀,继续滴加盐酸产生无色无味的气体。
Ⅱ.另取该溶液滴加一定量的NaOH溶液有白色沉淀生成。
试回答下列问题:
①该溶液中一定存在的离子有__________,一定不存在的离子__________。
②用一个离子方程式表示操作②的实验现象:________________________。
(2)下列各项中的两种物质在溶液中的反应,可用同一离子方程式表示的是( ),请写出该离子反应方程式: ____________________________。
A.盐酸和烧碱溶液、硫酸和氢氧化钡溶液
B.纯碱溶液和盐酸、石灰石和硫酸
C.氯化钡溶液和硫酸钠溶液、硝酸钡溶液和硫酸
D.碳酸铵溶液和氢氧化钠溶液、碳酸铵溶液和氢氧化钙溶液
Ⅰ.取适量该溶液加入CaCl2溶液无沉淀,继续滴加盐酸产生无色无味的气体。
Ⅱ.另取该溶液滴加一定量的NaOH溶液有白色沉淀生成。
试回答下列问题:
①该溶液中一定存在的离子有__________,一定不存在的离子__________。
②用一个离子方程式表示操作②的实验现象:________________________。
(2)下列各项中的两种物质在溶液中的反应,可用同一离子方程式表示的是( ),请写出该离子反应方程式: ____________________________。
A.盐酸和烧碱溶液、硫酸和氢氧化钡溶液
B.纯碱溶液和盐酸、石灰石和硫酸
C.氯化钡溶液和硫酸钠溶液、硝酸钡溶液和硫酸
D.碳酸铵溶液和氢氧化钠溶液、碳酸铵溶液和氢氧化钙溶液
11-12高一上·云南玉溪·期中 查看更多[1]
(已下线)2011-2012学年云南省玉溪一中高一上学期期中考试化学试题试卷
更新时间:2016-12-09 02:09:38
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】回答下列问题:
(1)常温下盛装浓硝酸时可使用的容器是_______ (填“铁罐”或“铜罐”)。
(2)实验室用于盛放碱性试剂的试剂瓶不用磨口玻璃塞的原因是(用化学方程式表示):_______ 。
(3)胃液中含有盐酸,胃酸过多常有胃疼烧心的感觉,服用含有小苏打的药品可以中和胃酸,其反应的离子方程式为:_______ 。
(4)肉制品加工中使用发色剂亚硝酸钠 时必须严格控制用量。误食
时必须严格控制用量。误食 会导致血红蛋白中的
会导致血红蛋白中的 转化为
转化为 而中毒,服用维生素C可以解除
而中毒,服用维生素C可以解除 引起的中毒。这说明维生素C具有
引起的中毒。这说明维生素C具有_______ (填“氧化性”或“还原性”)。
(5)我国古代四大发明之一的黑火药是由硫黄粉、硝酸钾和木炭粉按一定比例混合而成的,爆炸时的反应为: 。
。
①该反应中,还原剂是_______ (填化学式)。
②每消耗0.1molS,释放的气体体积为_______ L(换算成标准状况)。
(1)常温下盛装浓硝酸时可使用的容器是
(2)实验室用于盛放碱性试剂的试剂瓶不用磨口玻璃塞的原因是(用化学方程式表示):
(3)胃液中含有盐酸,胃酸过多常有胃疼烧心的感觉,服用含有小苏打的药品可以中和胃酸,其反应的离子方程式为:
(4)肉制品加工中使用发色剂亚硝酸钠
 时必须严格控制用量。误食
时必须严格控制用量。误食 会导致血红蛋白中的
会导致血红蛋白中的 转化为
转化为 而中毒,服用维生素C可以解除
而中毒,服用维生素C可以解除 引起的中毒。这说明维生素C具有
引起的中毒。这说明维生素C具有(5)我国古代四大发明之一的黑火药是由硫黄粉、硝酸钾和木炭粉按一定比例混合而成的,爆炸时的反应为:
 。
。①该反应中,还原剂是
②每消耗0.1molS,释放的气体体积为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】实验室制备氯化氢的反应化学方程式为:H2SO4(浓)+NaCl=HCl↑+NaHSO4,回答以下问题:
(1)该反应能发生的原因是________________ 。
A.硫酸酸性强于盐酸 B.盐酸易挥发 C.硫酸氧化性强于盐酸
(2)向NaHSO4溶液中滴加Ba(OH)2溶液至中性,反应的离子方程式为_____________________ 。
(3)实验室需要配制0.50 mol·L-1 NaCl溶液240 mL。
①所需的仪器有:托盘天平、药匙、烧杯、________ 、______ 、______ 以及等质量的两片滤纸。
②配制该溶液需取NaCl晶体______ g。
③配制一定物质的量浓度溶液定容时的操作是____________________________________
(4)在标准状况下,将44.8 L HCl气体溶于127 mL水中,所得盐酸的密度为1.18 g·cm-3。该盐酸的物质的量浓度是______________________ 。
(1)该反应能发生的原因是
A.硫酸酸性强于盐酸 B.盐酸易挥发 C.硫酸氧化性强于盐酸
(2)向NaHSO4溶液中滴加Ba(OH)2溶液至中性,反应的离子方程式为
(3)实验室需要配制0.50 mol·L-1 NaCl溶液240 mL。
①所需的仪器有:托盘天平、药匙、烧杯、
②配制该溶液需取NaCl晶体
③配制一定物质的量浓度溶液定容时的操作是
(4)在标准状况下,将44.8 L HCl气体溶于127 mL水中,所得盐酸的密度为1.18 g·cm-3。该盐酸的物质的量浓度是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】某化学小组甲同学学习了酸、碱、盐化学性质后展开了如下探究活动:
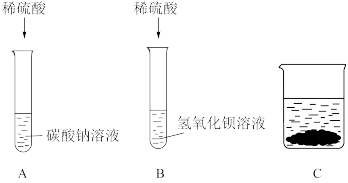
(1)B试管中发生反应的离子方程式为___________ 。
(2)【实验一】A、B试管中物质分别充分反应后,先将B试管中所有物质倒入空烧杯C中,再将A试管中所得溶液慢慢滴加到C烧杯中,烧杯内固体质量随A试管中加入液体质量变化如图一所示;

据此判断B试管中反应后所得溶液中的溶质是____ (填化学式)。
(3)【实验二】将C烧杯中沉淀过滤,向滤渣中加入过量稀硝酸,观察到____ 的实验现象,进而证明滤渣为混合物;
(4)【猜想与假设】实验二C烧杯的滤液中含有哪些离子?
猜想一:Na+、Ba2+、OH-
猜想二:Na+、H+、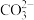
猜想三:Na+、OH-、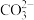
猜想四:Na+、OH-、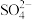
猜想五:___________ (写出一种即可);
小组同学一致认为猜想___________ 不正确,理由是___________ 。
(5)【实验探究】为确定最终滤液中溶质成分,小组同学向滤液中加入稀硫酸,观察到___________ 的实验现象,最终证明了溶液的溶质成分为Na+、Ba2+、OH-。向Ba(OH)2溶液中滴加稀H2SO4反应至过量,导电能力随时间变化的曲线图为___________ 。
A.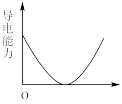 B.
B. C.
C.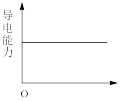 D.
D.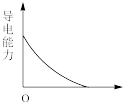
若将稀硫酸改为等浓度的Na2SO4溶液,测得的溶液的导电性曲线是否与上述曲线相同___________ 。(填“是”或“否”)

(1)B试管中发生反应的离子方程式为
(2)【实验一】A、B试管中物质分别充分反应后,先将B试管中所有物质倒入空烧杯C中,再将A试管中所得溶液慢慢滴加到C烧杯中,烧杯内固体质量随A试管中加入液体质量变化如图一所示;

据此判断B试管中反应后所得溶液中的溶质是
(3)【实验二】将C烧杯中沉淀过滤,向滤渣中加入过量稀硝酸,观察到
(4)【猜想与假设】实验二C烧杯的滤液中含有哪些离子?
猜想一:Na+、Ba2+、OH-
猜想二:Na+、H+、
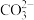
猜想三:Na+、OH-、
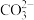
猜想四:Na+、OH-、
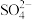
猜想五:
小组同学一致认为猜想
(5)【实验探究】为确定最终滤液中溶质成分,小组同学向滤液中加入稀硫酸,观察到
A.
 B.
B. C.
C. D.
D.
若将稀硫酸改为等浓度的Na2SO4溶液,测得的溶液的导电性曲线是否与上述曲线相同
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】常温下,酸性溶液A中可能含有NH4+、K+、Na+、Fe2+、Al3+、Fe3+、CO32-、NO3-、Cl-、I-、SO42-中的几种,现取该溶液进行有关实验,实验结果如下图所示:

回答下列问题:
(1)溶液A中一定存在的离子有___________________
(2)生成沉淀甲的离子方程式为___________________
(3)生成气体丙的离子方程式为__________________ ,若实验消耗Cu 144g,则最多生成气体丙的体积(标准状况下)为_____ 。
依据上述实验,某小组同学通过讨论后认为:溶液中可能含有的离子有NH4+、K+、Na+ 、Cl-、SO42-。为进一步确认溶液中存在的离子,分别取100ml废水又进行了如下图所示的三组实验:
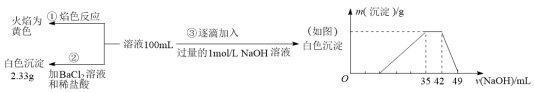
(4)根据上述实验可进一步确定NH4+、K+、Na+ 、Cl-、SO42-中一定存在的离子有_________ ,沉淀溶解时发生反应的离子方程式为________________________________ 。

回答下列问题:
(1)溶液A中一定存在的离子有
(2)生成沉淀甲的离子方程式为
(3)生成气体丙的离子方程式为
依据上述实验,某小组同学通过讨论后认为:溶液中可能含有的离子有NH4+、K+、Na+ 、Cl-、SO42-。为进一步确认溶液中存在的离子,分别取100ml废水又进行了如下图所示的三组实验:

(4)根据上述实验可进一步确定NH4+、K+、Na+ 、Cl-、SO42-中一定存在的离子有
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】为研究盛装浓硫酸的铁质材料(碳素钢)与热浓硫酸的反应,某学习小组进行了以下探究活动:
(1)[实验]
称取铁钉5.6g放入15.0mL浓硫酸中,加热,充分应后得到溶液X并收集到气体Y。
①甲同学认为X中除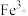 外还可能含有
外还可能含有 。若要确认其中的
。若要确认其中的 ,应选用
,应选用______ 选填序号)。
a.KSCN溶液和氯水 b.铁粉和KSCN溶液 c.浓氨水 d.酸性 溶液
溶液
②乙同学取448mL(标准状况)气体Y通入足量溴水中,发生的反应式为:Br2+SO2+2H2O=2HBr+H2SO4,然后加入足量 溶液,经适当操作后得干燥固体2.33g。由此推知气体Y中
溶液,经适当操作后得干燥固体2.33g。由此推知气体Y中 的体积分数为
的体积分数为____________ 。
(2)[提出猜想]
分析上述实验中 体积分数的结果,同学们认为气体Y中还可能含量有其它气体并作如下猜想:
体积分数的结果,同学们认为气体Y中还可能含量有其它气体并作如下猜想:
猜想一:Y气体中可能含有H2;
猜想二:________________ ;
猜想三:________________ ;
(3)[设计实验,验证猜想]
为验证以上猜想,同学们准备用下列装置设计探究实验(装置可重复使用,夹持仪器省略)。

①实验装置的连接顺序为A→____ →_____ → F →____ →______ →F(填字母)。
②装置B中试剂的作用是___________ 。
③猜想一的理由是______________________ (用化学方程式表示)。
④如果猜想一成立,预计实验现象应该是_____________________________ 。
(1)[实验]
称取铁钉5.6g放入15.0mL浓硫酸中,加热,充分应后得到溶液X并收集到气体Y。
①甲同学认为X中除
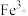 外还可能含有
外还可能含有 。若要确认其中的
。若要确认其中的 ,应选用
,应选用a.KSCN溶液和氯水 b.铁粉和KSCN溶液 c.浓氨水 d.酸性
 溶液
溶液②乙同学取448mL(标准状况)气体Y通入足量溴水中,发生的反应式为:Br2+SO2+2H2O=2HBr+H2SO4,然后加入足量
 溶液,经适当操作后得干燥固体2.33g。由此推知气体Y中
溶液,经适当操作后得干燥固体2.33g。由此推知气体Y中 的体积分数为
的体积分数为(2)[提出猜想]
分析上述实验中
 体积分数的结果,同学们认为气体Y中还可能含量有其它气体并作如下猜想:
体积分数的结果,同学们认为气体Y中还可能含量有其它气体并作如下猜想:猜想一:Y气体中可能含有H2;
猜想二:
猜想三:
(3)[设计实验,验证猜想]
为验证以上猜想,同学们准备用下列装置设计探究实验(装置可重复使用,夹持仪器省略)。

①实验装置的连接顺序为A→
②装置B中试剂的作用是
③猜想一的理由是
④如果猜想一成立,预计实验现象应该是
您最近一年使用:0次
【推荐3】有一包粉末可能含有K+、Fe3+、Al3+、Cl-、SO42-、CO32-中的若干种,现进行以下实验:
①取少量固体,加入稀硝酸搅拌,固体全部溶解,没有气体放出;
②向①溶液中加入一定量Ba(OH)2溶液,生成有色沉淀,过滤后滤液中 滴入硝酸酸化的AgNO3溶液,有白色沉淀生成;
③取②中有色沉淀加入足量稀盐酸后,沉淀全部溶解;
④重新取少量固体加入适量蒸馏水搅拌后,固体全部溶解,得到澄清溶液;
⑤向④的溶液中加入氨水使溶液呈碱性,有沉淀生成,过滤,往得到沉淀中加入过量的NaOH溶液,沉淀减少。
(1)根据上述实验,判断粉末中一定含有的离子是_______ , 肯定没有的离子是_____ 不能确定是否含有的离子是___________ ,通过_________ 来进一步确定该离子。
(2)写出②中生成有色沉淀反应的离子方程式:______________________ 。
①取少量固体,加入稀硝酸搅拌,固体全部溶解,没有气体放出;
②向①溶液中加入一定量Ba(OH)2溶液,生成有色沉淀,过滤后滤液中 滴入硝酸酸化的AgNO3溶液,有白色沉淀生成;
③取②中有色沉淀加入足量稀盐酸后,沉淀全部溶解;
④重新取少量固体加入适量蒸馏水搅拌后,固体全部溶解,得到澄清溶液;
⑤向④的溶液中加入氨水使溶液呈碱性,有沉淀生成,过滤,往得到沉淀中加入过量的NaOH溶液,沉淀减少。
(1)根据上述实验,判断粉末中一定含有的离子是
(2)写出②中生成有色沉淀反应的离子方程式:
您最近一年使用:0次
【推荐1】废旧太阳能电池CIGS具有较高的回收利用价值,其主要组成为 。某探究小组回收处理流程如图:
。某探究小组回收处理流程如图:
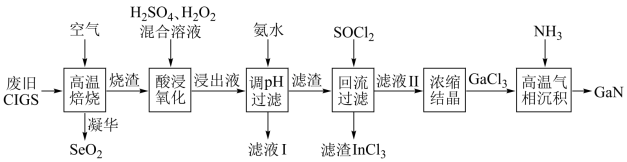
回答下列问题:
(1)硒(Se)与硫为同族元素,Se的最外层电子数为_______ ;在化合物 中镓(Ga)和铟(In)均为+3价,则Cu的化合价为
中镓(Ga)和铟(In)均为+3价,则Cu的化合价为_______ 。
(2)“酸浸氧化”得蓝色溶液,则该过程发生的主要氧化还原反应的化学方程式为_______ 。
(3)氢氧化铜沉淀可溶于氨水,则滤液I中的阴离子主要有_______ 和_______ 两种。
(4)滤渣加入 混合前需要洗涤、干燥,并用试剂
混合前需要洗涤、干燥,并用试剂_______ 和_______ 来检验滤渣中的 是否洗净。
是否洗净。
(5)滤渣加入 可反生反应:
可反生反应: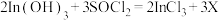 ;对物质X的性质有如下判断,你认为不正确的是 。
;对物质X的性质有如下判断,你认为不正确的是 。
(6)“高温气相沉积”过程中发生的化学反应方程式为_______ 。
 。某探究小组回收处理流程如图:
。某探究小组回收处理流程如图:
回答下列问题:
(1)硒(Se)与硫为同族元素,Se的最外层电子数为
 中镓(Ga)和铟(In)均为+3价,则Cu的化合价为
中镓(Ga)和铟(In)均为+3价,则Cu的化合价为(2)“酸浸氧化”得蓝色溶液,则该过程发生的主要氧化还原反应的化学方程式为
(3)氢氧化铜沉淀可溶于氨水,则滤液I中的阴离子主要有
(4)滤渣加入
 混合前需要洗涤、干燥,并用试剂
混合前需要洗涤、干燥,并用试剂 是否洗净。
是否洗净。(5)滤渣加入
 可反生反应:
可反生反应: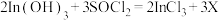 ;对物质X的性质有如下判断,你认为不正确的是 。
;对物质X的性质有如下判断,你认为不正确的是 。| A.有弱酸性 | B.可使溴水褪色 |
C.与 溶液反应得白色沉淀 溶液反应得白色沉淀 | D.与烧碱溶液反应可生成两种盐 |
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】某混合物的水溶液,可能含有以下离子中的若干种:K+、Al3+、Fe3+、Mg2+、Ba2+、NH4+、Cl-、CO32-、SO42-,现分别取100 mL的两等份溶液进行如下实验:
①第一份加过量NaOH溶液后加热,收集到0.02 mol气体,无沉淀生成,同时得到溶液甲。
②向甲溶液中通入过量CO2,生成白色沉淀,沉淀经过滤、洗涤、干燥、灼烧后,得到1.02 g固体。
③第二份加足量BaCl2溶液后,生成白色沉淀,沉淀经足量盐酸洗涤、干燥后,得到11.65 g固体。
依据实验回答下列问题:
(1)由①可知一定存在的离子为_______ ,其浓度为_______ mol·L-1。
(2)写出②中产生沉淀的离子方程式_______ 。
(3)由③可知一定存在的离子为_______ ,其浓度为_______ mol·L-1。
(4)综合上面三个实验,该混合物的水溶液中一定不存在的离子是_______ (填离子符号)。
(5)某同学通过分析认为该溶液中一定存在K+,他的理由是_______ 。
①第一份加过量NaOH溶液后加热,收集到0.02 mol气体,无沉淀生成,同时得到溶液甲。
②向甲溶液中通入过量CO2,生成白色沉淀,沉淀经过滤、洗涤、干燥、灼烧后,得到1.02 g固体。
③第二份加足量BaCl2溶液后,生成白色沉淀,沉淀经足量盐酸洗涤、干燥后,得到11.65 g固体。
依据实验回答下列问题:
(1)由①可知一定存在的离子为
(2)写出②中产生沉淀的离子方程式
(3)由③可知一定存在的离子为
(4)综合上面三个实验,该混合物的水溶液中一定不存在的离子是
(5)某同学通过分析认为该溶液中一定存在K+,他的理由是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】Ⅰ.下表有三组物质,每组均有甲、乙、丙三种物质(酸、碱、盐均为溶液)。
根据该表回答问题:
(1)第Ⅱ组物质中与第Ⅰ组任何物质都不发生反应的是___________ 。
(2)第Ⅱ组物质中与第Ⅲ组任何物质都能发生反应的是___________ 。
(3)第Ⅲ组中与其他两种物质不同类的是___________ 。
(4)第Ⅲ组中有一种物质能与第___________ 组中的所有物质反应,这种物质是___________ 。
Ⅱ.某无色溶液中可能含Mg2+、Cu2+、Ba2+、CO 、Cl−、
、Cl−、 、NO
、NO 中的几种,现进行如下实验:
中的几种,现进行如下实验:
①取适量溶液,加入足量NaOH溶液,生成白色沉淀。
②过滤,向实验Ⅰ所得的滤液中加入足量 溶液,有白色沉淀生成。根据上述实验回答下列问题。
溶液,有白色沉淀生成。根据上述实验回答下列问题。
(5)溶液中一定不存在的离子是___________ ;
(6)写出①和②中所发生反应的离子方程式___________ 、___________ ;
(7)为了验证溶液中是否存在Cl−、NO ,某同学提出下列假设:
,某同学提出下列假设:
①只存在Cl−;②Cl−、NO 同时存在;③
同时存在;③___________
已知实验提供的试剂只有稀盐酸, 溶液、稀硝酸、NaOH溶液和蒸馏水。
溶液、稀硝酸、NaOH溶液和蒸馏水。
实验方法:___________
实验现象:___________
实验结论:假设③正确。
| 第I组 | 第Ⅱ组 | 第Ⅲ组 | |
| 甲 | BaCl2 | HCl | Cu(NO3)2 |
| 乙 | Fe2O3 | K2SO4 | H2SO4 |
| 丙 | Mg | NaOH | MgCl2 |
(1)第Ⅱ组物质中与第Ⅰ组任何物质都不发生反应的是
(2)第Ⅱ组物质中与第Ⅲ组任何物质都能发生反应的是
(3)第Ⅲ组中与其他两种物质不同类的是
(4)第Ⅲ组中有一种物质能与第
Ⅱ.某无色溶液中可能含Mg2+、Cu2+、Ba2+、CO
 、Cl−、
、Cl−、 、NO
、NO 中的几种,现进行如下实验:
中的几种,现进行如下实验:①取适量溶液,加入足量NaOH溶液,生成白色沉淀。
②过滤,向实验Ⅰ所得的滤液中加入足量
 溶液,有白色沉淀生成。根据上述实验回答下列问题。
溶液,有白色沉淀生成。根据上述实验回答下列问题。(5)溶液中一定不存在的离子是
(6)写出①和②中所发生反应的离子方程式
(7)为了验证溶液中是否存在Cl−、NO
 ,某同学提出下列假设:
,某同学提出下列假设:①只存在Cl−;②Cl−、NO
 同时存在;③
同时存在;③已知实验提供的试剂只有稀盐酸,
 溶液、稀硝酸、NaOH溶液和蒸馏水。
溶液、稀硝酸、NaOH溶液和蒸馏水。实验方法:
实验现象:
实验结论:假设③正确。
您最近一年使用:0次



