按要求完成下列各题:
(1)画出Li2O的电子式________________________
(2)用电子式表示CO2分子的形成过程_________________________________________
(3)画出N2分子的结构式_________________
(4)写出全部是由H、O、S、K四种元素形成的两种盐相互反应的离子方程式__________
(5)第3周期的两种金属氧化物对应的水化物间能相互发生反应,写出其化学反应方程式_____________
(6)如图是元素周期表的一个方格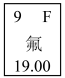 ,其中19.00的意义是
,其中19.00的意义是___________
(1)画出Li2O的电子式
(2)用电子式表示CO2分子的形成过程
(3)画出N2分子的结构式
(4)写出全部是由H、O、S、K四种元素形成的两种盐相互反应的离子方程式
(5)第3周期的两种金属氧化物对应的水化物间能相互发生反应,写出其化学反应方程式
(6)如图是元素周期表的一个方格
 ,其中19.00的意义是
,其中19.00的意义是
更新时间:2019-04-04 08:46:02
|
相似题推荐
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】写出下列物质的电子式:
(1)Cl2_______
(2)N2_______
(3)H2O_______
(4)NaOH_______
(5)CO2_______
(1)Cl2
(2)N2
(3)H2O
(4)NaOH
(5)CO2
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】按要求完成下列填空:
(1)①写出乙醛的结构简式:_______ ;
②写出过氧化氢的电子式:_______ 。
(2)写出过量铁与稀硝酸反应的离子方程式:_______ 。
(3)蔗糖遇浓硫酸变黑,体现了浓硫酸的_______ 性。
(4)写出 与少量氢氧化钠溶液反应的离子方程式:
与少量氢氧化钠溶液反应的离子方程式:_______ 。 气体通入
气体通入 溶液中无明显现象,然后再通入下列气体有沉淀生成,则该气体不可能是
溶液中无明显现象,然后再通入下列气体有沉淀生成,则该气体不可能是_______ (填标号)。
①H2S ②Cl2 ③NH3 ④CO2 ⑤HCl
(1)①写出乙醛的结构简式:
②写出过氧化氢的电子式:
(2)写出过量铁与稀硝酸反应的离子方程式:
(3)蔗糖遇浓硫酸变黑,体现了浓硫酸的
(4)写出
 与少量氢氧化钠溶液反应的离子方程式:
与少量氢氧化钠溶液反应的离子方程式: 气体通入
气体通入 溶液中无明显现象,然后再通入下列气体有沉淀生成,则该气体不可能是
溶液中无明显现象,然后再通入下列气体有沉淀生成,则该气体不可能是①H2S ②Cl2 ③NH3 ④CO2 ⑤HCl
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】如图是元素周期表的一部分,请回答下列问题:
(1)在这些元素中,单质的化学性质最不活泼的 是______________ (填元素符号)。
(2)③的气态氢化物的电子式______________ ,②④形成的可溶于水的气态化合物的结构式______________ 。
(3)这些元素形成的最高价氧化物的水化物中,碱性最强的化合物为______________ (填物质的化学式),酸性最强的含氧酸为______________ (填物质的化学式)。
| IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0族 | |
| 1 | ① | |||||||
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ |
(1)在这些元素中,单质的化学性质
(2)③的气态氢化物的电子式
(3)这些元素形成的最高价氧化物的水化物中,碱性最强的化合物为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】某微粒的结构示意图为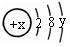 试回答:
试回答:
(1)当x-y=10时,该粒子为_____ (选填“原子”或“阳离子”、“阴离子”);
(2)当y=8时,该粒子可能是(用化学式表示,任填3种)_______ 、_______ 、_______ ;
(3)请写出工业上制取y=7元素对应单质时的离子方程式:_____________ 。
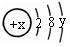 试回答:
试回答:(1)当x-y=10时,该粒子为
(2)当y=8时,该粒子可能是(用化学式表示,任填3种)
(3)请写出工业上制取y=7元素对应单质时的离子方程式:
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】下表为元素周期表中的一部分。
用化学式或元素符号回答下列问题:
(1)①③⑤中,最高价氧化物的水化物,碱性最强的是___ 。
(2)①和⑨的最高价氧化物对应水化物的化学式为___ 和___ 。①和⑨两元素形成化合物的化学式为___ ,该化合物的溶液与元素⑧的单质反应的离子方程式为___ 。
(3)⑧⑨⑪三种元素形成的气态氢化物最稳定的是__ ,三者非金属性的强弱顺序为__ 。
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 二 | ⑥ | ⑦ | ⑪ | |||||
| 三 | ① | ③ | ⑤ | ⑧ | ⑩ | |||
| 四 | ② | ④ | ⑨ |
用化学式或元素符号回答下列问题:
(1)①③⑤中,最高价氧化物的水化物,碱性最强的是
(2)①和⑨的最高价氧化物对应水化物的化学式为
(3)⑧⑨⑪三种元素形成的气态氢化物最稳定的是
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】元素M、T、U、V、N 在元素周期表中的相对位置如图所示,其中M单质在冷暗处与H2剧烈化合并爆炸。回答下列问题:
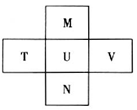
(1)元素T的原子序数为______ ,元素U的简单离子结构示意图为_________ 。
(2)V元素形成的单质中______ (填“存在”或“不存在”)化学键。
(3)M、N两元素分别与氢形成的气态氢化物是甲和乙,其中甲的电子式为______ ,甲和乙的稳定性强弱顺序为______ (用化学式表示,下同),其水溶液的酸性强弱顺序为______ 。
(4)写出元素U的单质置换出元素T的单质的离子方程式:____________ 。

(1)元素T的原子序数为
(2)V元素形成的单质中
(3)M、N两元素分别与氢形成的气态氢化物是甲和乙,其中甲的电子式为
(4)写出元素U的单质置换出元素T的单质的离子方程式:
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】下表是元素周期律的一部分用元素符号或化学式、化学用语填空。
(1)在写出元素⑦的气态氢化物的电子式___ ;元素⑨的核外电子排布式为___ ;
(2)元素③的原子核外有___ 种能量不同的电子,有___ 种运动状态电子。
(3)元素⑧与⑥形成的晶体是___ 晶体:元素⑤和⑩形成的分子属于___ 分子(极性、非极性):
(4)写出元素②与④的最高价氧化物对应水化物之间反应的方程式___ ;
(5)元素⑨和⑩的非金属性比较更强___ (元素符号),用一个方程式说明这一结论___ 。
(6)关于氟、钠、镁、氯四种元素的性质递变规律,描述正确的是___ (写编号)。
a.原子半径:Na<Cl b.离子半径:F-<Mg2+
c.热稳定性:HF>HCl d.碱性:NaOH>Mg(OH)2
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ① | ⑤ | ⑦ | ⑧ | ||||
| 3 | ② | ③ | ④ | ⑥ | ⑨ | ⑩ |
(1)在写出元素⑦的气态氢化物的电子式
(2)元素③的原子核外有
(3)元素⑧与⑥形成的晶体是
(4)写出元素②与④的最高价氧化物对应水化物之间反应的方程式
(5)元素⑨和⑩的非金属性比较更强
(6)关于氟、钠、镁、氯四种元素的性质递变规律,描述正确的是
a.原子半径:Na<Cl b.离子半径:F-<Mg2+
c.热稳定性:HF>HCl d.碱性:NaOH>Mg(OH)2
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】2019年是元素周期表发表150周年,期间科学家为完善周期表做出了不懈努力。中国科学院院士张青莲教授曾主持测定了铟(49In)等9种元素相对原子质量的新值,被采用为国际新标准。
(1)In在周期表中的位置是___ 。
(2)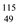 In的中子数与电子数的差值为
In的中子数与电子数的差值为___ 。
(1)In在周期表中的位置是
(2)
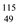 In的中子数与电子数的差值为
In的中子数与电子数的差值为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】联合国将2019年定为“国际化学元素周期表年”,以纪念门捷列夫发现元素周期律150周年。元素周期律把元素及其化合物纳入一个统一的理论体系,为系统研究元素及其化合物提供了科学方法,为发现和探索新元素、新物质提供了有效思路。
1. 为纪念门捷列夫,科学家将1955年人工合成的一种新元素用符号“Md”表示,中文命名为“钔”。核素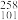 Md的质量数为
Md的质量数为( )
A. 101 B. 157 C. 258 D. 359
2. Mg和Si都属于元素周期表第3周期元素,它们原子结构中相同的是( )
A. 质子数 B. 电子层数 C. 核外电子数 D. 最外层电子数
3. 判断Cl的非金属性比S的强,可依据的事实是( )
A. HCl的热稳定性比H2S的强 B. 氯气能溶于水,硫难溶于水
C. 常温下,氯单质呈气态,硫单质呈固态 D. AgCl是白色固体,Ag2S是黑色固体
4. 锂是第2周期ⅠA族元素,下列有关锂元素性质推测正确的是( )
A. 最高化合价为+2 B. 原子半径比钠的大
C. 单质与水的反应比钠更剧烈 D. 最高价氧化物对应的水化物碱性比钠的弱
1. 为纪念门捷列夫,科学家将1955年人工合成的一种新元素用符号“Md”表示,中文命名为“钔”。核素
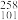 Md的质量数为
Md的质量数为A. 101 B. 157 C. 258 D. 359
2. Mg和Si都属于元素周期表第3周期元素,它们原子结构中相同的是
A. 质子数 B. 电子层数 C. 核外电子数 D. 最外层电子数
3. 判断Cl的非金属性比S的强,可依据的事实是
A. HCl的热稳定性比H2S的强 B. 氯气能溶于水,硫难溶于水
C. 常温下,氯单质呈气态,硫单质呈固态 D. AgCl是白色固体,Ag2S是黑色固体
4. 锂是第2周期ⅠA族元素,下列有关锂元素性质推测正确的是
A. 最高化合价为+2 B. 原子半径比钠的大
C. 单质与水的反应比钠更剧烈 D. 最高价氧化物对应的水化物碱性比钠的弱
您最近一年使用:0次



