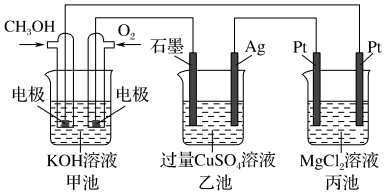
以LiPF6和SO(CH3)2为电解质的高能锂电池的总反应式为2Li+FeS=Fe+LiS,用该电池为电源进行如图的电解实验,电解一段时间测得甲电池产生标准状况下H24.48L。下列有关叙述正确的是


| A.Y电极为高能锂电池的负极从隔膜中通过的离子数目为0.4NA |
| B.电解池中换成阴离子交换膜,总反应不发生变化 |
| C.若电解过程体积变化忽略不计,则电解后甲池中溶液浓度为4mol/L |
| D.电源正极反应式为:FeS+2Li++2e-=Fe+Li2S |
更新时间:2019-04-05 19:49:36
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】随着现代工农业的发展,水体内氮的含量超标会引发水华现象。科学家探索使用电化学原理,用铁和石墨作电极进行污水除氮,其工作原理如图所示。下列说法正确的是
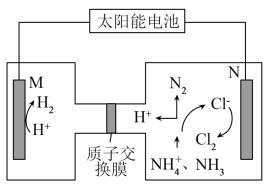

| A.M极材料为铁,连接太阳能电池的正极 |
B.氨气在阳极上的电极反应式为 |
C.制得1mol ,理论上溶液中迁移了6mol电子 ,理论上溶液中迁移了6mol电子 |
| D.电解一段时间后,阳极室的酸性增强 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】工业上常用三种方法制氢:
(1)绿氢。电解水制氢气。(添加NaOH溶液或稀硫酸增强导电性)
(2)蓝氢。利用天然气在高温下与水蒸气反应: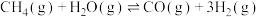 。
。
(3)灰氢。利用焦炭在高温下与水蒸气反应: 。
。
设 为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是
(1)绿氢。电解水制氢气。(添加NaOH溶液或稀硫酸增强导电性)
(2)蓝氢。利用天然气在高温下与水蒸气反应:
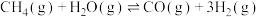 。
。(3)灰氢。利用焦炭在高温下与水蒸气反应:
 。
。设
 为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是A.制绿氢时,当阳极产生amol气体时,转移的电子数为2a |
B.制备蓝氢时,16g 与足量水蒸气反应可制备 与足量水蒸气反应可制备 的分子数为3 的分子数为3 |
C.标准状况下,制备44.8L灰氢时断裂的极性键数目为 |
D.制备1mol 时,三种制氢方法中,转移的电子数均为2 时,三种制氢方法中,转移的电子数均为2 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】电化学原理在生产生活中广泛存在,下列说法正确的是
| A.钢铁发生析氢腐蚀或吸氧腐蚀时,负极都是铁失去电子变成Fe2+ |
| B.铁表面的镀锌层破损后,就完全失去了对铁的保护作用 |
| C.将地下金属管道连接直流电源的负极,属于牺牲阳极法 |
| D.电解精炼铜时,电解质溶液中铜离子浓度基本保持不变 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】中学阶段介绍的应用电解法制备物质主要有三种:一是铝的工业制备、二是氯碱工业、三是金属钠的制备。下列关于这三个工业生产的描述中正确的是
| A.电解法制金属钠时,正极反应式:Na++e-=Na |
| B.电解法生产铝时,需对铝土矿进行提纯,在提纯过程中应用了氧化铝或氢氧化铝的两性 |
| C.在氯碱工业中,电解池中的阴极产生的是H2,NaOH 在阳极附近产生 |
| D.氯碱工业和金属钠的冶炼都用到了NaCl,在电解时它们的阴极都是Cl-失电子 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】基于甲烷蒸汽重整工业制氢面临着大量的“碳排放”,我国科技工作者发明了一种电化学分解甲烷的方法,从而实现了碳和水的零排放方式生产氢气。电化学反应机理如下图所示下列说法错误的是


A.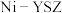 电极为阳极, 电极为阳极, 电极为阴极 电极为阴极 |
B.阳极的电极反应式为 |
C.电解的总反应为 |
| D.上述电化学装置中的电解质溶液可换为水 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】如图(Ⅰ)为全钒电池,电池工作原理为:2H++VO2++V2+ VO2++V3++H2O。装置(Ⅱ)中的电解液是硝酸、硫酸的混合水溶液,当闭合开关K时,铂电极上生成NH2OH。则下列说法正确的是
VO2++V3++H2O。装置(Ⅱ)中的电解液是硝酸、硫酸的混合水溶液,当闭合开关K时,铂电极上生成NH2OH。则下列说法正确的是

 VO2++V3++H2O。装置(Ⅱ)中的电解液是硝酸、硫酸的混合水溶液,当闭合开关K时,铂电极上生成NH2OH。则下列说法正确的是
VO2++V3++H2O。装置(Ⅱ)中的电解液是硝酸、硫酸的混合水溶液,当闭合开关K时,铂电极上生成NH2OH。则下列说法正确的是
| A.闭合K时,全钒电池负极区pH基本不变 |
| B.闭合K时,铂电极的电极反应式为:NO3ˉ+6eˉ+5H2O=NH2OH +7OHˉ |
| C.全钒电池充电时,电极B上发生还原反应 |
| D.全钒电池放电时,电极B上发生的反应为:VO2++2H++e-=VO2++H2O |
您最近一年使用:0次



 +8H+
+8H+

