已知某主族元素R的原子序数为35,依据元素周期律对该元素的性质进行预测。对下列性质的预测,你认为错误的是
| A.原子核外有4个电子层 | B.原子最外层有7个电子 |
| C.该元素是非金属元素 | D.最高价氧化物既可以与盐酸反应又可以与NaOH溶液反应 |
更新时间:2019/04/09 08:50:06
|
相似题推荐
单选题
|
较易
(0.85)
【推荐1】图为周期表的一部分,已知A,B,C,D,E五种元素原子核外共有85个电子,E原子核外有四个电子层,B元素是( )
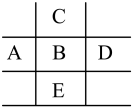

| A.P | B.Mg | C.Cl | D.S |
您最近半年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐2】铊(thallium,Tl) 相对原子质量为204,广泛用于电子、军工、航天、化工、冶金、通讯、医学等领域。但铊盐有剧毒。1992年清华大学铊中毒案、2013年复旦大学研究生投毒案令其家喻户晓。已知铊元素中质子数比中子数少42,下列关于铊的说法中错误的是
| A.原子序数为81 | B.位于第六周期ⅢA族 |
| C.质量数约为204 | D.中子数为81 |
您最近半年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐1】W、X、Y、Z、M、N六种主族元素,它们在周期表中位置如图所示,下列说法不正确 的是
| W | ||||||||||
| X | Y | Z | M | |||||||
…… | N | |||||||||
A.原子半径: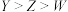 |
B.单质的还原性: |
| C.溴与元素M同主族,最高价氧化物的水化物的酸性比M的弱 |
| D.W的气态氢化物热稳定性比Z的气态氢化物热稳定性好,是因为W的氢化物分子间有氢键 |
您最近半年使用:0次
单选题
|
较易
(0.85)
【推荐2】已知元素铝(A1)的原子序数为13,下列叙述正确的是( )
| A.元素的最高化合价为+3 |
| B.元素是第四周期的主族元素 |
| C.原子的第3电子层含有18个电子 |
| D.铝的氧化物的水溶液呈强碱性 |
您最近半年使用:0次

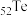 )元素和钛(
)元素和钛(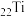 )元素都是过渡元素
)元素都是过渡元素 、
、 、
、 三种元素的原子核外电子总数等于
三种元素的原子核外电子总数等于

