(1)NaOH的摩尔质量是__________________ 。将4gNaOH溶于水配制成100mL溶液,所得溶液中NaOH的物质的量浓度是____________________ 。取出10mL上述溶液加水稀释到100mL,稀释后溶液中NaOH的物质的量浓度是________________ 。
(2)根据交叉分类法,请用直线将下面的酸与酸的分类连接起来
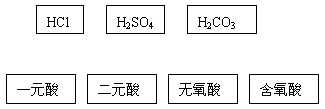
还可以补充的酸的分类标准有(只填一种):________________________________ ,从而将酸分成__________________________________________ 。
(2)根据交叉分类法,请用直线将下面的酸与酸的分类连接起来

还可以补充的酸的分类标准有(只填一种):
11-12高一上·吉林·期中 查看更多[1]
(已下线)2011-2012学年吉林省吉林市普通中学高一上学期期中考试化学试卷
更新时间:2016-12-09 02:15:21
|
相似题推荐
填空题
|
较易
(0.85)
解题方法
【推荐1】按要求完成下列各题
(1)按照物质的树状分类和交叉分类,HNO3应属于_____ (填字母代号)。
①酸 ②氢化物 ③氧化物 ④含氧酸 ⑤难挥发性酸 ⑥化合物 ⑦一元酸
A. ①②③④⑤⑥⑦ B. ①④⑥⑦ C. ①③⑤⑥ D. ①④⑤⑥⑦
(2)现有以下物质:①NaCl晶体、 ②液态HCl、 ③CaCO3固体、 ④熔融KCl、⑤蔗糖、 ⑥铜、 ⑦CO2、 ⑧H2SO4。
其中:属于电解质的是____ ,属于非电解质的是____ 。
(3)Fe(OH)3胶体呈红褐色,插入两个惰性电极,通直流电一段时间,阴极附近的颜色逐渐变深,这种现象叫_____ ;光束通过Fe(OH)3胶体,可看到明亮的通路,这种现象叫_____ ;向Fe(OH)3胶体中逐滴加入稀盐酸,刚开始有红褐色沉淀生成,这是因为____ ,然后红褐色沉淀又逐渐溶解,原因是___ (用离子方程式解释)。
(1)按照物质的树状分类和交叉分类,HNO3应属于
①酸 ②氢化物 ③氧化物 ④含氧酸 ⑤难挥发性酸 ⑥化合物 ⑦一元酸
A. ①②③④⑤⑥⑦ B. ①④⑥⑦ C. ①③⑤⑥ D. ①④⑤⑥⑦
(2)现有以下物质:①NaCl晶体、 ②液态HCl、 ③CaCO3固体、 ④熔融KCl、⑤蔗糖、 ⑥铜、 ⑦CO2、 ⑧H2SO4。
其中:属于电解质的是
(3)Fe(OH)3胶体呈红褐色,插入两个惰性电极,通直流电一段时间,阴极附近的颜色逐渐变深,这种现象叫
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】下列状态下的物质:①NaCl固体②NaOH溶液③BaSO4④酒精⑤铁或石墨⑥液态HCl。回答下列问题(填序号)
(1)属于能导电的有____________________ ,
(2)属于电解质的有____________________ ,
(3)属于非电解质的有__________________ ,
(4)属于既不是电解质也不是非电解质的有_________________ 。
(5)人们常根据物质的组成、结构、性质或用途等进行分类。
①Al2(SO4)3既属于铝盐,又属于硫酸盐,这是_________________ 分类方法。
②根据分类的方法可以预测物质的性质及可能发生的变化。SiO2是普通玻璃的主要成分,与CO2一样是酸性氧化物,写出SiO2溶于NaOH溶液的化学方程式:__________________ 。
(1)属于能导电的有
(2)属于电解质的有
(3)属于非电解质的有
(4)属于既不是电解质也不是非电解质的有
(5)人们常根据物质的组成、结构、性质或用途等进行分类。
①Al2(SO4)3既属于铝盐,又属于硫酸盐,这是
②根据分类的方法可以预测物质的性质及可能发生的变化。SiO2是普通玻璃的主要成分,与CO2一样是酸性氧化物,写出SiO2溶于NaOH溶液的化学方程式:
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】实验室药品橱柜中摆列着如下试剂和药品:①稀盐酸,②氢氧化钠固体,③氢氧化钠溶液,④铜,⑤氯化钠固体,⑥硝酸银溶液,⑦酒精,⑧碳酸钠固体,⑨碳酸钾固体。回答下面问题:
(1)氯化钠、碳酸钠与碳酸钾有如下关系:

该分类属于_______ (填“树状分类法”或“交叉分类法”)。属于图Ⅱ部分的是_______ (填“氯化钠”“碳酸钠”或“碳酸钾”)。
(2)上述9种试剂或药品中属于电解质的是_______ (填序号,下同),属于非电解质的是_______ ,能导电但既不属于电解质也不属于非电解质的是_______ 。
(3)写出试剂③中NaOH在水溶液中的电离方程式_______ 。写出试剂⑨中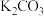 在水溶液中的电离方程式
在水溶液中的电离方程式_______ 。
(4)称取53g试剂⑧ 固体,含有
固体,含有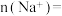
_______ mol,与足量试剂①稀盐酸反应,消耗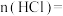
_______ mol,反应的化学方程式是_______ 。
(1)氯化钠、碳酸钠与碳酸钾有如下关系:

该分类属于
(2)上述9种试剂或药品中属于电解质的是
(3)写出试剂③中NaOH在水溶液中的电离方程式
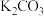 在水溶液中的电离方程式
在水溶液中的电离方程式(4)称取53g试剂⑧
 固体,含有
固体,含有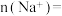
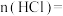
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】补充完整下列化学计算公式:
(1)N=________ NA , N表示 ________ ;NA表示 ________ .
(2)________ =n M,n表示_________ m表示 ________ .
(3)V=________ Vm,V表示 ________ ;Vm表示 ________
(4)________ =c V,c表示 ________ ;V的单位为 ________
(1)N=
(2)
(3)V=
(4)
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】CO和CO2的混合气体18g,完全燃烧后测得CO2体积为11.2L(STP),则混合气体的平均摩尔质量是_______ 。
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】铁是人体必需的微量元素,黑木耳等食品中富含铁元素。下图是某学习小组同学检验黑木耳中的铁元素并测定其含量的实验流程图。
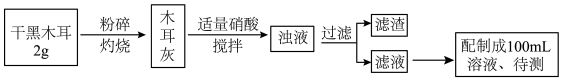
(一)定性检验
(1)粉碎后的黑木耳应置于___________ (填仪器名称)中灼烧。取3滴待测液滴在点滴板上,加几滴___________ (填化学式)溶液,若出现___________ 的现象,则此溶液中存在Fe3+。
(2)下列过滤操作中不规范的有___________(填字母序号)。
(二)定量测定
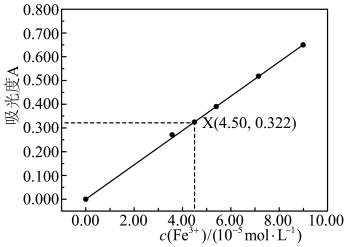
(3)已知溶液的吸光度A与溶液中c(Fe3+)关系如下图。该小组从上述100mL溶液中取出10mL待测液,测得待测液吸光度位于图中X点,试计算该黑木耳中铁元素的含量(mg/100g)___________ 。(要求有计算过程)

(一)定性检验
(1)粉碎后的黑木耳应置于
(2)下列过滤操作中不规范的有___________(填字母序号)。
| A.玻璃棒用作引流 |
| B.用玻璃棒在漏斗中轻轻搅动以加快过滤速度 |
| C.将滤纸湿润,使其紧贴漏斗壁 |
| D.漏斗末端颈尖未紧靠烧杯内壁 |
(二)定量测定
(3)已知溶液的吸光度A与溶液中c(Fe3+)关系如下图。该小组从上述100mL溶液中取出10mL待测液,测得待测液吸光度位于图中X点,试计算该黑木耳中铁元素的含量(mg/100g)

您最近一年使用:0次
填空题
|
较易
(0.85)
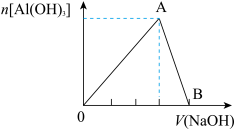
【推荐2】向20mL含有1mol/L的氯化铝溶液中逐滴加入浓度为1mol/L的氢氧化钠溶液,产生沉淀的物质的量与所加碱的体积如图所示:
(1)写出OA段和AB段发生反应的离子方程式:OA段_____ ;AB段_____ 。
(2)A点溶液中的溶质为:____ 。(填化学式)
(3)若产生0.78g白色沉淀,则加入的氢氧化钠溶液的体积可能是____ mL或____ mL。
(4)B点表示的氢氧化钠溶液的体积是___ mL。
(1)写出OA段和AB段发生反应的离子方程式:OA段
(2)A点溶液中的溶质为:
(3)若产生0.78g白色沉淀,则加入的氢氧化钠溶液的体积可能是
(4)B点表示的氢氧化钠溶液的体积是
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】在花瓶中加入“鲜花保鲜剂”可延长鲜花的寿命。如表是1L“鲜花保鲜剂”的成分(其中阿司匹林不含K+,其存在也不会干扰成分中其他离子的检验)。
(1)问题一:“鲜花保鲜剂”中物质的量浓度最大的成分是什么___ ?其物质的量浓度为多少___ ?
(2)问题二:“鲜花保鲜剂”中SO 、MnO
、MnO 、K+的物质的量浓度分别为多少
、K+的物质的量浓度分别为多少___ 、___ 、___ ?写出计算式。
| 成分 | 蔗糖 | 硫酸钾 | 阿司匹林 | 高锰酸钾 |
| 质量/g | 50.00 | 0.50 | 0.35 | 0.50 |
| 摩尔质量/(g·mol-1) | 342 | 174 | 180 | 158 |
(1)问题一:“鲜花保鲜剂”中物质的量浓度最大的成分是什么
(2)问题二:“鲜花保鲜剂”中SO
 、MnO
、MnO 、K+的物质的量浓度分别为多少
、K+的物质的量浓度分别为多少
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】物质的量是联系宏观的和微观的桥梁。
(1)标准状况下,与5.6L的CH4气体含相同H原子数的H2S的质量为____ g。
(2)将0.2mol·L-1Al2(SO4)3和0.2mol·L-1H2SO4溶液等体积混合(设混合溶液体积等于两溶液体积之和),计算混合液中c (SO )=
)=____ mol·L-1。若用容量瓶以质量分数为98%、密度为1.84g·cm-3的浓硫酸,配制500mL浓度成0.2mol·L-1稀硫酸,计算需要量取____ mL的浓硫酸。
(3)某无土栽培用的营养液,要求KCl、K2SO4和NH4Cl三种固体原料的物质的量之比为1︰4︰8。
①配制该营养液后c(NH )=0.016mol·L-1,溶液中c(K+)=
)=0.016mol·L-1,溶液中c(K+)=____ 。
②若采用(NH4)2SO4和KCl来配制该营养液,则(NH4)2SO4和KCl物质的量之比为____ 。
(1)标准状况下,与5.6L的CH4气体含相同H原子数的H2S的质量为
(2)将0.2mol·L-1Al2(SO4)3和0.2mol·L-1H2SO4溶液等体积混合(设混合溶液体积等于两溶液体积之和),计算混合液中c (SO
 )=
)=(3)某无土栽培用的营养液,要求KCl、K2SO4和NH4Cl三种固体原料的物质的量之比为1︰4︰8。
①配制该营养液后c(NH
 )=0.016mol·L-1,溶液中c(K+)=
)=0.016mol·L-1,溶液中c(K+)=②若采用(NH4)2SO4和KCl来配制该营养液,则(NH4)2SO4和KCl物质的量之比为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】如图为实验室某浓盐酸试剂瓶标签上的有关数据,根据有关数据回答下列问题:
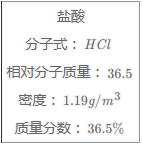
(1)该浓盐酸中HCl的物质的量浓度为________ mol/L。
(2)取用任意体积的该盐酸溶液时,下列物理量不随所取体积多少而变化的是_______ 。
A.溶液中HCl的质量
B.溶液的pH
C.溶液中H+的数目
D.溶液的密度
(3)欲用上述浓盐酸配制500mL 2mol/L的稀盐酸,需要_____ mL上述盐酸 (保留1位小数)
(4)现有1 L1mol/L的稀盐酸,欲使其浓度增大1倍。采取的措施合理的是________________ 。
A、通入标况下HCl气体22.4L
B、将溶液加热浓缩至0. 5L
C、加入5mol/L的盐酸0.6L.再稀释至2L.
D、加入1L 3mol/L的盐酸混合均匀

(1)该浓盐酸中HCl的物质的量浓度为
(2)取用任意体积的该盐酸溶液时,下列物理量不随所取体积多少而变化的是
A.溶液中HCl的质量
B.溶液的pH
C.溶液中H+的数目
D.溶液的密度
(3)欲用上述浓盐酸配制500mL 2mol/L的稀盐酸,需要
(4)现有1 L1mol/L的稀盐酸,欲使其浓度增大1倍。采取的措施合理的是
A、通入标况下HCl气体22.4L
B、将溶液加热浓缩至0. 5L
C、加入5mol/L的盐酸0.6L.再稀释至2L.
D、加入1L 3mol/L的盐酸混合均匀
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】填空。
(1)工业上用_______ 和_______ 作为原料来制取漂白粉,反应的化学方程式为_______ 。漂白粉的有效成分是_______ ,漂白粉溶于水后,滴加少量盐酸可加快漂白和杀菌的速度,此过程中发生反应的化学方程式_______ 。
(2)从200 mL、5 mol/L Na2CO3溶液中取出20 mL溶液,其溶质的物质的量是_______ 。将取出的溶液稀释至100 mL,其Na+的物质的量浓度是_______ 。
(3)有K2SO4和Al2(SO4)3的混合溶液,已知其中Al3+的物质的量浓度为0.2 mol/L, 的物质的量浓度为0.5 mol/L,则此溶液中K+的物质的量浓度为
的物质的量浓度为0.5 mol/L,则此溶液中K+的物质的量浓度为_______ 。
(4)在标准状况下,CO和CO2的混合气体共11.2 L,质量为18.8 g,其中含有_______ 个CO分子,该混合气体中CO与CO2的密度之比为_______ 。
(1)工业上用
(2)从200 mL、5 mol/L Na2CO3溶液中取出20 mL溶液,其溶质的物质的量是
(3)有K2SO4和Al2(SO4)3的混合溶液,已知其中Al3+的物质的量浓度为0.2 mol/L,
 的物质的量浓度为0.5 mol/L,则此溶液中K+的物质的量浓度为
的物质的量浓度为0.5 mol/L,则此溶液中K+的物质的量浓度为(4)在标准状况下,CO和CO2的混合气体共11.2 L,质量为18.8 g,其中含有
您最近一年使用:0次



