填空。
(1)工业上用_______ 和_______ 作为原料来制取漂白粉,反应的化学方程式为_______ 。漂白粉的有效成分是_______ ,漂白粉溶于水后,滴加少量盐酸可加快漂白和杀菌的速度,此过程中发生反应的化学方程式_______ 。
(2)从200 mL、5 mol/L Na2CO3溶液中取出20 mL溶液,其溶质的物质的量是_______ 。将取出的溶液稀释至100 mL,其Na+的物质的量浓度是_______ 。
(3)有K2SO4和Al2(SO4)3的混合溶液,已知其中Al3+的物质的量浓度为0.2 mol/L, 的物质的量浓度为0.5 mol/L,则此溶液中K+的物质的量浓度为
的物质的量浓度为0.5 mol/L,则此溶液中K+的物质的量浓度为_______ 。
(4)在标准状况下,CO和CO2的混合气体共11.2 L,质量为18.8 g,其中含有_______ 个CO分子,该混合气体中CO与CO2的密度之比为_______ 。
(1)工业上用
(2)从200 mL、5 mol/L Na2CO3溶液中取出20 mL溶液,其溶质的物质的量是
(3)有K2SO4和Al2(SO4)3的混合溶液,已知其中Al3+的物质的量浓度为0.2 mol/L,
 的物质的量浓度为0.5 mol/L,则此溶液中K+的物质的量浓度为
的物质的量浓度为0.5 mol/L,则此溶液中K+的物质的量浓度为(4)在标准状况下,CO和CO2的混合气体共11.2 L,质量为18.8 g,其中含有
更新时间:2022-11-19 09:09:55
|
相似题推荐
填空题
|
较易
(0.85)
【推荐1】设NA为阿伏加德罗常数,完成下列问题。
(1)0.3molNH3分子中所含质子数与__ 个H2O分子中所含质子数相等。
(2)含0.4molAl3+的Al2(SO4)3中所含的SO 的物质的量是
的物质的量是___ 。
(3)已知16gA和20gB恰好完全反应生成0.04molC和31.76gD,则C的摩尔质量为___ 。
(4)如果ag某气体中含有的分子数为b,则cg该气体在标准状况下的体积是__ 。
(5)将质量比为14:15的N2和NO混合,则混合气体中N2和NO的物质的量之比为___ 。
(1)0.3molNH3分子中所含质子数与
(2)含0.4molAl3+的Al2(SO4)3中所含的SO
 的物质的量是
的物质的量是(3)已知16gA和20gB恰好完全反应生成0.04molC和31.76gD,则C的摩尔质量为
(4)如果ag某气体中含有的分子数为b,则cg该气体在标准状况下的体积是
(5)将质量比为14:15的N2和NO混合,则混合气体中N2和NO的物质的量之比为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】化学与生产、生活及科研密切相关。回答下列问题:
(1)《淮南子·说山训》云:慈石能引铁(慈,旧作磁)。“慈石”的主要成分是___________ (填化学式)。
(2)人造空气(氧气和氦气的混合气)可用于减轻某些疾病或供深水潜水员使用。在标准状况下,11.2L“人造空气”的质量是4.8g,其中氧气和氦气的分子数之比为___________ 。
(3)厨房中常用小苏打作面包和糕点的发泡剂,写出小苏打受热分解的化学方程式___________ 。
(4)科学家经过研究发现中国霾呈中性,其主要原因如图所示:

请判断A的符号是___________ 。
(5)火药是古代道士配出的“药”,燃放烟花爆竹“产生大量烟雾”,这种烟雾的成分是二氧化硫,与空气中的水分最终形成了稀硫酸气溶胶。下列说法正确的是___________ (填字母)。
A.二氧化硫与空气中的水通过化合反应直接形成稀硫酸
B.稀硫酸具有强氧化性,可用于杀菌消毒
C.烟花爆竹燃烧产生的 和可吸入颗粒物均属于大气污染物
和可吸入颗粒物均属于大气污染物
(6)据文献报道,难溶于水的 可在
可在 溶液中“溶解”,“溶解”后硫元素都以
溶液中“溶解”,“溶解”后硫元素都以 的形式存在。若要检验“溶解”后溶液中
的形式存在。若要检验“溶解”后溶液中 是否有剩余,简要写出相关的实验操作
是否有剩余,简要写出相关的实验操作___________ 。
(7) 和氮的氧化物以及它们在大气中发生反应后的生成物溶于雨水会形成酸雨,我们所说的酸雨是指其pH小于
和氮的氧化物以及它们在大气中发生反应后的生成物溶于雨水会形成酸雨,我们所说的酸雨是指其pH小于___________ 。
(8)氨气(NH3)在工农业中应用广泛,实验室制取氨气的化学方程式为___________
(1)《淮南子·说山训》云:慈石能引铁(慈,旧作磁)。“慈石”的主要成分是
(2)人造空气(氧气和氦气的混合气)可用于减轻某些疾病或供深水潜水员使用。在标准状况下,11.2L“人造空气”的质量是4.8g,其中氧气和氦气的分子数之比为
(3)厨房中常用小苏打作面包和糕点的发泡剂,写出小苏打受热分解的化学方程式
(4)科学家经过研究发现中国霾呈中性,其主要原因如图所示:

请判断A的符号是
(5)火药是古代道士配出的“药”,燃放烟花爆竹“产生大量烟雾”,这种烟雾的成分是二氧化硫,与空气中的水分最终形成了稀硫酸气溶胶。下列说法正确的是
A.二氧化硫与空气中的水通过化合反应直接形成稀硫酸
B.稀硫酸具有强氧化性,可用于杀菌消毒
C.烟花爆竹燃烧产生的
 和可吸入颗粒物均属于大气污染物
和可吸入颗粒物均属于大气污染物(6)据文献报道,难溶于水的
 可在
可在 溶液中“溶解”,“溶解”后硫元素都以
溶液中“溶解”,“溶解”后硫元素都以 的形式存在。若要检验“溶解”后溶液中
的形式存在。若要检验“溶解”后溶液中 是否有剩余,简要写出相关的实验操作
是否有剩余,简要写出相关的实验操作(7)
 和氮的氧化物以及它们在大气中发生反应后的生成物溶于雨水会形成酸雨,我们所说的酸雨是指其pH小于
和氮的氧化物以及它们在大气中发生反应后的生成物溶于雨水会形成酸雨,我们所说的酸雨是指其pH小于(8)氨气(NH3)在工农业中应用广泛,实验室制取氨气的化学方程式为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】完成下面问题
(1)同温同压下的两个容积相同的容器中分别装有O2和O3气体,则两瓶气体中分子数之比是_________ ,质量之比是__________ 。
(2)下列所给出的几组物质中:标准状况下体积最大的是_______ 。(填序号)
① 1gH2; ② 2.408×1023个CH4;③ 10.8gH2O; ④ 标准状况下6.72LCO2
(3)在紫外线作用下,氧气可转化为臭氧:3O2=2O3,低空臭氧的浓度过高时对人体有害,因此要尽量避免在阳光强烈照射的中午前后进行户外活动。1.6gO2和O3的混合气体中含有氧原子的数目为________ (用NA表示阿伏加德罗常数的值)。O2与O3的关系是____________ 。
(4)相同条件下,气体A相对与氢气的相对密度为14,则该气体的摩尔质量为_____________ 。
(5)在标准状况下15 g CO与CO2的混合气体,体积为11.2 L。该混合气体中CO与CO2的物质的量比为________________ 。
(1)同温同压下的两个容积相同的容器中分别装有O2和O3气体,则两瓶气体中分子数之比是
(2)下列所给出的几组物质中:标准状况下体积最大的是
① 1gH2; ② 2.408×1023个CH4;③ 10.8gH2O; ④ 标准状况下6.72LCO2
(3)在紫外线作用下,氧气可转化为臭氧:3O2=2O3,低空臭氧的浓度过高时对人体有害,因此要尽量避免在阳光强烈照射的中午前后进行户外活动。1.6gO2和O3的混合气体中含有氧原子的数目为
(4)相同条件下,气体A相对与氢气的相对密度为14,则该气体的摩尔质量为
(5)在标准状况下15 g CO与CO2的混合气体,体积为11.2 L。该混合气体中CO与CO2的物质的量比为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】按要求填空
(1)12.4gNa2R含Na+0.4mol,则Na2R的摩尔质量为__________ ;含R的质量为1.6g的Na2R,其物质的量为_____ 。
(2)质量分数为36.5%浓盐酸(密度为1.25g·mL-1)的物质的量浓度为_____________ 。
(3)请举出符合离子方程式:2H++ = H2O+CO2↑的化学方程式:
= H2O+CO2↑的化学方程式:_________ 。
(1)12.4gNa2R含Na+0.4mol,则Na2R的摩尔质量为
(2)质量分数为36.5%浓盐酸(密度为1.25g·mL-1)的物质的量浓度为
(3)请举出符合离子方程式:2H++
 = H2O+CO2↑的化学方程式:
= H2O+CO2↑的化学方程式:
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】离子反应广泛用于化学研究、化工生产、医疗诊断、环境保护等方面。现有四种溶液: A.盐酸 B.稀硫酸 C.NaOH溶液 D.Ba(OH)2溶液。这些溶液溶质物质的量浓度均为0.3 mol·L-1,根据溶液取用情况,判断得到的溶液中存在的主要离子及其浓度;或者根据最终离子的情况,推断最终溶液可能是哪些溶液按怎样的体积比混合的结果(忽略溶液混合后的体积变化)
| 溶液取用情况 | 溶液中存在的主要离子及其浓度 |
| 示例:只取溶液C | Na+ 和OH-物质的量浓度均为0.3mol·L-1 |
| 等体积混合溶液B和C | ① |
| 溶液A和D按体积比2:1混合 | ② |
| ③ | Ba2+物质的量浓度为0.1mol·L-1, OH-物质的量浓度为0.2mol·L-1 |
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】按要求填空。
(1)与 具有相同电子数且含两种元素的阴离子的符号为
具有相同电子数且含两种元素的阴离子的符号为______ 。
(2)某元素的一种同位素X的质量数为A,含N个中子,它与 原子组成
原子组成 分子。在a克
分子。在a克 中所含质子的物质的量是
中所含质子的物质的量是______ mol。
(3)10.8g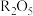 中氧原子的数目为
中氧原子的数目为 ,则元素R的相对原子质量为
,则元素R的相对原子质量为______ 。
(4)由CO、 两气体组成的混合气体12.8g,标况下,体积为8.96L,则CO和
两气体组成的混合气体12.8g,标况下,体积为8.96L,则CO和 的物质的量之比为
的物质的量之比为______ 。
(5) 和
和 的混合溶液,已知其中
的混合溶液,已知其中 物质的量浓度为
物质的量浓度为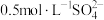 物质的量浓度为
物质的量浓度为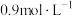 ,则
,则 的物质的量浓度为
的物质的量浓度为______  。
。
(6)体积相等的NaCl、 、
、 三种溶液,与等体积、等物质的量浓度的
三种溶液,与等体积、等物质的量浓度的 溶液均恰好完全反应,则NaCl、
溶液均恰好完全反应,则NaCl、 、
、 三种溶液的物质的量浓度之比为
三种溶液的物质的量浓度之比为______ 。
(7)等质量的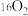 和
和 ,所含中子数之比为
,所含中子数之比为______ 。
(8)以下为中学化学中常见的几种物质:①液氨,②熔融KCl,③ 固体,④铜,⑤稀硫酸,⑥蔗糖,⑦澄清石灰水。请按下列分类标准回答问题。
固体,④铜,⑤稀硫酸,⑥蔗糖,⑦澄清石灰水。请按下列分类标准回答问题。
能导电的有______ (填写物质编号);属于电解质有______ (填写物质编号)
(9)如图是中学化学中常用于混合物分离和提纯的装置,请根据装置回答问题:
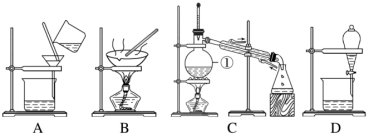
装置C中①的名称是______ ,在分液时,为使液体顺利滴下,应进行的具体操作是______ 。
(1)与
 具有相同电子数且含两种元素的阴离子的符号为
具有相同电子数且含两种元素的阴离子的符号为(2)某元素的一种同位素X的质量数为A,含N个中子,它与
 原子组成
原子组成 分子。在a克
分子。在a克 中所含质子的物质的量是
中所含质子的物质的量是(3)10.8g
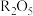 中氧原子的数目为
中氧原子的数目为 ,则元素R的相对原子质量为
,则元素R的相对原子质量为(4)由CO、
 两气体组成的混合气体12.8g,标况下,体积为8.96L,则CO和
两气体组成的混合气体12.8g,标况下,体积为8.96L,则CO和 的物质的量之比为
的物质的量之比为(5)
 和
和 的混合溶液,已知其中
的混合溶液,已知其中 物质的量浓度为
物质的量浓度为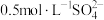 物质的量浓度为
物质的量浓度为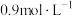 ,则
,则 的物质的量浓度为
的物质的量浓度为 。
。(6)体积相等的NaCl、
 、
、 三种溶液,与等体积、等物质的量浓度的
三种溶液,与等体积、等物质的量浓度的 溶液均恰好完全反应,则NaCl、
溶液均恰好完全反应,则NaCl、 、
、 三种溶液的物质的量浓度之比为
三种溶液的物质的量浓度之比为(7)等质量的
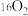 和
和 ,所含中子数之比为
,所含中子数之比为(8)以下为中学化学中常见的几种物质:①液氨,②熔融KCl,③
 固体,④铜,⑤稀硫酸,⑥蔗糖,⑦澄清石灰水。请按下列分类标准回答问题。
固体,④铜,⑤稀硫酸,⑥蔗糖,⑦澄清石灰水。请按下列分类标准回答问题。能导电的有
(9)如图是中学化学中常用于混合物分离和提纯的装置,请根据装置回答问题:

装置C中①的名称是
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】如图为浓硫酸的标签。

图示浓硫酸的物质的量浓度为多少___ ?配制200mL4.6mol/L的稀硫酸需取该硫酸多少体积___ ?

图示浓硫酸的物质的量浓度为多少
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】取10g 硫酸铁溶于水配成100ml溶液,
(1)该硫酸铁的物质的量浓度___________
(2)Fe3+物质的量浓度___________
(3)取出该溶液20ml含SO 物质的量为
物质的量为___________ ,然后稀释,使其硫酸铁物质的量浓度变为0.05mol/L,则应加水___________ ml(设稀释时,对溶液体积的影响忽略不计)
(1)该硫酸铁的物质的量浓度
(2)Fe3+物质的量浓度
(3)取出该溶液20ml含SO
 物质的量为
物质的量为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】氯及其化合物在生产生活中有重要的作用。
(1)已知某品牌的84消毒液和洁厕灵的部分标签如图所示:
①王女士在清洁马桶时,在倒入上述洁厕灵后将上述84消毒液也倒入其中,随后突然晕倒,送往医院抢救无效死亡。该过程发生反应的离子方程式为_______ 。
②已知“有效氯”的基本含义是指一定质量的这种消毒剂与多少质量的氯气的氧化能力相当,其数值可以用此时氯气的质量对消毒剂质量的百分比表示。例如,100g某84消毒液与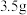 氯气的氧化能力相当,该产品的“有效氯”就是
氯气的氧化能力相当,该产品的“有效氯”就是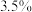 。
。
上述500mL“××牌84消毒液”中含有的 的质量为
的质量为_______ g(“有效氯”含量按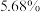 、溶液密度按
、溶液密度按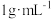 计算);现需要将原消毒液与水按
计算);现需要将原消毒液与水按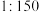 比例稀释后用于织物消毒。则稀释后的溶液中
比例稀释后用于织物消毒。则稀释后的溶液中 的浓度为
的浓度为_______  (忽略混合后溶液体积变化,保留两位有效数字)。
(忽略混合后溶液体积变化,保留两位有效数字)。
(2) 越来越多地取代以次氯酸盐为有效成分的漂白剂和消毒剂。其制取方法有多种,如图是其中的一种制取方法:
越来越多地取代以次氯酸盐为有效成分的漂白剂和消毒剂。其制取方法有多种,如图是其中的一种制取方法:
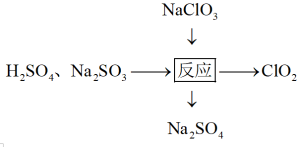
写出该反应的化学方程式并用单线桥表示电子转移的方向和数目_______ ,该反应的还原剂为_______ 。
(1)已知某品牌的84消毒液和洁厕灵的部分标签如图所示:
| ××牌洁厕灵 规格:1L 有效成分:盐酸,表面活性剂,香精 | ××牌84消毒液 规格:  有效成分:  (“有效氯”含量:  ) ) |
①王女士在清洁马桶时,在倒入上述洁厕灵后将上述84消毒液也倒入其中,随后突然晕倒,送往医院抢救无效死亡。该过程发生反应的离子方程式为
②已知“有效氯”的基本含义是指一定质量的这种消毒剂与多少质量的氯气的氧化能力相当,其数值可以用此时氯气的质量对消毒剂质量的百分比表示。例如,100g某84消毒液与
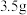 氯气的氧化能力相当,该产品的“有效氯”就是
氯气的氧化能力相当,该产品的“有效氯”就是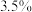 。
。上述500mL“××牌84消毒液”中含有的
 的质量为
的质量为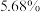 、溶液密度按
、溶液密度按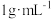 计算);现需要将原消毒液与水按
计算);现需要将原消毒液与水按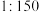 比例稀释后用于织物消毒。则稀释后的溶液中
比例稀释后用于织物消毒。则稀释后的溶液中 的浓度为
的浓度为 (忽略混合后溶液体积变化,保留两位有效数字)。
(忽略混合后溶液体积变化,保留两位有效数字)。(2)
 越来越多地取代以次氯酸盐为有效成分的漂白剂和消毒剂。其制取方法有多种,如图是其中的一种制取方法:
越来越多地取代以次氯酸盐为有效成分的漂白剂和消毒剂。其制取方法有多种,如图是其中的一种制取方法:
写出该反应的化学方程式并用单线桥表示电子转移的方向和数目
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】(1)①写出漂白粉有效成分的化学式:_____ ;
②写出乙炔的结构式:______ 。
(2)写出实验室用二氧化锰与浓盐酸共热制备氯气的离子方程式:______ 。
(3)写出制备聚丙烯的化学方程式:______ 。
②写出乙炔的结构式:
(2)写出实验室用二氧化锰与浓盐酸共热制备氯气的离子方程式:
(3)写出制备聚丙烯的化学方程式:
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】按要求写出下列化学方程式。
(1)钠与熔融四氯化钛(TiCl4)反应:___ 。
(2)工业生产漂白粉:___ 。
(3)氯气和氢氧化钠溶液:___ 。
(4)过氧化钠与水反应:___ 。
(5)次氯酸光照分解:___ 。
(1)钠与熔融四氯化钛(TiCl4)反应:
(2)工业生产漂白粉:
(3)氯气和氢氧化钠溶液:
(4)过氧化钠与水反应:
(5)次氯酸光照分解:
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】回答下列问题:
(1)漂白粉是一种常用消毒剂,其中的有效成分是________ (写出化学式)。
(2)高铁酸钠(Na2FeO4)可以用作自来水处理剂,高铁酸钠处理过程中有氢氧化铁胶体生成,则高铁酸钠作自来水处理剂的优点是________ 。
(3)铁是应用最广泛的金属,铁有卤化物、氧化物以及高价铁的含氧酸盐等。电子工业常用 30%的 FeCl3溶液腐蚀敷在绝缘板上的铜箔,制造印刷电路板。请写出 FeCl3 溶液与铜反应的离子方程式________ ;如何检验 FeCl3 腐蚀铜后的溶液是否含 Fe3+ ________ 。
(4)在用二氧化氯进行水处理时,ClO2 除了杀菌消毒外,还能除去水中的 Fe2+和 Mn2+。用 ClO2氧化除去 Mn2+生成 和 MnO2的离子方程式为
和 MnO2的离子方程式为 ________________ 。
(1)漂白粉是一种常用消毒剂,其中的有效成分是
(2)高铁酸钠(Na2FeO4)可以用作自来水处理剂,高铁酸钠处理过程中有氢氧化铁胶体生成,则高铁酸钠作自来水处理剂的优点是
(3)铁是应用最广泛的金属,铁有卤化物、氧化物以及高价铁的含氧酸盐等。电子工业常用 30%的 FeCl3溶液腐蚀敷在绝缘板上的铜箔,制造印刷电路板。请写出 FeCl3 溶液与铜反应的离子方程式
(4)在用二氧化氯进行水处理时,ClO2 除了杀菌消毒外,还能除去水中的 Fe2+和 Mn2+。用 ClO2氧化除去 Mn2+生成
 和 MnO2的离子方程式为
和 MnO2的离子方程式为
您最近一年使用:0次



