氯及其化合物在生产生活中有重要的作用。
(1)已知某品牌的84消毒液和洁厕灵的部分标签如图所示:
①王女士在清洁马桶时,在倒入上述洁厕灵后将上述84消毒液也倒入其中,随后突然晕倒,送往医院抢救无效死亡。该过程发生反应的离子方程式为_______ 。
②已知“有效氯”的基本含义是指一定质量的这种消毒剂与多少质量的氯气的氧化能力相当,其数值可以用此时氯气的质量对消毒剂质量的百分比表示。例如,100g某84消毒液与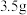 氯气的氧化能力相当,该产品的“有效氯”就是
氯气的氧化能力相当,该产品的“有效氯”就是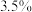 。
。
上述500mL“××牌84消毒液”中含有的 的质量为
的质量为_______ g(“有效氯”含量按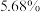 、溶液密度按
、溶液密度按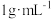 计算);现需要将原消毒液与水按
计算);现需要将原消毒液与水按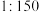 比例稀释后用于织物消毒。则稀释后的溶液中
比例稀释后用于织物消毒。则稀释后的溶液中 的浓度为
的浓度为_______  (忽略混合后溶液体积变化,保留两位有效数字)。
(忽略混合后溶液体积变化,保留两位有效数字)。
(2) 越来越多地取代以次氯酸盐为有效成分的漂白剂和消毒剂。其制取方法有多种,如图是其中的一种制取方法:
越来越多地取代以次氯酸盐为有效成分的漂白剂和消毒剂。其制取方法有多种,如图是其中的一种制取方法:
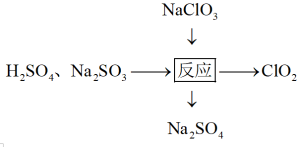
写出该反应的化学方程式并用单线桥表示电子转移的方向和数目_______ ,该反应的还原剂为_______ 。
(1)已知某品牌的84消毒液和洁厕灵的部分标签如图所示:
| ××牌洁厕灵 规格:1L 有效成分:盐酸,表面活性剂,香精 | ××牌84消毒液 规格:  有效成分:  (“有效氯”含量:  ) ) |
①王女士在清洁马桶时,在倒入上述洁厕灵后将上述84消毒液也倒入其中,随后突然晕倒,送往医院抢救无效死亡。该过程发生反应的离子方程式为
②已知“有效氯”的基本含义是指一定质量的这种消毒剂与多少质量的氯气的氧化能力相当,其数值可以用此时氯气的质量对消毒剂质量的百分比表示。例如,100g某84消毒液与
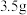 氯气的氧化能力相当,该产品的“有效氯”就是
氯气的氧化能力相当,该产品的“有效氯”就是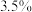 。
。上述500mL“××牌84消毒液”中含有的
 的质量为
的质量为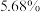 、溶液密度按
、溶液密度按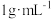 计算);现需要将原消毒液与水按
计算);现需要将原消毒液与水按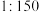 比例稀释后用于织物消毒。则稀释后的溶液中
比例稀释后用于织物消毒。则稀释后的溶液中 的浓度为
的浓度为 (忽略混合后溶液体积变化,保留两位有效数字)。
(忽略混合后溶液体积变化,保留两位有效数字)。(2)
 越来越多地取代以次氯酸盐为有效成分的漂白剂和消毒剂。其制取方法有多种,如图是其中的一种制取方法:
越来越多地取代以次氯酸盐为有效成分的漂白剂和消毒剂。其制取方法有多种,如图是其中的一种制取方法:
写出该反应的化学方程式并用单线桥表示电子转移的方向和数目
更新时间:2022-01-25 18:13:37
|
相似题推荐
填空题
|
较易
(0.85)
【推荐1】(1)4gH2与24.5L(常温常压)CO2相比,所含分子数目多的是____ ;各1.5 mol上述两种气体相比较,质量大的是_____
(2)在温度和压强相等的条件下,氧气和氢气的密度比为____ ,质量相等时的体积比为____ ,体积相等时的物质的量之比为____ 。
(2)在温度和压强相等的条件下,氧气和氢气的密度比为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】现有14.4gCO和CO2的混合气体,在标准状况下所占的体积约为8.96L。回答下列问题:
(1)该混合气体中CO物质的量为________ mol;CO2物质的量为_________ mol;
(2)混合气体中碳原子的个数___________ ;(用NA表示阿伏伽德罗常数的值)
(3)将混合气体依次通过如图装置,最后收集在气球中。

①气球中收集到的气体的摩尔质量_________ ;
②标况下气球中收集到的气体的体积为________________ ;
③气球中收集到的气体的电子总数为________ ;(用NA表示阿伏伽德罗常数的值)
(1)该混合气体中CO物质的量为
(2)混合气体中碳原子的个数
(3)将混合气体依次通过如图装置,最后收集在气球中。

①气球中收集到的气体的摩尔质量
②标况下气球中收集到的气体的体积为
③气球中收集到的气体的电子总数为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】填空。
(1)工业上用_______ 和_______ 作为原料来制取漂白粉,反应的化学方程式为_______ 。漂白粉的有效成分是_______ ,漂白粉溶于水后,滴加少量盐酸可加快漂白和杀菌的速度,此过程中发生反应的化学方程式_______ 。
(2)从200 mL、5 mol/L Na2CO3溶液中取出20 mL溶液,其溶质的物质的量是_______ 。将取出的溶液稀释至100 mL,其Na+的物质的量浓度是_______ 。
(3)有K2SO4和Al2(SO4)3的混合溶液,已知其中Al3+的物质的量浓度为0.2 mol/L, 的物质的量浓度为0.5 mol/L,则此溶液中K+的物质的量浓度为
的物质的量浓度为0.5 mol/L,则此溶液中K+的物质的量浓度为_______ 。
(4)在标准状况下,CO和CO2的混合气体共11.2 L,质量为18.8 g,其中含有_______ 个CO分子,该混合气体中CO与CO2的密度之比为_______ 。
(1)工业上用
(2)从200 mL、5 mol/L Na2CO3溶液中取出20 mL溶液,其溶质的物质的量是
(3)有K2SO4和Al2(SO4)3的混合溶液,已知其中Al3+的物质的量浓度为0.2 mol/L,
 的物质的量浓度为0.5 mol/L,则此溶液中K+的物质的量浓度为
的物质的量浓度为0.5 mol/L,则此溶液中K+的物质的量浓度为(4)在标准状况下,CO和CO2的混合气体共11.2 L,质量为18.8 g,其中含有
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】某同学按下列步骤配制500mL0.2mol·L-1Na2SO4溶液。
(1)上述实验中使用容量瓶前应_______ 。
(2)需要Na2SO4的质量为_______ 克。
(3)取出该Na2SO4溶液10mL加水稀释到100mL,稀释后溶液中Na+的物质的量浓度是_______ mol·L-1。
(4)若定容加蒸馏水时超过刻度线,则需要_______ 。
(5)在实验中,以下操作可能造成实验结果偏低的是_______ (填序号)。
A.定容时仰视刻度线
B.称量时砝码和物体放反
C.转移前没有将使用的容量瓶烘干
D.在转移溶液时有液体溅到容量瓶外
E.定容摇匀后,发现凹液面低于刻度线,又用胶头滴管加蒸馏水至刻度线
(1)上述实验中使用容量瓶前应
(2)需要Na2SO4的质量为
(3)取出该Na2SO4溶液10mL加水稀释到100mL,稀释后溶液中Na+的物质的量浓度是
(4)若定容加蒸馏水时超过刻度线,则需要
(5)在实验中,以下操作可能造成实验结果偏低的是
A.定容时仰视刻度线
B.称量时砝码和物体放反
C.转移前没有将使用的容量瓶烘干
D.在转移溶液时有液体溅到容量瓶外
E.定容摇匀后,发现凹液面低于刻度线,又用胶头滴管加蒸馏水至刻度线
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】硫有多种含氧酸,亚硫酸(H2SO3)、硫酸(H2SO4)、焦硫酸(H2SO4·SO3)……等,其中硫酸最为重要,在工业上有广泛的应用。试回答以下问题(并写出必要的过程):
(1)已知某硫酸溶液的的密度为1.84 g/cm3,质量分数为98%,该硫酸溶液的物质的量浓度为_____ mol·L-1。
(2)若将其稀释为500mL 0.2mol/L的溶液,需用量筒取该浓硫酸___________ mL
(3)焦硫酸(H2SO4·SO3)溶于水,其中的SO3都转化为硫酸。若将89 g焦硫酸溶于水配成800 mL硫酸,则该硫酸的物质的量浓度为_____ mol·L-1。
(4)硫铁矿是工业上制硫酸的主要原料。硫铁矿氧化焙烧的化学反应如下:3FeS2+8 O2=Fe3O4+6SO2,4FeS2+11 O2=2Fe2O3+8SO2,若2.4 mol FeS2完全反应耗用氧气145.6 L(标准状况),计算反应产物中Fe3O4与Fe2O3物质的量之比___________ 。
(1)已知某硫酸溶液的的密度为1.84 g/cm3,质量分数为98%,该硫酸溶液的物质的量浓度为
(2)若将其稀释为500mL 0.2mol/L的溶液,需用量筒取该浓硫酸
(3)焦硫酸(H2SO4·SO3)溶于水,其中的SO3都转化为硫酸。若将89 g焦硫酸溶于水配成800 mL硫酸,则该硫酸的物质的量浓度为
(4)硫铁矿是工业上制硫酸的主要原料。硫铁矿氧化焙烧的化学反应如下:3FeS2+8 O2=Fe3O4+6SO2,4FeS2+11 O2=2Fe2O3+8SO2,若2.4 mol FeS2完全反应耗用氧气145.6 L(标准状况),计算反应产物中Fe3O4与Fe2O3物质的量之比
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】硫元素的氢化物与氧化物都是大气污染物,硫单质是古代四大发明之一黑火药的重要成分。
(1)在实验室可以用足量的NaOH溶液来吸收SO2,请写出其反应方程式____________ 。
(2)SO2是导致酸雨的主要原因之一,请写出SO2转化为H2SO4的化学方程式_____________ 。
(3)请你提出防治SO2污染的措施(任写一点)_______________ 。
(1)在实验室可以用足量的NaOH溶液来吸收SO2,请写出其反应方程式
(2)SO2是导致酸雨的主要原因之一,请写出SO2转化为H2SO4的化学方程式
(3)请你提出防治SO2污染的措施(任写一点)
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】“价-类”二维图是学习化学的一种重要工具.如图为硫元素的“价-类”二维图,回答下列问题:
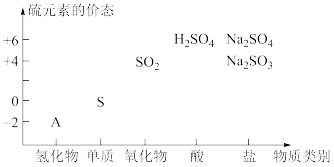
(1)A的化学式为_______ 。
(2) 与A溶液反应有淡黄色固体生成,该反应的化学方程式为
与A溶液反应有淡黄色固体生成,该反应的化学方程式为_______ ,体现了A的_______ (填“氧化性”或“还原性”)。
(3)①将 通入品红溶液,观察到的现象为
通入品红溶液,观察到的现象为_______ ,体现了 的
的_______ 性。
②将 通入新制氯水中主要反应的离子方程式为
通入新制氯水中主要反应的离子方程式为_______ 。
(4)写出浓硫酸与 反应的化学方程式
反应的化学方程式_______ ,反应中消耗了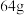 铜,则转移
铜,则转移_______  电子。
电子。
(5)大苏打( )在照相、电影、纺织、化纤、造纸、皮革、农药等方面均有重要作用。现欲在实验室制备大苏打,从氧化还原角度分析,下列合理的是_______(填标号)。
)在照相、电影、纺织、化纤、造纸、皮革、农药等方面均有重要作用。现欲在实验室制备大苏打,从氧化还原角度分析,下列合理的是_______(填标号)。

(1)A的化学式为
(2)
 与A溶液反应有淡黄色固体生成,该反应的化学方程式为
与A溶液反应有淡黄色固体生成,该反应的化学方程式为(3)①将
 通入品红溶液,观察到的现象为
通入品红溶液,观察到的现象为 的
的②将
 通入新制氯水中主要反应的离子方程式为
通入新制氯水中主要反应的离子方程式为(4)写出浓硫酸与
 反应的化学方程式
反应的化学方程式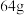 铜,则转移
铜,则转移 电子。
电子。(5)大苏打(
 )在照相、电影、纺织、化纤、造纸、皮革、农药等方面均有重要作用。现欲在实验室制备大苏打,从氧化还原角度分析,下列合理的是_______(填标号)。
)在照相、电影、纺织、化纤、造纸、皮革、农药等方面均有重要作用。现欲在实验室制备大苏打,从氧化还原角度分析,下列合理的是_______(填标号)。A. | B. | C. | D.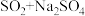 |
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】已知反应:①SO2 + H2O = H2SO3 ②2SO2 + O2 = 2SO3 ③SO2 + 2H2S = 3S↓ + 2H2O
(1)上述反应中不属于氧化还原反应的是_______ (填序号);SO2做还原剂的是_______ (填序号),SO2做氧化剂的是_______ (填序号)。
(2)用双线桥法标出反应②的电子转移方向和数目:_______ 。
(3)反应③中,参与反应的氧化剂与还原剂的质量比是_______ 。
(4)误食亚硝酸钠(NaNO2)会使人体血液中的Fe2+转化为Fe3+而引起中毒,服用维生素C可使Fe3+转化为Fe2+,从而达到解毒的目的。由此可见,在解毒反应中,维生素C表现_______ 性。
(1)上述反应中不属于氧化还原反应的是
(2)用双线桥法标出反应②的电子转移方向和数目:
(3)反应③中,参与反应的氧化剂与还原剂的质量比是
(4)误食亚硝酸钠(NaNO2)会使人体血液中的Fe2+转化为Fe3+而引起中毒,服用维生素C可使Fe3+转化为Fe2+,从而达到解毒的目的。由此可见,在解毒反应中,维生素C表现
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】用单线桥法表示下列反应的的电子转移情况并将其改写成离子方程式:3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O,离子方程式为___________________________________ 。
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】
(1)已知氯气通入热的苛性钠溶液中会发生如下反应:
3Cl2+6NaOH=5NaCl+NaClO3+3H2O
①反应中还原剂是____________ (填化学式);
②把此反应改写成离子方程式:______________________ ;
③若消耗106.5gCl2,则生成的氧化产物的物质的量是____________________ 。
(2)用“双线桥”表示下列氧化还原反应中电子转移的方向和数目:______
3Cl2+6NaOH=5NaCl+ NaClO3+3H2O
(1)已知氯气通入热的苛性钠溶液中会发生如下反应:
3Cl2+6NaOH=5NaCl+NaClO3+3H2O
①反应中还原剂是
②把此反应改写成离子方程式:
③若消耗106.5gCl2,则生成的氧化产物的物质的量是
(2)用“双线桥”表示下列氧化还原反应中电子转移的方向和数目:
3Cl2+6NaOH=5NaCl+ NaClO3+3H2O
您最近一年使用:0次



