如图为实验室某浓盐酸试剂瓶标签上的有关数据,根据有关数据回答下列问题:
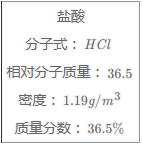
(1)该浓盐酸中HCl的物质的量浓度为________ mol/L。
(2)取用任意体积的该盐酸溶液时,下列物理量不随所取体积多少而变化的是_______ 。
A.溶液中HCl的质量
B.溶液的pH
C.溶液中H+的数目
D.溶液的密度
(3)欲用上述浓盐酸配制500mL 2mol/L的稀盐酸,需要_____ mL上述盐酸 (保留1位小数)
(4)现有1 L1mol/L的稀盐酸,欲使其浓度增大1倍。采取的措施合理的是________________ 。
A、通入标况下HCl气体22.4L
B、将溶液加热浓缩至0. 5L
C、加入5mol/L的盐酸0.6L.再稀释至2L.
D、加入1L 3mol/L的盐酸混合均匀

(1)该浓盐酸中HCl的物质的量浓度为
(2)取用任意体积的该盐酸溶液时,下列物理量不随所取体积多少而变化的是
A.溶液中HCl的质量
B.溶液的pH
C.溶液中H+的数目
D.溶液的密度
(3)欲用上述浓盐酸配制500mL 2mol/L的稀盐酸,需要
(4)现有1 L1mol/L的稀盐酸,欲使其浓度增大1倍。采取的措施合理的是
A、通入标况下HCl气体22.4L
B、将溶液加热浓缩至0. 5L
C、加入5mol/L的盐酸0.6L.再稀释至2L.
D、加入1L 3mol/L的盐酸混合均匀
19-20高一·江西南昌·阶段练习 查看更多[1]
(已下线)【南昌新东方】13. 新建二中 梁莎.
更新时间:2020-10-30 23:25:26
|
相似题推荐
填空题
|
较易
(0.85)
名校
【推荐1】现有下列十种物质:①液态氯化氢;②小苏打;③固体纯碱:④二氧化碳;⑤葡萄糖:⑥氢氧化钾;⑦氢氧化铁胶体;⑧氨水;⑨空气;⑩硫酸铁溶液
(1)上述十种物质中,属于电解质的有________ (填序号),属于非电解质的有________ (填序号)
(2)除去③中少量②的操作是________ ,化学方程式为________ ;
(3)现有100mL⑩溶液中含Fe3+5.6g,则溶液中 的物质的量浓度是
的物质的量浓度是________ ;
(4)若在⑦中缓慢加入①的水溶液,产生的现象是________ 。
(1)上述十种物质中,属于电解质的有
(2)除去③中少量②的操作是
(3)现有100mL⑩溶液中含Fe3+5.6g,则溶液中
 的物质的量浓度是
的物质的量浓度是(4)若在⑦中缓慢加入①的水溶液,产生的现象是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】硫有多种含氧酸,亚硫酸(H2SO3)、硫酸(H2SO4)、焦硫酸(H2SO4·SO3)……等,其中硫酸最为重要,在工业上有广泛的应用。试回答以下问题(并写出必要的过程):
(1)已知某硫酸溶液的的密度为1.84 g/cm3,质量分数为98%,该硫酸溶液的物质的量浓度为_____ mol·L-1。
(2)若将其稀释为500mL 0.2mol/L的溶液,需用量筒取该浓硫酸___________ mL
(3)焦硫酸(H2SO4·SO3)溶于水,其中的SO3都转化为硫酸。若将89 g焦硫酸溶于水配成800 mL硫酸,则该硫酸的物质的量浓度为_____ mol·L-1。
(4)硫铁矿是工业上制硫酸的主要原料。硫铁矿氧化焙烧的化学反应如下:3FeS2+8 O2=Fe3O4+6SO2,4FeS2+11 O2=2Fe2O3+8SO2,若2.4 mol FeS2完全反应耗用氧气145.6 L(标准状况),计算反应产物中Fe3O4与Fe2O3物质的量之比___________ 。
(1)已知某硫酸溶液的的密度为1.84 g/cm3,质量分数为98%,该硫酸溶液的物质的量浓度为
(2)若将其稀释为500mL 0.2mol/L的溶液,需用量筒取该浓硫酸
(3)焦硫酸(H2SO4·SO3)溶于水,其中的SO3都转化为硫酸。若将89 g焦硫酸溶于水配成800 mL硫酸,则该硫酸的物质的量浓度为
(4)硫铁矿是工业上制硫酸的主要原料。硫铁矿氧化焙烧的化学反应如下:3FeS2+8 O2=Fe3O4+6SO2,4FeS2+11 O2=2Fe2O3+8SO2,若2.4 mol FeS2完全反应耗用氧气145.6 L(标准状况),计算反应产物中Fe3O4与Fe2O3物质的量之比
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】质量、物质的量、物质的量浓度等是用于化学计算的常见物理量,根据所学知识回答下列问题。
(1)标准状况下,17gNH3的体积为___________ ,含有氢原子个数为___________ ,它与标准状况下___________ L H2S含有相同数目的氢原子。
(2)某气体氧化物的化学式为RO2,在标准状况下,1.28g该氧化物的体积为448mL,则该氧化物的摩尔质量为___________ ,R的相对原子质量为___________ 。
(3)现有含 、
、 和
和 的混合溶液
的混合溶液 ,已知其中
,已知其中 ,
, ,
,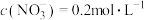 ,则此溶液中
,则此溶液中 为
为___________  。
。
(4) 溶液中含
溶液中含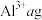 ,取
,取 溶液稀释到
溶液稀释到 ,则稀释后溶液中
,则稀释后溶液中 的物质的量浓度是
的物质的量浓度是___________  。
。
(5)标准状况下,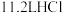 的物质的量是
的物质的量是___________  ,将这些气体溶于水中配成
,将这些气体溶于水中配成 溶液,所得盐酸的物质的量浓度是
溶液,所得盐酸的物质的量浓度是___________  。
。
(1)标准状况下,17gNH3的体积为
(2)某气体氧化物的化学式为RO2,在标准状况下,1.28g该氧化物的体积为448mL,则该氧化物的摩尔质量为
(3)现有含
 、
、 和
和 的混合溶液
的混合溶液 ,已知其中
,已知其中 ,
, ,
,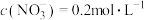 ,则此溶液中
,则此溶液中 为
为 。
。(4)
 溶液中含
溶液中含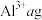 ,取
,取 溶液稀释到
溶液稀释到 ,则稀释后溶液中
,则稀释后溶液中 的物质的量浓度是
的物质的量浓度是 。
。(5)标准状况下,
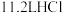 的物质的量是
的物质的量是 ,将这些气体溶于水中配成
,将这些气体溶于水中配成 溶液,所得盐酸的物质的量浓度是
溶液,所得盐酸的物质的量浓度是 。
。
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】25℃时,向20mL硫酸氢钠和盐酸的混合液中,逐滴加入0.05 mol∙L−1Ba(OH)2溶液时,生成BaSO4的量和溶液的pH变化如图(忽略溶液混合时溶液体积的变化),计算:

(1)原混合液中硫酸氢钠的物质的量浓度___ 。
(2)原混合液中HCl的物质的量浓度___ 。
(3)B点时溶液的pH___ 。

(1)原混合液中硫酸氢钠的物质的量浓度
(2)原混合液中HCl的物质的量浓度
(3)B点时溶液的pH
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】近年来,我国储氢碳管研究获得重大进展,电弧法合成碳纳米管,常伴有大量物质——碳纳米颗粒,这种碳纳米颗粒可用氧化气化法提纯,其反应的化学方程式为: 。
。
请回答下列问题。
(1) 的摩尔质量为
的摩尔质量为_______ , 的物质的量为
的物质的量为_______
(2)配制 溶液
溶液 ,则需要密度
,则需要密度 质量分数98%的
质量分数98%的 的体积为
的体积为_______ 
(3)在上述的反应中,若生成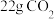
i.标准状况下, 的体积为
的体积为_______ L
ii.转移电子的数目为_______
(4)在上述反应中,氧化剂是_______ ,被氧化的元素是_______ 。
 。
。请回答下列问题。
(1)
 的摩尔质量为
的摩尔质量为 的物质的量为
的物质的量为(2)配制
 溶液
溶液 ,则需要密度
,则需要密度 质量分数98%的
质量分数98%的 的体积为
的体积为
(3)在上述的反应中,若生成
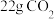
i.标准状况下,
 的体积为
的体积为ii.转移电子的数目为
(4)在上述反应中,氧化剂是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】某化学兴趣小组取4.6g Na投入99.6g滴有无色酚酞的水中,充分反应后得到密度为1.04g·cm-3的NaOH溶液。根据所学知识,按要求回答下列问题:
(1)该过程中发生反应的化学方程式为___________ 。
(2)该过程中生成的气体在标准状况下的体积为___________ L;反应过程中转移的电子数约为___________ 。
(3)所得NaOH溶液的物质的量浓度为___________ mol·L-1;从中取出5mL后,剩余NaOH溶液中c(Na+)=___________ mol·L-1。
(4)用量筒量取___________ mL上述所得NaOH溶液,可配得100mL 0.5mol·L-1 NaOH溶液。
(1)该过程中发生反应的化学方程式为
(2)该过程中生成的气体在标准状况下的体积为
(3)所得NaOH溶液的物质的量浓度为
(4)用量筒量取
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】氯及其化合物在生产生活中有重要的作用。
(1)已知某品牌的84消毒液和洁厕灵的部分标签如图所示:
①王女士在清洁马桶时,在倒入上述洁厕灵后将上述84消毒液也倒入其中,随后突然晕倒,送往医院抢救无效死亡。该过程发生反应的离子方程式为_______ 。
②已知“有效氯”的基本含义是指一定质量的这种消毒剂与多少质量的氯气的氧化能力相当,其数值可以用此时氯气的质量对消毒剂质量的百分比表示。例如,100g某84消毒液与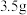 氯气的氧化能力相当,该产品的“有效氯”就是
氯气的氧化能力相当,该产品的“有效氯”就是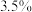 。
。
上述500mL“××牌84消毒液”中含有的 的质量为
的质量为_______ g(“有效氯”含量按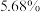 、溶液密度按
、溶液密度按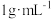 计算);现需要将原消毒液与水按
计算);现需要将原消毒液与水按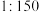 比例稀释后用于织物消毒。则稀释后的溶液中
比例稀释后用于织物消毒。则稀释后的溶液中 的浓度为
的浓度为_______  (忽略混合后溶液体积变化,保留两位有效数字)。
(忽略混合后溶液体积变化,保留两位有效数字)。
(2) 越来越多地取代以次氯酸盐为有效成分的漂白剂和消毒剂。其制取方法有多种,如图是其中的一种制取方法:
越来越多地取代以次氯酸盐为有效成分的漂白剂和消毒剂。其制取方法有多种,如图是其中的一种制取方法:
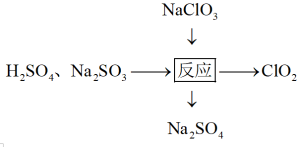
写出该反应的化学方程式并用单线桥表示电子转移的方向和数目_______ ,该反应的还原剂为_______ 。
(1)已知某品牌的84消毒液和洁厕灵的部分标签如图所示:
| ××牌洁厕灵 规格:1L 有效成分:盐酸,表面活性剂,香精 | ××牌84消毒液 规格:  有效成分:  (“有效氯”含量:  ) ) |
①王女士在清洁马桶时,在倒入上述洁厕灵后将上述84消毒液也倒入其中,随后突然晕倒,送往医院抢救无效死亡。该过程发生反应的离子方程式为
②已知“有效氯”的基本含义是指一定质量的这种消毒剂与多少质量的氯气的氧化能力相当,其数值可以用此时氯气的质量对消毒剂质量的百分比表示。例如,100g某84消毒液与
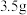 氯气的氧化能力相当,该产品的“有效氯”就是
氯气的氧化能力相当,该产品的“有效氯”就是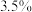 。
。上述500mL“××牌84消毒液”中含有的
 的质量为
的质量为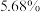 、溶液密度按
、溶液密度按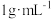 计算);现需要将原消毒液与水按
计算);现需要将原消毒液与水按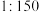 比例稀释后用于织物消毒。则稀释后的溶液中
比例稀释后用于织物消毒。则稀释后的溶液中 的浓度为
的浓度为 (忽略混合后溶液体积变化,保留两位有效数字)。
(忽略混合后溶液体积变化,保留两位有效数字)。(2)
 越来越多地取代以次氯酸盐为有效成分的漂白剂和消毒剂。其制取方法有多种,如图是其中的一种制取方法:
越来越多地取代以次氯酸盐为有效成分的漂白剂和消毒剂。其制取方法有多种,如图是其中的一种制取方法:
写出该反应的化学方程式并用单线桥表示电子转移的方向和数目
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】在0.4L由NaCl、MgCl2、CaCl2组成的混合液中,部分离子浓度大小如图所示,回答下列问题。

(1)该混合液中,NaCl的物质的量为___________ mol,含溶质MgCl2的质量为___________ g.
(2)该混合液中CaCl2的物质的量为___________ mol,将该混合液加水稀释至体积为2L,稀释后溶液中Ca2+的物质的量浓度为___________  。
。
(3)取该稀释后的溶液1L,加入足量硝酸化的硝酸银溶液,可得到沉淀___________ mol。

(1)该混合液中,NaCl的物质的量为
(2)该混合液中CaCl2的物质的量为
 。
。(3)取该稀释后的溶液1L,加入足量硝酸化的硝酸银溶液,可得到沉淀
您最近一年使用:0次

 )=
)=

