如图所示,若电解5 min时,测得铜电极的质量增加2.16 g。试回答:
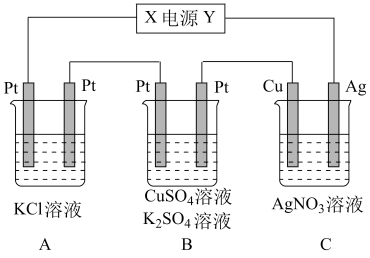
(1)电源中Y极是____ (填“正”或“负”)极,C中银电极发生的电极反应式是___
(2)通电5 min时,B中共收集到224 mL(标准状况)气体,B中阳极发生的电极反应式___ 。溶液体积为200 mL(电解前后溶液的体积变化忽略不计),则通电前c(CuSO4)=______ 。
(3)若A中KCl溶液的体积也是200 mL,电解后溶液中仍有Cl-,则电解5 min后,共产生气体的体积为(标准状况)___ ,此时溶液c(OH-)=_____ 。

(1)电源中Y极是
(2)通电5 min时,B中共收集到224 mL(标准状况)气体,B中阳极发生的电极反应式
(3)若A中KCl溶液的体积也是200 mL,电解后溶液中仍有Cl-,则电解5 min后,共产生气体的体积为(标准状况)
18-19高二下·江苏无锡·期中 查看更多[3]
(已下线)【浙江新东方】【2020】【高二上】【期中】【HD-LP406】【化学】黑龙江省哈尔滨师范大学青冈实验中学校2019-2020学年高二上学期开学考试(8月)化学试题江苏省江阴市第一中学2018-2019学年高二下学期期中考试化学试题
更新时间:2019-04-29 17:05:21
|
相似题推荐
填空题
|
较难
(0.4)
解题方法
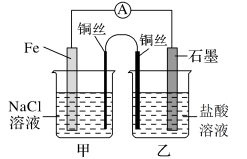
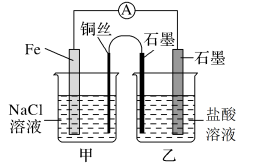
【推荐1】某化学兴趣小组同学对电化学原理进行了一系列探究活动。
(1)如图,为某化学兴趣小组依据氧化还原反应:___________ (用离子方程式表示)设计的原电池装置,当导线中通过0.5mol电子的电量时,理论上石墨电极上产生气体体积为___________ L(标准状况下)。

(2)该实验小组的同学发现,用吸管吸出铁片附近溶液少许置于试管中,滴加几滴酚酞试剂,溶液变红,针对这一现象,某同学的假设是:铁电极材料不纯(材料中含有碳杂质),所以发生了___________ 腐蚀(填“吸氧”或“析氢”),试写出使酚酞溶液变红的电极反应式为___________ 。
(3)如图其他条件不变,若将盐桥换成n型铜丝,一段时间后,乙装置中石墨为___________ 极(填“正”、“负”、“阴”或“阳”),乙装置中总反应的离子方程式为___________ ,该反应为___________ (填“自发”或“非自发”)的氧化还原反应。___________ ,产物常用___________ 检验,一段时间后,乙装置中溶液pH___________ (填“变大”、“变小”或“不变”)。
(1)如图,为某化学兴趣小组依据氧化还原反应:

(2)该实验小组的同学发现,用吸管吸出铁片附近溶液少许置于试管中,滴加几滴酚酞试剂,溶液变红,针对这一现象,某同学的假设是:铁电极材料不纯(材料中含有碳杂质),所以发生了
(3)如图其他条件不变,若将盐桥换成n型铜丝,一段时间后,乙装置中石墨为
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐2】酸性锌锰干电池是一种一次电池,外壳为金属锌,中间是碳棒,其周围是碳粉,MnO2,ZnCl2和NH4Cl等组成的糊状填充物,该电池在放电过程产生MnOOH,回收处理该废电池可得到多种化工原料,有关数据如表所示:
溶解度/(g/100g水)
溶度积常数
回答下列问题:
(1)该电池的正极反应式为______ ,电池反应的离子方程式为____
(2)维持电流强度为0.5A,电池工作五分钟,理论上消耗Zn_____ g。(已经F=96500C/mol)
(3)废电池糊状填充物加水处理后,过滤,滤液中主要有ZnCl2和NH4Cl,二者可通过____ 分离回收;滤渣的主要成分是MnO2、______ 和______ ,欲从中得到较纯的MnO2,最简便的方法是_____________ ,其原理是_______ 。
溶解度/(g/100g水)
| 0 | 20 | 40 | 60 | 80 | 100 | |
| NH4Cl | 29.3 | 37.2 | 45.8 | 55.3 | 65.6 | 77.3 |
| ZnCl2 | 343 | 395 | 452 | 488 | 541 | 614 |
溶度积常数
| 化合物 | Zn(OH)2 | Fe(OH)2 | Fe(OH)3 |
| Ksp近似值 | 10-17 | 10-17 | 10-39 |
回答下列问题:
(1)该电池的正极反应式为
(2)维持电流强度为0.5A,电池工作五分钟,理论上消耗Zn
(3)废电池糊状填充物加水处理后,过滤,滤液中主要有ZnCl2和NH4Cl,二者可通过
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
解题方法
【推荐3】A、B、C三种强电解质,它们在水中电离出的离子如表所示:
如图1所示的装置中,甲、乙、丙三个烧杯依次分别盛放足量的A溶液、足量的B溶液、足量的C溶液,电极均为石墨电极,接通电源,经过一段时间后,测得乙烧杯中电极c质量增加32g。常温下各烧杯中溶液的pH与电解时间t的关系如图2。据此回答下列问题:
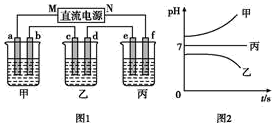
(1)M为电源的______ 极(填写“正”或“负”),电极b上发生的电极反应为_______ ;
(2)电极e上生成的气体在标准状态下的体积为:______ ;
(3)写出乙烧杯的电解池反应______ ;
(4)若要使丙恢复到原来的状态,正确的操作是______ 。
| 阳离子 | Na+、K+、Cu2+ |
| 阴离子 | SO42−、OH− |
如图1所示的装置中,甲、乙、丙三个烧杯依次分别盛放足量的A溶液、足量的B溶液、足量的C溶液,电极均为石墨电极,接通电源,经过一段时间后,测得乙烧杯中电极c质量增加32g。常温下各烧杯中溶液的pH与电解时间t的关系如图2。据此回答下列问题:

(1)M为电源的
(2)电极e上生成的气体在标准状态下的体积为:
(3)写出乙烧杯的电解池反应
(4)若要使丙恢复到原来的状态,正确的操作是
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐1】锂系电池包括锂电池和锂离子电池,锂电池是一类由锂金属或锂合金为正/负极材料、使用非水电解质溶液的电池。1912年锂金属电池最早由GilbertN。Lewis提出并研究。20世纪70年代时,M。S。Whittingham提出并开始研究锂离子电池。
(1)全固态锂离子电池放电时电池发生反应: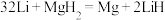 ,写出充电时,阴极反应式为
,写出充电时,阴极反应式为___________ 。
(2)上述锂离子电池可用于电解精炼法提纯镓,具体原理如图所示。
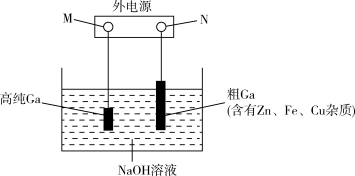
已知:金属活动性强弱顺序为:Zn>Ga>Fe>Cu,镓的化学性质与铝相似。
①M为电源的___________ 极,电解精炼镓时产生的,阳极泥的主要成分是___________ 。
②电解过程中阳极产生的离子迁移到阴极并在NaOH溶液阴极析出高纯镓。请写出电解过程中阴极析出高纯镓的电极反应式___________ 。
③电解过程中需控制合适的电压,若电压太高,阴极会产生H2导致电解效率下降。若外电路通过 ,阴极得到3.5g的镓,则该电解装置的电解效率η=
,阴极得到3.5g的镓,则该电解装置的电解效率η=___________ (η=生成目标产物消耗的电子数÷转移的电子总数)。
(3)上述锂离子电池也可用于氢碘酸“电解法”制备,装置下图所示。其中双极膜(BPM)是阴、阳复合膜,在直流电的作用下,阴、阳膜复合层间的H2O解离成 和
和 ;A、B为离子交换膜。B膜最佳应选择
;A、B为离子交换膜。B膜最佳应选择___________ 。少量的 因浓度差通过BPM膜,若撤去A膜,其缺点是
因浓度差通过BPM膜,若撤去A膜,其缺点是___________ 。

(1)全固态锂离子电池放电时电池发生反应:
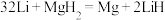 ,写出充电时,阴极反应式为
,写出充电时,阴极反应式为(2)上述锂离子电池可用于电解精炼法提纯镓,具体原理如图所示。

已知:金属活动性强弱顺序为:Zn>Ga>Fe>Cu,镓的化学性质与铝相似。
①M为电源的
②电解过程中阳极产生的离子迁移到阴极并在NaOH溶液阴极析出高纯镓。请写出电解过程中阴极析出高纯镓的电极反应式
③电解过程中需控制合适的电压,若电压太高,阴极会产生H2导致电解效率下降。若外电路通过
 ,阴极得到3.5g的镓,则该电解装置的电解效率η=
,阴极得到3.5g的镓,则该电解装置的电解效率η=(3)上述锂离子电池也可用于氢碘酸“电解法”制备,装置下图所示。其中双极膜(BPM)是阴、阳复合膜,在直流电的作用下,阴、阳膜复合层间的H2O解离成
 和
和 ;A、B为离子交换膜。B膜最佳应选择
;A、B为离子交换膜。B膜最佳应选择 因浓度差通过BPM膜,若撤去A膜,其缺点是
因浓度差通过BPM膜,若撤去A膜,其缺点是
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
解题方法
【推荐2】请回答下列问题:
(1)已知水存在如下平衡:H2O⇌H++OH- △H﹥0,现欲使平衡向右移动,且所得溶液显酸性,选择的下列方法是_____。
(2)物质的量浓度相同的①NaOH②H2SO4③CH3COOH④NaCl⑤CH3COONa⑥(NH4)2SO4六种稀溶液中,水电离的OH-浓度由大到小的顺序_____ (填序号)
(3)25℃时,向水的电离平衡体系中加入少量碳酸钠固体,得到pH为11的溶液,其水解方程式为_____ ,由水电离出的c(OH-)=_____ mol·L-1.
(4)MnO2与Li构成LiMnO2,它可作为某锂离子电池的正极材料,电池反应方程式为:Li1-xMnO2+LixC6=LiMnO2+6C,写出该锂离子电池的正极电极反应式_____ 。MnO2可做超级电容器材料,用惰性电极电解MnSO4溶液可制得MnO2,其阳极的电极反应式是_____ 。
(5)已知:H2S的电离常数K1=1.3×10-7,K2=7.0×10-15,在废水处理领域中常用H2S将Mn2+转化为MnS除去,向含有0.020mol·L-1Mn2+废水中通入一定量的H2S气体,调节溶液的pH=a,当HS—浓度为1.0×10-4mol·L-1时,Mn2+开始沉淀,则a=_____ 。[已知:Ksp(MnS)=1.4×10-15]
(1)已知水存在如下平衡:H2O⇌H++OH- △H﹥0,现欲使平衡向右移动,且所得溶液显酸性,选择的下列方法是_____。
| A.向水中加入NaHSO4固体 |
| B.向水中加NaHCO3固体 |
| C.加热至100℃[其中c(H+)=1×10-6mol/L] |
| D.向水中加入NH4Cl固体 |
(3)25℃时,向水的电离平衡体系中加入少量碳酸钠固体,得到pH为11的溶液,其水解方程式为
(4)MnO2与Li构成LiMnO2,它可作为某锂离子电池的正极材料,电池反应方程式为:Li1-xMnO2+LixC6=LiMnO2+6C,写出该锂离子电池的正极电极反应式
(5)已知:H2S的电离常数K1=1.3×10-7,K2=7.0×10-15,在废水处理领域中常用H2S将Mn2+转化为MnS除去,向含有0.020mol·L-1Mn2+废水中通入一定量的H2S气体,调节溶液的pH=a,当HS—浓度为1.0×10-4mol·L-1时,Mn2+开始沉淀,则a=
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐3】能源的开发、利用与人类社会的可持续发展息息相关,充分利用好能源是摆在人类面前的重大课题。如图所示的装置,X、Y都是惰性电极。丙为电解精炼铜的装置。试回答下列问题:
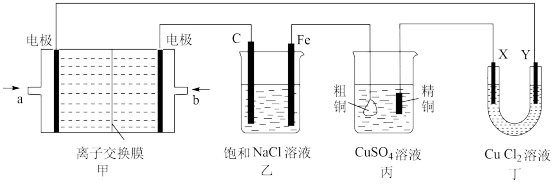
(1)甲装置是甲烷燃料电池(电解质溶液为 溶液)的结构示意图,则a处通入的是
溶液)的结构示意图,则a处通入的是___________ (填“ ”或“
”或“ ”),电极上发生的电极反应是
”),电极上发生的电极反应是___________ 。
(2)在乙装置中,总反应的离子方程式是___________ 。向乙中滴入酚酞溶液,___________ 电极附近溶液先变红(填“C”或“Fe”)。
(3)如果丙装置中精铜电极的质量增加了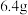 ,则甲装置中消耗的
,则甲装置中消耗的 的质量为
的质量为___________ g。
(4)丁装置中在电解初期,Y电极上发生的电极反应是___________ 。
(5)燃料电池是一种绿色环保、高效的化学电源。若用甲装置电解 硫酸铜溶液,一段时间后:两极共收集到标准状况下的气体
硫酸铜溶液,一段时间后:两极共收集到标准状况下的气体 ,则电路中共转移
,则电路中共转移___________  电子。
电子。

(1)甲装置是甲烷燃料电池(电解质溶液为
 溶液)的结构示意图,则a处通入的是
溶液)的结构示意图,则a处通入的是 ”或“
”或“ ”),电极上发生的电极反应是
”),电极上发生的电极反应是(2)在乙装置中,总反应的离子方程式是
(3)如果丙装置中精铜电极的质量增加了
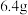 ,则甲装置中消耗的
,则甲装置中消耗的 的质量为
的质量为(4)丁装置中在电解初期,Y电极上发生的电极反应是
(5)燃料电池是一种绿色环保、高效的化学电源。若用甲装置电解
 硫酸铜溶液,一段时间后:两极共收集到标准状况下的气体
硫酸铜溶液,一段时间后:两极共收集到标准状况下的气体 ,则电路中共转移
,则电路中共转移 电子。
电子。
您最近一年使用:0次
填空题
|
较难
(0.4)
解题方法
【推荐1】 2023年7月全球首枚液氧甲烷火箭——朱雀二号在酒泉卫星发射中心发射成功。根据所学知识,回答下列问题:
(1)某科研小组用甲烷燃料电池(电解质溶液为 溶液)提供能量制备
溶液)提供能量制备 ,并获得副产品
,并获得副产品 ,其工作原理如下图所示(已知:电解装置的电极材料分别为金属钴和不锈钢,
,其工作原理如下图所示(已知:电解装置的电极材料分别为金属钴和不锈钢, 是一元弱酸)。
是一元弱酸)。 为
为___________ (填“阳”或“阴”)离子交换膜。
②电解过程中,原料室溶液的
___________ (填“增大”“减小”或“不变”)。
③燃料电池 极的电极反应为
极的电极反应为___________ 。
(1)某科研小组用甲烷燃料电池(电解质溶液为
 溶液)提供能量制备
溶液)提供能量制备 ,并获得副产品
,并获得副产品 ,其工作原理如下图所示(已知:电解装置的电极材料分别为金属钴和不锈钢,
,其工作原理如下图所示(已知:电解装置的电极材料分别为金属钴和不锈钢, 是一元弱酸)。
是一元弱酸)。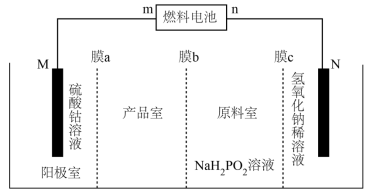
 为
为②电解过程中,原料室溶液的

③燃料电池
 极的电极反应为
极的电极反应为
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐2】回答下列问题
(1)汽车尾气中 生成过程的能量变化如图所示。
生成过程的能量变化如图所示。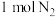 和
和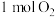 完全反应生成
完全反应生成 会
会_______ (填“吸收”或“放出”)_______ kJ能量。 和
和 组合形成的质子交换膜燃料电池的结构示意图如下图所示:
组合形成的质子交换膜燃料电池的结构示意图如下图所示: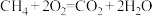 ,则c电极是
,则c电极是 _______ (填“正极”或“负极”),d电极的电极反应式:_______ 。若线路中转移 电子,则上述
电子,则上述 燃料电池消耗的
燃料电池消耗的 在标准状况下的体积为
在标准状况下的体积为_______ L。
(3)一种新型催化用于 和
和 的反应:
的反应: 。已知增大催化剂的表面积可提高该反应速率,为了验证温度、催化剂的比表面积对化学反应速率的影响规律,某同学设计了三组实验,部分条件已经填在下表中。
。已知增大催化剂的表面积可提高该反应速率,为了验证温度、催化剂的比表面积对化学反应速率的影响规律,某同学设计了三组实验,部分条件已经填在下表中。
①请将表中数据补充完整:a=_______ 。
②能验证温度对化学反应速率影响规律的是实验_______ (填序号)。
③实验I和实验II中, 的物质的量浓度
的物质的量浓度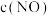 随时间
随时间 的变化曲线如图所示,其中表示实验II的是曲线
的变化曲线如图所示,其中表示实验II的是曲线 _______ (填“甲”或“乙”)。
(1)汽车尾气中
 生成过程的能量变化如图所示。
生成过程的能量变化如图所示。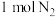 和
和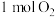 完全反应生成
完全反应生成 会
会
 和
和 组合形成的质子交换膜燃料电池的结构示意图如下图所示:
组合形成的质子交换膜燃料电池的结构示意图如下图所示:
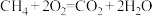 ,则c电极是
,则c电极是  电子,则上述
电子,则上述 燃料电池消耗的
燃料电池消耗的 在标准状况下的体积为
在标准状况下的体积为(3)一种新型催化用于
 和
和 的反应:
的反应: 。已知增大催化剂的表面积可提高该反应速率,为了验证温度、催化剂的比表面积对化学反应速率的影响规律,某同学设计了三组实验,部分条件已经填在下表中。
。已知增大催化剂的表面积可提高该反应速率,为了验证温度、催化剂的比表面积对化学反应速率的影响规律,某同学设计了三组实验,部分条件已经填在下表中。| 实验编号 | T/℃ | NO初始浓度/(mol∙L-1) | CO初始浓度/(mol∙L-1) | 催化剂的比表面积 (m2∙g-1) |
| I | 280 |  |  | 82 |
| II | 280 |  |  | 124 |
| III | 350 |  |  | 82 |
②能验证温度对化学反应速率影响规律的是实验
③实验I和实验II中,
 的物质的量浓度
的物质的量浓度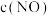 随时间
随时间 的变化曲线如图所示,其中表示实验II的是曲线
的变化曲线如图所示,其中表示实验II的是曲线 
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
解题方法
【推荐3】在电化学中,离子交换膜扮演了非常重要的角色,其中阴(阳)离子交换膜只允许阴(阳)离子通过的特性,往往有很多新奇的应用。

(1)用图一装置电解Na2SO4溶液。m、n分别为___ 、___ 离子交换膜(填“阳”或“阴”)。A、D口产品的化学式分别是A__ 、D__ (H2O除外),整个装置中的总反应方程式为__ 。
(2)电渗析法是近年发展起来的一种较好的海水淡化技术,其原理如图二。

①比较出水口的NaCl溶液浓度:b__ c(填“>、<或=”)。
②海水中含有较多的Ca2+和Mg2+,淡化过程中,__ 口对应的室会产生较多的水垢(填a、b、c、d、e)。

(1)用图一装置电解Na2SO4溶液。m、n分别为
(2)电渗析法是近年发展起来的一种较好的海水淡化技术,其原理如图二。

①比较出水口的NaCl溶液浓度:b
②海水中含有较多的Ca2+和Mg2+,淡化过程中,
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
解题方法
【推荐1】如图1所示,某同学设计了一个燃料电池并探究氯碱工业原理和粗铜的精炼原理,其中乙烧杯中X为阳离子交换膜。请按要求回答相关问题:
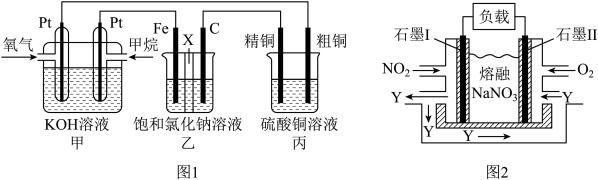
(1)甲烷燃料电池负极电极反应式是___________ ;正极电极反应式是___________________
(2)石墨(C)为__________ 极,其电极反应式为____________________________ ;乙中总反应的离子方程式为__________________________________________________
(3)若在标准状况下,有2.24 L氧气参加反应,则丙装置中阴极析出铜的质量为_________ g ;
(4)若将甲装置中的甲烷换成甲醇(CH3OH),KOH溶液换成稀硫酸,则负极电极反应式为___________ ,消耗等量氧气时,需要甲烷与甲醇的物质的量之比为_________ 。
(5)NO2、O2和熔融NaNO3可制作燃料电池,其原理见图2,该电池在使用过程中石墨I电极上生成氧化物Y,其电极反应式为________________________________

(1)甲烷燃料电池负极电极反应式是
(2)石墨(C)为
(3)若在标准状况下,有2.24 L氧气参加反应,则丙装置中阴极析出铜的质量为
(4)若将甲装置中的甲烷换成甲醇(CH3OH),KOH溶液换成稀硫酸,则负极电极反应式为
(5)NO2、O2和熔融NaNO3可制作燃料电池,其原理见图2,该电池在使用过程中石墨I电极上生成氧化物Y,其电极反应式为
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
解题方法
【推荐2】新型高效的甲烷燃料电池采用铂为电极材料,两电极上分别通入CH4和O2 ,电解质为KOH溶液。某研究小组将两个甲烷燃料电池串联后作为电源,进行饱和氯化钠溶液电解实验,如图所示。
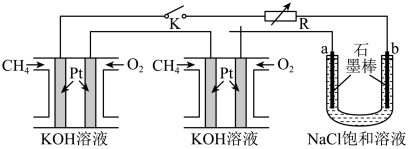
回答下列问题:
(1)闭合K开关后,a、b电极上均有气体产生。其中b电极为___________ 极(填“阴”或“阳”),得到的气体是___________ ,电解一段时间后,附近溶液的pH ___________ (填“升高”、“降低”、“不变”),要使溶液复原,应向溶液中加入 ___________ ,电解氯化钠溶液的总反应方程式为___________ 。如把氯化钠饱和溶液换成熔融氯化钠,则该池的总反应方程式为___________ 。
(2)甲烷燃料电池负极的电极反应为___________ 。
(3)若每个电池甲烷通入量为4.48 L(标准状况),且反应完全,则理论上通过电解池的电子数目为___________ (标准状况)。

回答下列问题:
(1)闭合K开关后,a、b电极上均有气体产生。其中b电极为
(2)甲烷燃料电池负极的电极反应为
(3)若每个电池甲烷通入量为4.48 L(标准状况),且反应完全,则理论上通过电解池的电子数目为
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐3】辉铜矿是冶炼铜的重要原料。
(1)工业上冶炼粗铜的某种反应为:Cu2S+O2=2Cu+SO2①当产生标况下11.2L气体时,转移电子数目为__________ ;
②将粗铜进行电解精炼,粗铜应与外电源的____________ 极相接;若精炼某种仅含杂质锌的粗铜,通电一段时间后测得阴极增重ag,电解质溶液增重bg,则粗铜中含锌的质量分数为________________ ;
(2)将辉铜矿、软锰矿做如下处理,可以制得碱式碳酸铜:
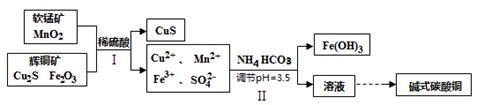
① 步骤I中用稀硫酸浸取矿石,为提高浸取率可采取的措施有_____ (任写一种)。
② 步骤Ⅱ中调节浸出液pH=3.5的作用是______________________________ ;
③ 步骤Ⅰ中发生如下3个反应,已知反应Ⅰ中生成的硫酸铁起催化作用。请写出反应Ⅲ的化学方程式。
Ⅰ.Fe2O3+3H2SO4 = Fe2(SO4)3+3H2O
Ⅱ.Cu2S+ Fe2(SO4)3 = CuSO4+CuS+2FeSO4
Ⅲ.___________________________________ 。
④步骤Ⅱ中,碳酸氢铵参与反应的离子方程式为_______________________ 。
(1)工业上冶炼粗铜的某种反应为:Cu2S+O2=2Cu+SO2①当产生标况下11.2L气体时,转移电子数目为
②将粗铜进行电解精炼,粗铜应与外电源的
(2)将辉铜矿、软锰矿做如下处理,可以制得碱式碳酸铜:

① 步骤I中用稀硫酸浸取矿石,为提高浸取率可采取的措施有
② 步骤Ⅱ中调节浸出液pH=3.5的作用是
③ 步骤Ⅰ中发生如下3个反应,已知反应Ⅰ中生成的硫酸铁起催化作用。请写出反应Ⅲ的化学方程式。
Ⅰ.Fe2O3+3H2SO4 = Fe2(SO4)3+3H2O
Ⅱ.Cu2S+ Fe2(SO4)3 = CuSO4+CuS+2FeSO4
Ⅲ.
④步骤Ⅱ中,碳酸氢铵参与反应的离子方程式为
您最近一年使用:0次



