按照题目要求完成下列离子方程式
(1)在AgCl沉淀中加入KBr溶液,白色沉淀转化为淡黄色沉淀,写出反应的离子方程式:_____________________________ 。
(2)含氯消毒剂可防甲型H1N1流感。二氧化氯是目前国际上公认的第四代高效、无毒的广谱消毒剂,它可由KClO3在H2SO4存在下与Na2SO3反应制得。请写出反应的离子方程式:_______________________________ 。
(3)FeCl3溶液腐蚀钢铁设备,除H+作用外,另一主要原因是(用离子方程式表示)_________________________________ 。
(4)化学反应多姿多彩,把SO2通入硝酸铁溶液中,溶液由棕黄色变为浅绿色,但立即又变为棕黄色,此时向溶液中滴加氯化钡溶液,有白色沉淀产生。请写出上述变化中溶液由棕黄色变为浅绿色,但立即又变为棕黄色所涉及的两个离子方程式:____________________________ 。
(1)在AgCl沉淀中加入KBr溶液,白色沉淀转化为淡黄色沉淀,写出反应的离子方程式:
(2)含氯消毒剂可防甲型H1N1流感。二氧化氯是目前国际上公认的第四代高效、无毒的广谱消毒剂,它可由KClO3在H2SO4存在下与Na2SO3反应制得。请写出反应的离子方程式:
(3)FeCl3溶液腐蚀钢铁设备,除H+作用外,另一主要原因是(用离子方程式表示)
(4)化学反应多姿多彩,把SO2通入硝酸铁溶液中,溶液由棕黄色变为浅绿色,但立即又变为棕黄色,此时向溶液中滴加氯化钡溶液,有白色沉淀产生。请写出上述变化中溶液由棕黄色变为浅绿色,但立即又变为棕黄色所涉及的两个离子方程式:
18-19高二·全国·假期作业 查看更多[2]
更新时间:2019/05/24 14:39:38
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】实验室有如下物质:①NaHSO4 ②NH4HCO3 ③BaCO3 ④CuSO4 ⑤饱和氯化铁溶液 ⑥CO2 ⑦CH3COOH ⑧稀盐酸。溶液回答下列问题:
(1)某同学将②③④归为一类,他的分类依据是_______ 。
A.都属于酸式盐 B.都属于盐 C.都易溶于水
(2)以上物质属于非电解质的有_______ (填编号,下同),能导电的有_______ 。
(3)写出①在水中的电离方程式_______ 。
(4)向BaCO3固体中滴加过量稀盐酸,写出反应的离子方程式_______ 。
(5)向NaHSO4溶液中滴加Ba(OH)2溶液至中性,写出反应的离子方程式_______ 。
(1)某同学将②③④归为一类,他的分类依据是
A.都属于酸式盐 B.都属于盐 C.都易溶于水
(2)以上物质属于非电解质的有
(3)写出①在水中的电离方程式
(4)向BaCO3固体中滴加过量稀盐酸,写出反应的离子方程式
(5)向NaHSO4溶液中滴加Ba(OH)2溶液至中性,写出反应的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】按要求填空:
Ⅰ.初步 分离或提纯下列各组物质,应选用方法的哪一种?(填选项字母)
A. 萃取 B. 加热 C. 重结晶 D. 分液 E. 过滤 F. 蒸馏
(1)除去食盐水中的泥沙__________
(2)从含有少量氯化钠的硝酸钾溶液中提取硝酸钾__________
(3)分离水和汽油___________
(4)分离 CCl4 (沸点为76.75℃)和甲苯(沸点为110.6℃)的液体混合物___________
(5)从溴水中提取溴单质_________
Ⅱ.用离子方程式解释以下实验现象
(1)少量的SO2气体能够使NaAlO2溶液产生浑浊:______________________________________
(2)稀硝酸无需加热就能腐蚀铜片:__________________________________________________
Ⅰ.
A. 萃取 B. 加热 C. 重结晶 D. 分液 E. 过滤 F. 蒸馏
(1)除去食盐水中的泥沙
(2)从含有少量氯化钠的硝酸钾溶液中提取硝酸钾
(3)分离水和汽油
(4)分离 CCl4 (沸点为76.75℃)和甲苯(沸点为110.6℃)的液体混合物
(5)从溴水中提取溴单质
Ⅱ.用离子方程式解释以下实验现象
(1)少量的SO2气体能够使NaAlO2溶液产生浑浊:
(2)稀硝酸无需加热就能腐蚀铜片:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】向BaCl2溶液中通入SO2后,将溶液分置于两支试管中。向一份中通入NH3气体,出现白色沉淀A;另一份通入少量Cl2,产生白色沉淀B。已知硝酸具有强氧化性。试回答下列问题:
(1)向BaCl2溶液中通入SO2气体无明显现象,“无明显现象”可能是“不反应”,也可能是“反应但无现象”。此处应为_____________ ,原因是_____________ 。
(2)沉淀A的化学式为________ ,该沉淀能否溶于稀盐酸?________ 。
(3)写出通入少量Cl2,生成沉淀B的离子方程式:_________________________ 。
(4)生成2.33 g沉淀B,理论上需要消耗标准状况下的Cl2________ mL。
(5)常温下,若将SO2通入BaCl2溶液至饱和,再通入下列某些气体也有沉淀生成,则该气体可能是__________
A.CO2 B.H2S C.NO与O2混合气体 D.SO3
(6)若将BaCl2溶液换成Ba(OH)2溶液
①少量SO2通入到Ba(OH)2溶液中的离子反应方程式为
______________________________________________________ ,
②过量的SO2通入到Ba(OH)2溶液中的离子反应方程式为
______________________________________________________ 。
③少量Cl2通入到Ba(OH)2溶液中的离子反应方程式为
______________________________________________________ ,
(1)向BaCl2溶液中通入SO2气体无明显现象,“无明显现象”可能是“不反应”,也可能是“反应但无现象”。此处应为
(2)沉淀A的化学式为
(3)写出通入少量Cl2,生成沉淀B的离子方程式:
(4)生成2.33 g沉淀B,理论上需要消耗标准状况下的Cl2
(5)常温下,若将SO2通入BaCl2溶液至饱和,再通入下列某些气体也有沉淀生成,则该气体可能是
A.CO2 B.H2S C.NO与O2混合气体 D.SO3
(6)若将BaCl2溶液换成Ba(OH)2溶液
①少量SO2通入到Ba(OH)2溶液中的离子反应方程式为
②过量的SO2通入到Ba(OH)2溶液中的离子反应方程式为
③少量Cl2通入到Ba(OH)2溶液中的离子反应方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】请根据要求回答问题:现有以下物质:①NaOH溶液;②液氨;③BaCO3固体;④熔融KHSO4;⑤Fe(OH)3胶体;⑥铜;⑦CO2;⑧CH3COOH;⑨蔗糖;
请回答下列问题:
(1)以上物质中属于电解质的是___________ (填序号);属于非电解质的是___________ (填序号);能导电的是___________ (填序号)。
(2)写出④的电离方程式___________ 。
(3)在①溶液中缓缓通入过量的CO2可生成酸式盐,写出该反应的离子方程式___________ 。
(4)⑥和⑦在潮湿的空气中反应生成一种新物质——碱式碳酸铜[Cu2(OH)2CO3],请写出该反应的化学方程式____________ 。
请回答下列问题:
(1)以上物质中属于电解质的是
(2)写出④的电离方程式
(3)在①溶液中缓缓通入过量的CO2可生成酸式盐,写出该反应的离子方程式
(4)⑥和⑦在潮湿的空气中反应生成一种新物质——碱式碳酸铜[Cu2(OH)2CO3],请写出该反应的化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】实验室制备Cl2有三种常用方法:
a.MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O
b. KMnO4+
KMnO4+ HCl(浓)=
HCl(浓)= KCl+
KCl+ MnCl2+
MnCl2+ Cl2↑+
Cl2↑+ H2O
H2O
c.KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O
(1)常温下,医用酒精、Cl2、KMnO4、MnCl2、浓盐酸中能导电的是______ ,属于混合物的是______ ,属于电解质的是______ 。
(2)写出反应c对应的离子方程式:______ [已知HCl(浓)可拆分为H+和Cl-]。
(3)配平反应b的方程式______ 。
(4)当三个反应中参与反应的HCl的质量相同时,得到Cl2的质量最多的是反应______ (填“a”“b”或“c”,下同);当得到等质量的Cl2时,消耗HCl的质量最多的是反应______ 。
a.MnO2+4HCl(浓)
 MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2Ob.
 KMnO4+
KMnO4+ HCl(浓)=
HCl(浓)= KCl+
KCl+ MnCl2+
MnCl2+ Cl2↑+
Cl2↑+ H2O
H2Oc.KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O
(1)常温下,医用酒精、Cl2、KMnO4、MnCl2、浓盐酸中能导电的是
(2)写出反应c对应的离子方程式:
(3)配平反应b的方程式
(4)当三个反应中参与反应的HCl的质量相同时,得到Cl2的质量最多的是反应
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】N2O、NO和NO2等氮氧化物是空气污染物,为保护环境,含有氮氧化物的尾气需处理后才能排放。回答下列问题:
(1)N2O的处理。N2O是硝酸生产中氨催化氧化的副产物,用特种催化剂能使N2O分解。NH3与O2在加热和催化剂作用下生成N2O的化学方程式为___________ 。
(2)NO和NO2的处理。已除去N2O的硝酸尾气可用NaOH浓溶液吸收,主要离子反应为:i. ;ii.
;ii.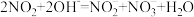 。
。
①下列措施能提高尾气中NO和NO2去除率的有___________ (填字母)。
A.加快通入尾气的速率
B.采用气、液逆流的方式吸收尾气
C.吸收尾气过程中定期补加适量NaOH浓溶液
D.用Ca(OH)2饱和溶液代替NaOH浓溶液
②吸收后的溶液经浓缩、结晶、过滤,得到O2晶体,该晶体中的主要杂质是___________ (填化学式,下同);吸收后的尾气中可能仍含有的氮氧化物是___________ 。
(3)NO的吸收。在某钒催化剂中添加一定量Cu2O可加快NO的脱除效率,其可能机理如图所示(表示物种吸附在催化剂表面,部分物种未画出)。
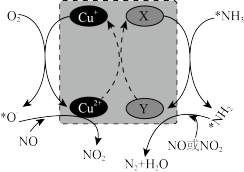
①X、Y处钒元素化合价为+4或+5。X处钒元素化合价为___________ 。
②写出在催化剂作用下NO与NH3反应的化学方程式:___________ ,上述反应中生成2.5molN2时,转移电子的物质的量为___________ 。
(1)N2O的处理。N2O是硝酸生产中氨催化氧化的副产物,用特种催化剂能使N2O分解。NH3与O2在加热和催化剂作用下生成N2O的化学方程式为
(2)NO和NO2的处理。已除去N2O的硝酸尾气可用NaOH浓溶液吸收,主要离子反应为:i.
 ;ii.
;ii.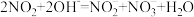 。
。①下列措施能提高尾气中NO和NO2去除率的有
A.加快通入尾气的速率
B.采用气、液逆流的方式吸收尾气
C.吸收尾气过程中定期补加适量NaOH浓溶液
D.用Ca(OH)2饱和溶液代替NaOH浓溶液
②吸收后的溶液经浓缩、结晶、过滤,得到O2晶体,该晶体中的主要杂质是
(3)NO的吸收。在某钒催化剂中添加一定量Cu2O可加快NO的脱除效率,其可能机理如图所示(表示物种吸附在催化剂表面,部分物种未画出)。

①X、Y处钒元素化合价为+4或+5。X处钒元素化合价为
②写出在催化剂作用下NO与NH3反应的化学方程式:
您最近一年使用:0次



