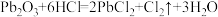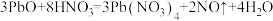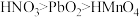下列根据实验操作和现象所得出的结论错误的是( )
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 取久置的Na2O2粉末,向其中滴加过量的盐酸 | 产生无色气体 | Na2O2没有完全变质 |
| B | ①将少量的溴水滴入FeCl2、NaI的混合溶液中,再滴加CCl4,振荡、静置,向上层溶液中滴加KSCN溶液。 ②再向上层溶液中滴加溴水 | 实验现象1: 上层溶液不变红,下层溶液呈紫红色 实验现象2: 上层溶液变红 | 氧化性:Br2>Fe3+>I2 |
| C | 将一片铝箔置于酒精灯外焰上灼烧 | 铝箔熔化但不滴落 | 铝箔表面有致密Al2O3薄膜,且Al2O3熔点高于Al的 |
| D | 取久置的绿矾(FeSO4·7H2O)溶于水,加入KSCN溶液 | 溶液变为红色 | 绿矾部分或全部被氧化 |
| A.A | B.B | C.C | D.D |
更新时间:2019-05-21 09:28:16
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】根据以下4个反应:
①H2S+I2=S↓+2I-+2H+, ②SO2+2H2S=3S+2H2O,
③2I-+Br2=I2+2Br-, ④SO2+I2+2H2O=H2SO4+2HI。
确定Br-、I-、H2S、SO2的还原性由强到弱的顺序是
①H2S+I2=S↓+2I-+2H+, ②SO2+2H2S=3S+2H2O,
③2I-+Br2=I2+2Br-, ④SO2+I2+2H2O=H2SO4+2HI。
确定Br-、I-、H2S、SO2的还原性由强到弱的顺序是
| A.H2S>SO2>I->Br- | B.I->Br->SO2>H2S |
| C.H2S>I->Br-> SO2 | D.I->Br->H2S>SO2 |
您最近半年使用:0次
【推荐2】氮及其化合物在工农业生产和生命活动中起着重要的作用,一种利用电化学制备NH3的转化历程如图所示。下列说法错误的是
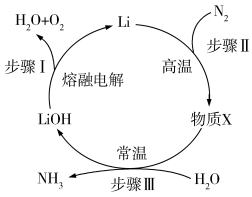

| A.步骤Ⅱ属于氮的固定 |
| B.LiOH可视为该历程中的催化剂 |
| C.该历程总反应为2N2+6H2O=4NH3+3O2 |
| D.由该历程说明N2的氧化性强于O2 |
您最近半年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】下列实验方案中,实验设计不恰当的是
| 选项 | A | B | C | D |
| 实验装置 |  |  | 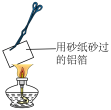 | 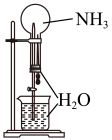 |
| 实验目的 | 制取蒸馏水 | 鉴别 和 和 | 证明氧化铝熔点高于铝 | 喷泉实验 |
| A.A | B.B | C.C | D.D。 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列现象或事实、解释都正确的是 ( )
| 选项 | 现象或事实 | 解释 |
| A | 将SO2通入溴水,溴水褪色 | SO2具有漂白性 |
| B | 加热用砂纸打磨过的铝箔,铝箔熔化但不滴落 | Al2O3的熔点高于Al |
| C | 古代青铜器表面有铜锈,可放入盐酸中浸泡除锈 | 铜锈是铜在空气中缓慢氧化生成的氧化物,可溶于盐酸 |
| D | 常温下,将铁片浸入足量的浓硫酸中,铁片不溶解 | 常温下,铁与浓硫酸没有发生化学反应 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐1】下列有关化学实验的设计合理的是
| A.采用蒸馏的方法分离碘的四氯化碳溶液 |
| B.用氢氟酸清洗做过硅酸分解实验的瓷坩埚 |
| C.H2S 气体通入CuSO4溶液,比较氢硫酸和硫酸的酸性 |
| D.向氯化亚铁溶液中滴加酸性高锰酸钾溶液,证明溶液中含有Fe2+ |
您最近半年使用:0次
【推荐2】下列离子常用“气体法”检验的是
A. | B. | C. | D. |
您最近半年使用:0次
【推荐3】根据下列实验操作和现象所得出的结论错误的是( )
| 选项 | 操作 | 现象 | 结论 |
| A | 向蔗糖中加入浓硫酸 | 蔗糖变成疏松多孔的海绵状炭,并放出有刺激性气味的气体 | 浓硫酸具有脱水性和强氧化性 |
| B | 向盛有 溶液的试管中加入几滴酸化的硫酸亚铁溶液 溶液的试管中加入几滴酸化的硫酸亚铁溶液 | 溶液变成棕黄色,一段时间后溶液中出现气泡,随后有红褐色沉淀生成 |  催化 催化 分解产生 分解产生 , , 分解反应放热,促进 分解反应放热,促进 的水解 的水解 |
| C | 将 通入紫色石蕊试液中 通入紫色石蕊试液中 | 溶液变红 |  与水反应生成 与水反应生成 使溶液显酸性 使溶液显酸性 |
| D | 向久置的 溶液中加入足量 溶液中加入足量 溶液,再加入足量稀盐酸 溶液,再加入足量稀盐酸 | 先出现白色沉淀,后部分沉淀溶解 | 部分 被氧化 被氧化 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次

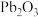 与
与 溶液发生反应I:
溶液发生反应I: ,
, 与酸化的
与酸化的 溶液发生反应II:
溶液发生反应II: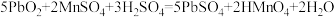 ,下列说法正确的是
,下列说法正确的是