将足量铁投入到200mLH2SO4和CuSO4的混和溶液中,充分反应后,产生H21.12L(标准状况),铁块的质量减轻了1.2g。求原溶液中c(H2SO4)及c(CuSO4)。(假设反应前后溶液的体积不变)
11-12高一上·湖南·期中 查看更多[2]
更新时间:2016-12-09 02:18:56
|
相似题推荐
计算题
|
较易
(0.85)
名校
解题方法
【推荐1】现有m g某气体,它由双原子分子构成,它的摩尔质量为M g/mol。若阿伏加德罗常数用NA表示,则:
(1)该气体的物质的量为________ mol。
(2)该气体所含原子总数为__________ 个。
(3)该气体在标准状况下的体积为____________ L。
(4)该气体溶于1 L水中(不考虑反应),其溶液中溶质的质量分数为___________ 。
(5)该气体溶于水后形成V L溶液,其溶液的物质的量浓度为_______ mol/L。
(1)该气体的物质的量为
(2)该气体所含原子总数为
(3)该气体在标准状况下的体积为
(4)该气体溶于1 L水中(不考虑反应),其溶液中溶质的质量分数为
(5)该气体溶于水后形成V L溶液,其溶液的物质的量浓度为
您最近一年使用:0次
计算题
|
较易
(0.85)
解题方法
【推荐2】实验室可以用高锰酸钾和浓盐酸反应制取氯气,反应的化学方程式如下:2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O。将15.8gKMnO4与足量的浓盐酸充分反应,产生气体的体积均在标准状况下测定,请计算:
(1)高锰酸钾的物质的量是___ mol。
(2)产生的Cl2的体积是___ L。
(3)若用MnO2与足量的浓盐酸反应制取相同体积的Cl2,理论上需要MnO2的质量是___ 克。
(1)高锰酸钾的物质的量是
(2)产生的Cl2的体积是
(3)若用MnO2与足量的浓盐酸反应制取相同体积的Cl2,理论上需要MnO2的质量是
您最近一年使用:0次
计算题
|
较易
(0.85)
名校
【推荐3】(1)标准状况下,与5.6L的CH4气体含相同H原子数的硫化氢的质量为___ g。
(2)将2mol·L-1Al2(SO4)3和0.2mol·L-1H2SO4溶液等体积混合(设混合溶液体积等于两溶液体积之和),计算混合液中c(SO42-)=__ mol·L-1。若用容量瓶以质量分数为98%、密度为1.84g/cm3的浓硫酸,配制480mL浓度成0.2mol·L-1 稀硫酸,计算需要量取____ mL的浓硫酸。
(3)配平以下方程式___
___K2Cr2O7+___HCl=___KCl+___CrCl3+___Cl2↑+___H2O
上述反应中物质氧化性:___ >__ ,每生成lmolCl2时有__ 个电子发生转移,氧化剂与还原剂的物质的量之比为__ 。
(2)将2mol·L-1Al2(SO4)3和0.2mol·L-1H2SO4溶液等体积混合(设混合溶液体积等于两溶液体积之和),计算混合液中c(SO42-)=
(3)配平以下方程式
___K2Cr2O7+___HCl=___KCl+___CrCl3+___Cl2↑+___H2O
上述反应中物质氧化性:
您最近一年使用:0次
计算题
|
较易
(0.85)
【推荐1】将100mL 0.2mol/L 的盐酸与100mL 0.3 mol/L 的盐酸混合(假设混合时体积变化忽略不计),求
(1)混合后盐酸溶液的物质的量浓度为_____________ ;
(2)若欲将该200mL盐酸溶液浓度重新恢复为0.3mol/L,则需要向其中通入标况下的HCl气体_____________ L(体积变化忽略不计)。
(1)混合后盐酸溶液的物质的量浓度为
(2)若欲将该200mL盐酸溶液浓度重新恢复为0.3mol/L,则需要向其中通入标况下的HCl气体
您最近一年使用:0次
计算题
|
较易
(0.85)
【推荐2】实验室需要配制1 mol·L-1的硫酸100mL,需取用98%的浓硫酸(密度为1.84g·mL-1)______________ mL(保留一位小数)
您最近一年使用:0次
计算题
|
较易
(0.85)
名校
解题方法
【推荐1】将18.6 g铁、锌混合物,加入到200 mL某浓度的稀硫酸中,恰好完全反应,在标准状况下生成氢气6.72 L。求:
(1)混合物中铁的质量_____________ 。
(2)原稀硫酸的物质的量浓度______________ 。
(1)混合物中铁的质量
(2)原稀硫酸的物质的量浓度
您最近一年使用:0次
计算题
|
较易
(0.85)
解题方法
【推荐2】欲测定某生铁 主要成分是铁,还含有少量的碳
主要成分是铁,还含有少量的碳 的组成,进行了如下实验:称取粉末状样品
的组成,进行了如下实验:称取粉末状样品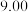 克,加入某浓度的盐酸100mL,充分反应后,收集到标准状况下气体
克,加入某浓度的盐酸100mL,充分反应后,收集到标准状况下气体 ;然后,继续往样品中加入同浓度的盐酸100mL,充分反应后又收集到标准状况下气体
;然后,继续往样品中加入同浓度的盐酸100mL,充分反应后又收集到标准状况下气体 。试求:
。试求: 写出具体计算过程
写出具体计算过程
(1)所取盐酸的物质的量浓度。________
(2)该生铁样品中铁的质量分数 保留3位有效数字
保留3位有效数字 。
。________
 主要成分是铁,还含有少量的碳
主要成分是铁,还含有少量的碳 的组成,进行了如下实验:称取粉末状样品
的组成,进行了如下实验:称取粉末状样品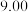 克,加入某浓度的盐酸100mL,充分反应后,收集到标准状况下气体
克,加入某浓度的盐酸100mL,充分反应后,收集到标准状况下气体 ;然后,继续往样品中加入同浓度的盐酸100mL,充分反应后又收集到标准状况下气体
;然后,继续往样品中加入同浓度的盐酸100mL,充分反应后又收集到标准状况下气体 。试求:
。试求: 写出具体计算过程
写出具体计算过程
(1)所取盐酸的物质的量浓度。
(2)该生铁样品中铁的质量分数
 保留3位有效数字
保留3位有效数字 。
。
您最近一年使用:0次
计算题
|
较易
(0.85)
【推荐1】铁粉、铜粉混合物样品11.6g,逐步加入2.0 mol/L的硫酸溶液,充分反应后剩余固体质量随加入硫酸溶液体积变化如下表:
请回答:
(1)样品中铁与铜的物质的量之比n(Fe):n(Cu)=________ 。
(2)反应后的体系中,再加入4.0mol∙L−1的H2O2溶液25.0mL ,并加入足量硫酸溶液,充分反应后溶液中存在的各金属离子的物质的量分别是多少?_________
| 硫酸溶液/mL | 20.0 | 40.0 | 60.0 | 80.0 |
| 剩余固体/g | 9.36 | 7.12 | 4.88 | 3.20 |
(1)样品中铁与铜的物质的量之比n(Fe):n(Cu)=
(2)反应后的体系中,再加入4.0mol∙L−1的H2O2溶液25.0mL ,并加入足量硫酸溶液,充分反应后溶液中存在的各金属离子的物质的量分别是多少?
您最近一年使用:0次
计算题
|
较易
(0.85)
解题方法
【推荐2】将55g铁片放入硫酸铜溶液片刻,取出洗涤干燥后称重,质量为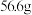 ,求参加反应的铁和生成的铜的质量
,求参加反应的铁和生成的铜的质量___________ 。
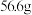 ,求参加反应的铁和生成的铜的质量
,求参加反应的铁和生成的铜的质量
您最近一年使用:0次

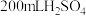 和
和 的混合溶液分成两等份。向其中一份中加入足量铁粉,充分反应后测的固体质量减少
的混合溶液分成两等份。向其中一份中加入足量铁粉,充分反应后测的固体质量减少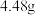 ;向另一份中加入足量
;向另一份中加入足量 溶液,经过滤、洗涤、干燥、称量,得到
溶液,经过滤、洗涤、干燥、称量,得到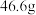 白色沉淀。请计算:
白色沉淀。请计算:
 ;
; 和
和

