现有下列短周期元素的数据(已知Be的原子半径为0.089 nm):
(1)元素⑧在周期表中的位置是_______ ;上述元素中处于同一主族的有______ (用元素符号表示)。
(2)上表中某两种元素形成的共价化合物中,每个原子都满足最外层为8电子的稳定结构,写出其电子式:__________________________ (任写一种)。
(3)元素①和⑥能形成两种化合物,写出其中含共价键的化合物与水反应的离子方程式_________ 。
(4)含锂材料在社会中广泛应用,如各种储氢材料(Li2NH等)、便携式电源材料(LiCoO2等)。根据下列要求回答问题:
①63Li和73Li作核反应堆最佳热载体,73LiH和73LiD用作高温堆减速剂。下列说法正确的是________ (填字母)。
A. 63Li和73Li互为同位素
B.63Li和73Li属于同种核素
C. 73LiH和73LiD的化学性质不同
D. 73LiH和73LiD是同种物质
②下列说法不正确的是_________ (填字母)。
A.碱性:Be(OH)2 < LiOH < NaOH < KOH
B.半径:K > Na > Li > Li+
C.氧化性:Li+ < Na+ < K+ < Rb+ < Cs+
D.金属性:Cs > Rb > K > Na > Li > Be
| ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |
| 原子半径(nm) | 0.074 | 0.160 | 0.152 | 0.110 | 0.099 | 0.186 | 0.075 | 0.082 |
| 最高正化合价 | +2 | +1 | +5 | +7 | +1 | +5 | +3 | |
| 最低负化合价 | −2 | −3 | −1 | −3 |
(2)上表中某两种元素形成的共价化合物中,每个原子都满足最外层为8电子的稳定结构,写出其电子式:
(3)元素①和⑥能形成两种化合物,写出其中含共价键的化合物与水反应的离子方程式
(4)含锂材料在社会中广泛应用,如各种储氢材料(Li2NH等)、便携式电源材料(LiCoO2等)。根据下列要求回答问题:
①63Li和73Li作核反应堆最佳热载体,73LiH和73LiD用作高温堆减速剂。下列说法正确的是
A. 63Li和73Li互为同位素
B.63Li和73Li属于同种核素
C. 73LiH和73LiD的化学性质不同
D. 73LiH和73LiD是同种物质
②下列说法不正确的是
A.碱性:Be(OH)2 < LiOH < NaOH < KOH
B.半径:K > Na > Li > Li+
C.氧化性:Li+ < Na+ < K+ < Rb+ < Cs+
D.金属性:Cs > Rb > K > Na > Li > Be
2019高一下·全国·专题练习 查看更多[1]
(已下线)2019年6月9日 《每日一题》 必修2 每周一测
更新时间:2019-06-05 08:15:37
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】如图为元素周期表的一部分,请参照元素①—⑧在表中的位置,回答问题:
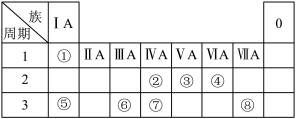
(1)氯元素在周期表中的位置是___________ 。
(2)③④⑦三种元素的原子半径由小到大的顺序为___________ 。(写元素符号)
(3)写出⑤的最高价氧化物对应的水化物与⑥的最高价氧化物反应的离子方程式___________ 。
(4)W是第四周期与④同主族的元素。据此推测W不可能具有的性质是___________(填字母)。
(5)已知X为第IIA族元素(前四周期),其原子序数为a,Y与X位于同一周期,且为第IIIA族元素,写出Y的原子序数
___________ (用含a的代数式表示)。

(1)氯元素在周期表中的位置是
(2)③④⑦三种元素的原子半径由小到大的顺序为
(3)写出⑤的最高价氧化物对应的水化物与⑥的最高价氧化物反应的离子方程式
(4)W是第四周期与④同主族的元素。据此推测W不可能具有的性质是___________(填字母)。
| A.最高化合价为+6 |
B.简单气态氢化物比 稳定 稳定 |
| C.最高价氧化物对应水化物的酸性比硫酸弱 |
| D.单质在常温下可与氢气化合 |
(5)已知X为第IIA族元素(前四周期),其原子序数为a,Y与X位于同一周期,且为第IIIA族元素,写出Y的原子序数

您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】A~M代表元素周期表的部分元素,其相对位置如表所示。回答下列问题:
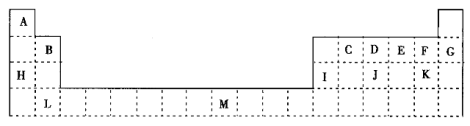
(1)M元素位于元素周期表中的_______ 区;D元素的电子排布式为_______ 。
(2)表中元素电负性最大的是_______ (填元素符号);C、D、F元素的第一电离能的大小顺序为_______ (用元素符号表示)。
(3)D的简单氢化物和J的简单氢化物稳定性更强的是_______ (填化学式)。
(4)A、E、H、J四种元素的原子半径由大到小的排列顺序为_______ (元素符号表示)
(5)H的最高价氧化物的水化物为:_______ (填化学式)。

(1)M元素位于元素周期表中的
(2)表中元素电负性最大的是
(3)D的简单氢化物和J的简单氢化物稳定性更强的是
(4)A、E、H、J四种元素的原子半径由大到小的排列顺序为
(5)H的最高价氧化物的水化物为:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】下表为元素周期表的一部分,请参照元素①-⑧在表中的位置,用化学用语回答下列问题:
(1)写出元素④的原子结构示意图________ ;④、⑤、⑥的原子半径由大到小的顺序为_______ 。
(2)②、③、⑦的最高价含氧酸的酸性由强到弱的顺序是________ 。
(3)①、④、⑤、⑧中的某三种元素可形成既含离子键又含极性共价键的化合物,写出其中一种化合物的化学式:________ 。
(4)写出⑤的最高价氧化物对应的水化物与⑥的最高价氧化物反应的离子方程式:_________ 。
(5)③的最高价氧化物对应的水化物与其气态氢化物反应的离子方程式为________ 。
(6)HNO3的酸性比HClO强,有人据此认为N的非金属性强于Cl,你认为这种看法是否正确,说明理由:__________ 。
| ⅠA | 0 | |||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ||||
(1)写出元素④的原子结构示意图
(2)②、③、⑦的最高价含氧酸的酸性由强到弱的顺序是
(3)①、④、⑤、⑧中的某三种元素可形成既含离子键又含极性共价键的化合物,写出其中一种化合物的化学式:
(4)写出⑤的最高价氧化物对应的水化物与⑥的最高价氧化物反应的离子方程式:
(5)③的最高价氧化物对应的水化物与其气态氢化物反应的离子方程式为
(6)HNO3的酸性比HClO强,有人据此认为N的非金属性强于Cl,你认为这种看法是否正确,说明理由:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】1869年,门捷列夫制得世界上第一张元素周期表,它反映了元素之间的内在联系,是对元素的一种很好的自然分类。如图为现代元素周期表的一部分,请回答下列问题:

(1)在这10种元素中,非金属性最强的元素在周期表中的位置是___________ 。
(2)由a、d、f三种元素形成的化合物属于___________ (填“离子”或“共价”)化合物。
(3)元素b、c形成的简单气态氢化物中较稳定的是___________ (填化学式)。
(4)d、h、i、j的简单离子半径由大到小 的顺序排列为___________ (填离子符号)。
(5)b和d可以形成一种酸性氧化物 ,其电子式为___________ 。
(6)c的最高价氧化物对应水化物的浓溶液与金属Cu反应的离子方程式 为___________ 。

(1)在这10种元素中,非金属性最强的元素在周期表中的位置是
(2)由a、d、f三种元素形成的化合物属于
(3)元素b、c形成的简单气态氢化物中较稳定的是
(4)d、h、i、j的简单离子半径
(5)b和d可以形成一种
(6)c的最高价氧化物对应水化物的浓溶液与金属Cu反应的
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】Q、W、X、Y、Z是原子序数依次增大的短周期元素,X、Y是金属元素,Q、W、Z是非金属元素。五种元素核电荷数之和为54,对应原子最外层电子数之和为20。W、Z最外层电子数相同,但Z的核电荷数是W的2倍。
(1)X、Y各自的最高价氧化物对应的水化物可以发生反应生成盐和水,该反应的离子方程式为______________________________________________________ 。
(2)X与W可形成X2W和X2W2两种化合物,X2W2的电子式为_____________ 。
(3)Q与W可形成化合物QW2,这种化合物固态时属于________ 晶体。
(4)Y的硝酸盐水溶液显________ 性,用离子方程式解释原因___________________ 。
(5)Z的氢化物与W的氢化物发生反应生成Z的单质和水,其化学方程式为_____________________ 。
(6)W、X、Y、Z四种元素原子半径由大到小的顺序是:________ (用元素符号表示)。
(7)0.5 mol Q的单质与足量的W单质完全反应,放出196.75 kJ的热量。写出该反应的热化学方程式:____________________________________________ 。
(1)X、Y各自的最高价氧化物对应的水化物可以发生反应生成盐和水,该反应的离子方程式为
(2)X与W可形成X2W和X2W2两种化合物,X2W2的电子式为
(3)Q与W可形成化合物QW2,这种化合物固态时属于
(4)Y的硝酸盐水溶液显
(5)Z的氢化物与W的氢化物发生反应生成Z的单质和水,其化学方程式为
(6)W、X、Y、Z四种元素原子半径由大到小的顺序是:
(7)0.5 mol Q的单质与足量的W单质完全反应,放出196.75 kJ的热量。写出该反应的热化学方程式:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】元素周期表的形式多种多样,如图是扇形元素周期表的一部分(1~36号元素),对比中学常见元素周期表思考扇形元素周期表的填充规律,并回答下列问题:
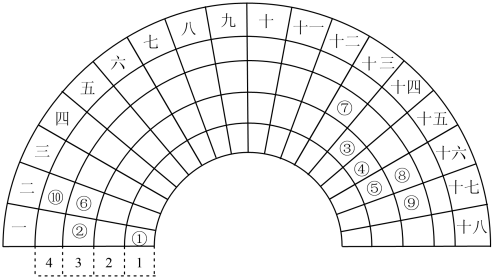
(1)元素⑩在常见周期表中的位置是___________ 。元素⑥的最高价氧化物对应的水化物的电子式为___________ ,用电子式表示元素②、⑧形成化合物的过程___________
(2)元素③、④、⑤形成的简单氢化物,稳定性最强的是___________ (填结构式);元素④、⑧、⑨的最高价氧化物对应的水化物,酸性最强的是___________ (填化学式)
(3)元素⑥、⑦、⑧对应的简单离子的半径由大到小的顺序为___________ (用离子符号表示)。
(4)元素①、⑤和元素①、⑧均能形成18电子的化合物,这两种化合物发生反应可生成一种黄色晶体,其化学方程式为___________ 。
(5)请设计简单实验,比较元素②、⑦的金属性强弱。

(1)元素⑩在常见周期表中的位置是
(2)元素③、④、⑤形成的简单氢化物,稳定性最强的是
(3)元素⑥、⑦、⑧对应的简单离子的半径由大到小的顺序为
(4)元素①、⑤和元素①、⑧均能形成18电子的化合物,这两种化合物发生反应可生成一种黄色晶体,其化学方程式为
(5)请设计简单实验,比较元素②、⑦的金属性强弱。
| 实验步骤 | 实验现象 | 实验结论 |
| 金属性:②>⑦ |
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】A、B、C、D、E、F是原子序数依次增大的短周期主族元素,A元素的原子核内只有1个质子;B元素的原子半径是同族元素原子中最小的,B的最高价氧化物对应水化物的化学式为 ;C元素原子的最外层电子数比次外层多4;C与D可形成化合物
;C元素原子的最外层电子数比次外层多4;C与D可形成化合物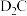 ;C、E同主族。回答下列问题:
;C、E同主族。回答下列问题:
(1)B在周期表中的位置为________ ;F元素简单离子结构示意图为_____________ 。
(2)C、D、E、F的简单离子半径由大到小的顺序为_______________ (用离子符号表示)。
(3)C元素与D元素以原子个数比1:1可形成化合物Q,Q的电子式为________ 。
(4)非金属性强弱:E______ F(填“强于”或“弱于”),请列出一个理由_________ 。
(5)E与 生成一种刺激性气味的气体X,写出X与少量的D最高价氧化物对应水化物反应的离子方程式
生成一种刺激性气味的气体X,写出X与少量的D最高价氧化物对应水化物反应的离子方程式_________ 。
 ;C元素原子的最外层电子数比次外层多4;C与D可形成化合物
;C元素原子的最外层电子数比次外层多4;C与D可形成化合物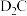 ;C、E同主族。回答下列问题:
;C、E同主族。回答下列问题:(1)B在周期表中的位置为
(2)C、D、E、F的简单离子半径由大到小的顺序为
(3)C元素与D元素以原子个数比1:1可形成化合物Q,Q的电子式为
(4)非金属性强弱:E
(5)E与
 生成一种刺激性气味的气体X,写出X与少量的D最高价氧化物对应水化物反应的离子方程式
生成一种刺激性气味的气体X,写出X与少量的D最高价氧化物对应水化物反应的离子方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】A、B、C、D四种短周期元素,A、B同主族,C、D同周期。气体A2与气体C2按体积比2:1混合后点燃能够发生爆炸,且产物在常温常压下是一种无色无味的液体。B的阳离子与C的-2价阴离子的核外电子排布相同。D能形成自然界硬度最大的单质。请根据上述所提供的信息回答下列问题。
(1)写出A、B、C三种元素的元素符号:A____ 、B_____ 、C_____ ;D在周期表中的位置是_____ 。
(2)写出化合物B2C2的电子式________ 。
(3)写出B2C2和A2C反应的离子方程式:__________ 。
(4)用电子式表示A2C形成的过程:__________ 。
(1)写出A、B、C三种元素的元素符号:A
(2)写出化合物B2C2的电子式
(3)写出B2C2和A2C反应的离子方程式:
(4)用电子式表示A2C形成的过程:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】X、Y、Z、Q、W、R属于元素周期表中前20号主族元素,且原子序数依次增大。基态X原子的2p能级上有2个电子,Z是地壳中含量最高的元素,W与Z同族,Q为电负性最强的主族元素。R的最外层电子数与最内层电子数相等。回答下列问题:
(1)R在元素周期表中的位置是___________ ;W的元素符号为___________ ,其基态简单离子的电子排布式为___________ 。
(2)Z元素位于元素周期表的___________ 区,其基态原子核外电子的空间运动状态有___________ 种。
(3)X、Y、Z三种元素中第一电离能最大的是________ (填元素符号),理由是________ 。
(4)Z、Q、W三种元素形成的简单气态氢化物的热稳定性由大到小的顺序___________ (用化学式表示)。
(1)R在元素周期表中的位置是
(2)Z元素位于元素周期表的
(3)X、Y、Z三种元素中第一电离能最大的是
(4)Z、Q、W三种元素形成的简单气态氢化物的热稳定性由大到小的顺序
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】Ⅰ.在下列各组物质中,找出合适的序号填在对应的空格内:
①NO2和N2O4②12C和14C ③40K和40Ca ④甲烷和丙烷 ⑤红磷和白磷 ⑥异戊烷( )和新戊烷(
)和新戊烷( ) ⑦
) ⑦ 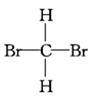 和
和
(1)互为同位素的是___________ 。
(2)互为同分异构体的是___________ 。
(3)互为同系物的是___________ 。
(4)为同一种物质的是___________ 。
(5)下列说法正确的的是___________ (填字母标号)。
A.聚乙烯(PE)、光导纤维、聚四氟乙烯(PTFE)、聚丙烯(PP)、聚氯乙烯(PVC)、石墨纤维属于有机高分子化合物。
B.合成高分子材料包括塑料、合成纤维、天然橡胶、粘合剂、涂料等。
C.则有机物M(CH≡C-CH=CH-CH3)分子中,共平面的原子数至少为9个
D.某高分子化合物结构如下:

其单体有三种,其中有一种是CH2=CH-CH=CH2 。
II.用石油裂化和裂解过程中得到的乙烯、丙烯来合成丙烯酸乙酯的路线如下:
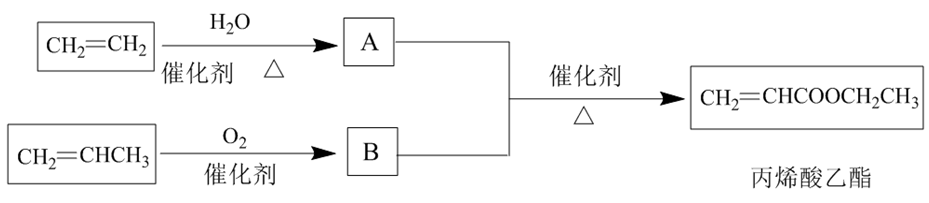
根据以上材料和所学的化学知识回答下列问题:
(6)A同分异构体结构简式为___________ 。
(7)有机物A和B反应的化学方程式为___________ 。
(8)久置的丙烯酸乙酯自身会发生聚合反应,写出生成的聚合物的化学方程式为___________ 。
①NO2和N2O4②12C和14C ③40K和40Ca ④甲烷和丙烷 ⑤红磷和白磷 ⑥异戊烷(
 )和新戊烷(
)和新戊烷( ) ⑦
) ⑦  和
和
(1)互为同位素的是
(2)互为同分异构体的是
(3)互为同系物的是
(4)为同一种物质的是
(5)下列说法正确的的是
A.聚乙烯(PE)、光导纤维、聚四氟乙烯(PTFE)、聚丙烯(PP)、聚氯乙烯(PVC)、石墨纤维属于有机高分子化合物。
B.合成高分子材料包括塑料、合成纤维、天然橡胶、粘合剂、涂料等。
C.则有机物M(CH≡C-CH=CH-CH3)分子中,共平面的原子数至少为9个
D.某高分子化合物结构如下:

其单体有三种,其中有一种是CH2=CH-CH=CH2 。
II.用石油裂化和裂解过程中得到的乙烯、丙烯来合成丙烯酸乙酯的路线如下:

根据以上材料和所学的化学知识回答下列问题:
(6)A同分异构体结构简式为
(7)有机物A和B反应的化学方程式为
(8)久置的丙烯酸乙酯自身会发生聚合反应,写出生成的聚合物的化学方程式为
您最近一年使用:0次



