如图是一个化学过程的示意图。
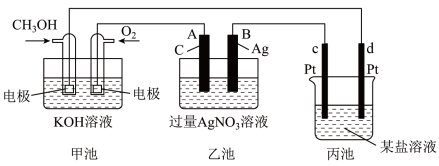
请回答:
(1)甲池是________ 池,通入O2的一极电极反应式为__________________ ,该电池的总反应方程式为______________ 。
(2)乙池中A电极名称为________ 极,电极反应式为__________________ 。一段时间后溶液的pH________ (填“增大”、“减小”或“不变”)。
(3)当乙池中B(Ag)极的质量增加5.40 g时,甲池中理论上消耗O2________ mL(标准状况下)。

请回答:
(1)甲池是
(2)乙池中A电极名称为
(3)当乙池中B(Ag)极的质量增加5.40 g时,甲池中理论上消耗O2
更新时间:2019-06-06 09:45:43
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】人们应用原电池原理制作了多种电池以满足不同的需要,电池发挥着重要的作用。请回答下列问题:
(1)电子表和电子计算器中所用的是钮扣式的微型银锌电池,其电极材料分别为Ag2O和Zn,电解液为KOH溶液。工作时电池总反应为:Ag2O+Zn+H2O=2Ag+Zn(OH)2。
①工作时电流从______ 极流向______ 极(两空均填“Ag2O”或“Zn”)。
②负极的电极反应式为__________________________ 。
③工作时电池正极区的pH__________ (填“增大”“减小”或“不变”)。
(2)中国科学院应用化学研究所在甲醇(CH3OH是一种可燃物)燃料电池技术方面获得新突破。甲醇燃料电池的工作原理如图所示。
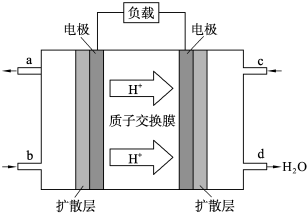
①该电池工作时,b口通入的物质为______________ 。
②该电池负极的电极反应式为______________ 。
③工作一段时间后,当6.4 g甲醇完全反应生成CO2时,有__________ NA个电子转移。
(1)电子表和电子计算器中所用的是钮扣式的微型银锌电池,其电极材料分别为Ag2O和Zn,电解液为KOH溶液。工作时电池总反应为:Ag2O+Zn+H2O=2Ag+Zn(OH)2。
①工作时电流从
②负极的电极反应式为
③工作时电池正极区的pH
(2)中国科学院应用化学研究所在甲醇(CH3OH是一种可燃物)燃料电池技术方面获得新突破。甲醇燃料电池的工作原理如图所示。

①该电池工作时,b口通入的物质为
②该电池负极的电极反应式为
③工作一段时间后,当6.4 g甲醇完全反应生成CO2时,有
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】由于温室效应和资源短缺等问题,如何降低大气中的CO2含量并加以开发利用,引起了各国的普遍重视。目前工业上有一种方法是用CO2生产燃料甲醇:CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g)。该反应进行过程中能量的变化(单位为kJ·mol-1)如图所示。

请回答下列问题:
(1)观察图象可知上述反应过程中,断裂反应物中的化学键吸收的总能量_____ (填“大于”“小于”或“等于”)形成生成物中的化学键释放的总能量。
(2)甲醇的结构类似于乙醇,试写出甲醇的结构式:______ 。甲醇分子中的化学键类型是______ (填“离子键“共价键”)。
(3)科研人员开发出一种新型甲醇燃料电池。其电解质溶液是KOH溶液,在该电池的负极发生反应的物质是________ ,发生的是________ (填"氧化"或"还原")反应。
(4)欲使合成甲醇的化学反应速率加快,请写出两条措施:________ ;

请回答下列问题:
(1)观察图象可知上述反应过程中,断裂反应物中的化学键吸收的总能量
(2)甲醇的结构类似于乙醇,试写出甲醇的结构式:
(3)科研人员开发出一种新型甲醇燃料电池。其电解质溶液是KOH溶液,在该电池的负极发生反应的物质是
(4)欲使合成甲醇的化学反应速率加快,请写出两条措施:
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】据图回答下列问题:
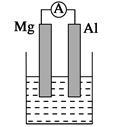
Ⅰ、(1)若烧杯中溶液为稀硫酸,则观察到的现象是___________ ,负极反应式为:_________________ 。
(2)若烧杯中溶液为氢氧化钠溶液,则负极为________ (填Mg或Al),总反应化学方程式为____________________________________ 。
Ⅱ、由Al、Cu、浓硝酸组成原电池,其正极的电极反应式为______________ 。
Ⅲ、中国科学院长春应用化学研究所在甲醇燃料电池技术方面获得新突破,组装出了自呼吸电池及主动式电堆。甲醇燃料电池的工作原理如下图所示。

(1)该电池工作时,b通入的物质为_____________ ,c通入的物质为_______________ 。
(2)该电池负极的电极反应式为:_______
(3)工作一段时间后,当12.8 g甲醇完全反应生成CO2时,有______________ NA个电子转移。

Ⅰ、(1)若烧杯中溶液为稀硫酸,则观察到的现象是
(2)若烧杯中溶液为氢氧化钠溶液,则负极为
Ⅱ、由Al、Cu、浓硝酸组成原电池,其正极的电极反应式为
Ⅲ、中国科学院长春应用化学研究所在甲醇燃料电池技术方面获得新突破,组装出了自呼吸电池及主动式电堆。甲醇燃料电池的工作原理如下图所示。

(1)该电池工作时,b通入的物质为
(2)该电池负极的电极反应式为:
(3)工作一段时间后,当12.8 g甲醇完全反应生成CO2时,有
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】回答下列问题
(1)在下图所示的原电池装置中,负极的电极反应为___________ ,电池总反应为___________ ,当电路中通过 电子时,交换膜左侧溶液中离子减少的物质的量为
电子时,交换膜左侧溶液中离子减少的物质的量为___________ 。
(2)某兴趣小组的同学认为,如果模拟工业上离子交换膜法制烧碱的方法,那么可以设想用如图装置电解硫酸钾溶液来制取氢气、氧气、硫酸和氢氧化钾。
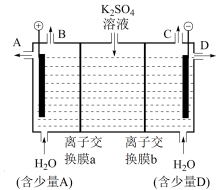
①该电解槽的阴极反应式为___________ 。
②离子交换膜b为___________ (填“阳离子交换膜”或“阴离子交换膜”)。
③出口A获得___________ 产品。
(1)在下图所示的原电池装置中,负极的电极反应为
 电子时,交换膜左侧溶液中离子减少的物质的量为
电子时,交换膜左侧溶液中离子减少的物质的量为
(2)某兴趣小组的同学认为,如果模拟工业上离子交换膜法制烧碱的方法,那么可以设想用如图装置电解硫酸钾溶液来制取氢气、氧气、硫酸和氢氧化钾。

①该电解槽的阴极反应式为
②离子交换膜b为
③出口A获得
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
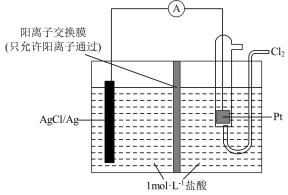
【推荐2】 也可采用“电解法”制备,装置如图所示。
也可采用“电解法”制备,装置如图所示。
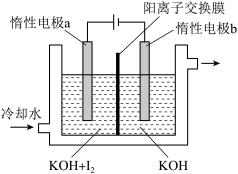
(1)写出电解时阴极的电极反应式:___________ 。
(2)电解过程中通过阳离子交换膜的离子主要为___________ ,其迁移方向是___________ 。
 也可采用“电解法”制备,装置如图所示。
也可采用“电解法”制备,装置如图所示。
(1)写出电解时阴极的电极反应式:
(2)电解过程中通过阳离子交换膜的离子主要为
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】如图是一个甲烷燃料电池工作时的示意图,乙池中的两个电极一个是石墨电极,一个是铁电极,工作时,M、N两个电极的质量都不减少,请回答下列问题:

(1)M电极的材料是______ ,其电极名称是______ ,N的电极反应式为______ ,乙池的总反应是______ ,加入甲烷的铂电极的电极反应式为______ 。
(2)在此过程中,乙池中某一电极析出金属银4.32g时,甲池中理论上消耗氧气为______ L(标准状况下),若此时乙池溶液的体积为200mL,则乙池中溶液的H+的浓度为_______ 。

(1)M电极的材料是
(2)在此过程中,乙池中某一电极析出金属银4.32g时,甲池中理论上消耗氧气为
您最近半年使用:0次
【推荐1】用电化学知识回答下列问题。
(1)“电絮凝-电气浮法”污水处理装置原理如图所示。在外电压作用下,可溶性阳极产生阳离子体对胶体污染物发生凝聚效应,同时另一极产生气体,在气体上浮过程中将絮体上浮,从而实现污染物的分离和水的净化。

①外接电源a端为___________ 极。
②石墨极电极反应为___________ 。
③铝电极___________ 用铁电极替换(填“能”或“不能”)。
(2)一种新型 可充电电池结构示意如图,电池由三个不同区域(A、B、C)组成,所用电解质分别为KOH、
可充电电池结构示意如图,电池由三个不同区域(A、B、C)组成,所用电解质分别为KOH、 和
和 ,不同区域由离子交换膜(a、b)隔开。
,不同区域由离子交换膜(a、b)隔开。
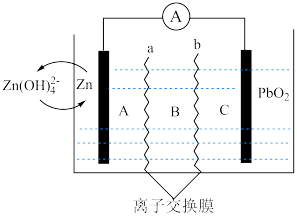
①Zn发生极___________ 反应(填“氧化”或“还原”)。
②a为极___________ 离子交换膜(填“阳”或“阴”,下同),b为极___________ 离子交换膜。
③ 的电极反应式为极
的电极反应式为极___________ 。
(3)一种二氧化碳的富集装置如图所示。

①电极材料采用多孔碳酸锂,“多孔”的优点是___________ 。
②电极a的电极反应式为___________ 。
(1)“电絮凝-电气浮法”污水处理装置原理如图所示。在外电压作用下,可溶性阳极产生阳离子体对胶体污染物发生凝聚效应,同时另一极产生气体,在气体上浮过程中将絮体上浮,从而实现污染物的分离和水的净化。

①外接电源a端为
②石墨极电极反应为
③铝电极
(2)一种新型
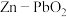 可充电电池结构示意如图,电池由三个不同区域(A、B、C)组成,所用电解质分别为KOH、
可充电电池结构示意如图,电池由三个不同区域(A、B、C)组成,所用电解质分别为KOH、 和
和 ,不同区域由离子交换膜(a、b)隔开。
,不同区域由离子交换膜(a、b)隔开。
①Zn发生极
②a为极
③
 的电极反应式为极
的电极反应式为极(3)一种二氧化碳的富集装置如图所示。

①电极材料采用多孔碳酸锂,“多孔”的优点是
②电极a的电极反应式为
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】我国科学家设计了一种锂离子电池,并用此电池来电解含有Na2SO3的工业废水,可获得硫酸等物质,该过程示意图如图:
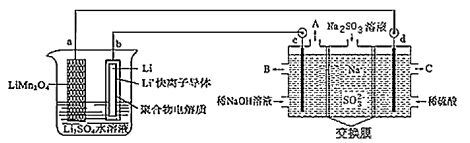
(1)锂离子电池工作时,a极发生_______ (填“氧化”或“还原”)反应, Li+移向_____ (填“a”或“b”)极, 写出b极的电极反应__________ 。
(2)电解池中物质A的化学式是_________ ,其中右侧交换膜的作用是______ ,写出 d极的电极反应___________ 。
(3)若电解池左侧溶液的体积为2 L,其浓度由2 mol/L变为4 mol/L时,理论上电路中通过的电子是____ mol。

(1)锂离子电池工作时,a极发生
(2)电解池中物质A的化学式是
(3)若电解池左侧溶液的体积为2 L,其浓度由2 mol/L变为4 mol/L时,理论上电路中通过的电子是
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】结合下列电化学装置回答问题:
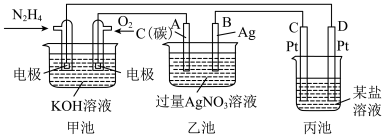
(1)图中甲池是___________ 装置(填“电解池”或“原电池”),其中 移向通
移向通___________ 的一极(填“ ”或“
”或“ ”)。
”)。
(2)写出通入 的电极的电极反应式:
的电极的电极反应式:___________ 。
(3)乙池中总反应的离子方程式为___________ 。
(4)当乙池中B(Ag)极的质量增加5.40g时,丙池也有金属析出,则丙中的某盐溶液可能是___________ (填选项),此时丙池某电极析出___________ g金属。
A. B.
B. C.NaCl D.
C.NaCl D.

(1)图中甲池是
 移向通
移向通 ”或“
”或“ ”)。
”)。(2)写出通入
 的电极的电极反应式:
的电极的电极反应式:(3)乙池中总反应的离子方程式为
(4)当乙池中B(Ag)极的质量增加5.40g时,丙池也有金属析出,则丙中的某盐溶液可能是
A.
 B.
B. C.NaCl D.
C.NaCl D.
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】(1)熔融盐燃料电池具有高的发电效率,因而受到重视。可用熔融的碳酸盐作为电解质,向负极充入燃料气 ,用空气与
,用空气与 的混合气作为正极的助燃气,以石墨为电极材料,制得燃料电池。工作过程中,
的混合气作为正极的助燃气,以石墨为电极材料,制得燃料电池。工作过程中, 移向
移向___________ 极(填“正”或“负”),负极的电极反应式为___________ ,正极的电极反应式为___________ 。
(2)某实验小组同学对电化学原理进行了一系列探究活动。
①如图为某实验小组依据的氧化还原反应:___________ (用离子方程式表示)设计的原电池装置。
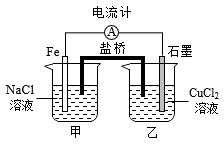
②其他条件不变,若将 溶液换为HCl溶液,石墨的电极反应式为
溶液换为HCl溶液,石墨的电极反应式为___________ 。
(3)如图为相互串联的甲、乙两电解池,其中甲池为电解精炼铜的装置。试回答下列问题:
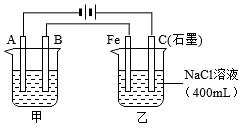
①乙池中若滴入少量酚酞溶液,电解一段时间后Fe极附近溶液呈___________ 色。
②常温下,若甲池中阴极增重 ,则乙池中阳极放出的气体在标准状况下的体积为
,则乙池中阳极放出的气体在标准状况下的体积为___________ ,若此时乙池剩余液体为400mL,则电解后溶液pH为___________ 。
 ,用空气与
,用空气与 的混合气作为正极的助燃气,以石墨为电极材料,制得燃料电池。工作过程中,
的混合气作为正极的助燃气,以石墨为电极材料,制得燃料电池。工作过程中, 移向
移向(2)某实验小组同学对电化学原理进行了一系列探究活动。
①如图为某实验小组依据的氧化还原反应:

②其他条件不变,若将
 溶液换为HCl溶液,石墨的电极反应式为
溶液换为HCl溶液,石墨的电极反应式为(3)如图为相互串联的甲、乙两电解池,其中甲池为电解精炼铜的装置。试回答下列问题:

①乙池中若滴入少量酚酞溶液,电解一段时间后Fe极附近溶液呈
②常温下,若甲池中阴极增重
 ,则乙池中阳极放出的气体在标准状况下的体积为
,则乙池中阳极放出的气体在标准状况下的体积为
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】下图是一个电化学过程的示意图:

请回答下列问题:
(1)图中甲池是__________ (填“原电池”、“原解池”、“原镀池”),乙池中A电极的名称是__________ (填“正极”、“负极”、“阴极”或“阳极”)
(2)写出甲池中甲醇发生反应的电极反应式:______________________________________________
(3)当乙池中B极质量增加10.8克,理论上甲池中消耗O2的体积为:_______ L(标准状况),此时丙池中D极析出3.2g某金属,则丙池中的某盐溶液可能是__________ (填字母,下同)
a.MgSO4溶液 b.CuSO4溶液 c.NaCl溶液 d.AgNO3溶液
(4)若丙中电极不变,将其溶液换成NaCl溶液,一段时间后,丙中溶液的pH将_________ (填“增大”、“减小”或“不变”);甲中溶液的pH将_________ (填“增大”、“减小”或“不变”)。

请回答下列问题:
(1)图中甲池是
(2)写出甲池中甲醇发生反应的电极反应式:
(3)当乙池中B极质量增加10.8克,理论上甲池中消耗O2的体积为:
a.MgSO4溶液 b.CuSO4溶液 c.NaCl溶液 d.AgNO3溶液
(4)若丙中电极不变,将其溶液换成NaCl溶液,一段时间后,丙中溶液的pH将
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】装置如图所示,C、D、E、F、X、Y都是惰性电极,甲、乙中溶液的体积和浓度都相同(假设通电前后溶液体积不变),A、B为外接直流电源的两极。将直流电源接通后,F极附近呈红色。请回答:

(1)B极是电源的________ 极,C极的电极反应式为_____________ ,
(2)一段时间后丁中X极附近的颜色逐渐____________ (填“变深”或“变浅”)。
(3)若甲、乙装置中的C、D、E、F电极均只有一种单质生成,对应单质的物质的量之比为_____________ 。
(4)现用丙装置给铜件镀银,则H应该是______ (填“铜”或“银”),电镀液是__________ 溶液。常温下,当乙中溶液的c(OH-)=0.1mol·L-1时(此时乙溶液体积为500mL),丙中镀件上析出银的质量为____________ g。
(5)若甲烧杯是在铁件表面镀铜,已知电镀前两电极质量相同,电镀完成后将它们取出,洗净、烘干、称量,发现二者质量相差7.68g,则电镀时电路中通过的电子为____ mol。

(1)B极是电源的
(2)一段时间后丁中X极附近的颜色逐渐
(3)若甲、乙装置中的C、D、E、F电极均只有一种单质生成,对应单质的物质的量之比为
(4)现用丙装置给铜件镀银,则H应该是
(5)若甲烧杯是在铁件表面镀铜,已知电镀前两电极质量相同,电镀完成后将它们取出,洗净、烘干、称量,发现二者质量相差7.68g,则电镀时电路中通过的电子为
您最近半年使用:0次



