对于:2C4H10(g) + 13O2(g) = 8CO2(g) + 10H2O(l) △H= -5800 kJ·molˉ1的叙述错误的是
| A.该反应的反应热为△H= -5800 kJ·molˉ1,是放热反应 |
| B.该反应的△H与各物质的状态有关,与化学计量数也有关 |
| C.该反应为丁烷燃烧的热化学方程式,可知丁烷的燃烧热为5800 kJ·molˉ1 |
| D.该式的含义为:25℃、101kPa下,2mol C4H10气体完全燃烧生成CO2气体和液态水时放出热量5800kJ |
更新时间:2019-06-06 21:38:40
|
相似题推荐
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】根据下面的信息,判断下列叙述正确的是


| A.氢气跟氧气反应生成水的同时吸收能量 |
| B.氢气跟氧气反应生成水的同时释放能量 |
| C.2 mol H2(g)跟1 mol O2(g)反应生成2 mol H2O(g)吸收能量490 kJ |
| D.1 mol H2跟1/2 mol O2反应生成1 mol H2O一定释放能量245 kJ |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】0.5mol 完全燃烧生成
完全燃烧生成 和液态
和液态 时,放出445kJ热量,则下列热化学方程式正确的是
时,放出445kJ热量,则下列热化学方程式正确的是
 完全燃烧生成
完全燃烧生成 和液态
和液态 时,放出445kJ热量,则下列热化学方程式正确的是
时,放出445kJ热量,则下列热化学方程式正确的是A.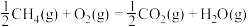 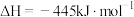 |
B.  |
C.  |
D.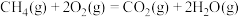 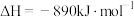 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐3】溴与氢气在一定条件下反应的热化学方程式如下:
①Br2(g)+ H2(g)⇌2HBr(g) △H=-Q1 kJ·mol-1
②Br2(l)+ H2(g)⇌2HBr(g) △H =-Q2 kJ·mol-1
下列说法正确的是
①Br2(g)+ H2(g)⇌2HBr(g) △H=-Q1 kJ·mol-1
②Br2(l)+ H2(g)⇌2HBr(g) △H =-Q2 kJ·mol-1
下列说法正确的是
| A.Q1<Q2 |
| B.1 mol HBr(g)具有的能量大于1mol HBr(l)具有的能量 |
| C.相同条件下,Cl2(g)+ H2(g)⇌2HCl(g) △H >-Q1 kJ·mol-1 |
| D.向1 mol Br2(g)中加入1 mol H2(g)在该条件下充分反应,放出Q1 kJ热量 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐1】工业上常用CH4在复合组分的催化剂作用下还原大气污染物SO2,生成S固体,同时生成CO2和液态H2O。已知:H2(g)、CH4(g)、S(s)的燃烧热(ΔH)分别是-285.8kJ·mol-1、-890.3kJ·mol-1、-297.2kJ·mol-1。下列说法正确的是
| A.1molS(s)燃烧生成SO3(1),放出297.2kJ的热量 |
| B.CH4(g)+2O2(g)=CO2(g)+2H2O(g) △H=-890.3kJ·mol-1 |
| C.CH4(g)+2SO2(g)=CO2(g)+2S(s)+2H2O(1) △H=-295.9kJ·mol-1 |
| D.同一条件下,单位质量的CH4完全燃烧放出的热量比H2多 |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐2】下列说法或表示正确的是
A.500℃、30 MPa 下,将 0.5 mol N2和 1.5 mol H2置于密闭容器中充分反应生成 NH3(g), 放热 19.3 kJ,其热化学方程式为:N2(g) + 3H2(g)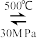 2NH3(g) △ H =− 38.6 kJ · mol−1 2NH3(g) △ H =− 38.6 kJ · mol−1 |
| B.等量的硫蒸气和硫固体分别完全燃烧,后者放出热量少 |
| C.由 C(石墨) = C(金刚石) ΔH =+ 1.9kJ·mol−1,可知,金刚石比石墨稳定 |
| D.1 mol 甲烷燃烧生成气态水和二氧化碳气体所放出的热量就是甲烷的燃烧热 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】已知H2(g)+F2(g)=2HF(g) ΔH=-270kJ/mol,下列说法正确的是
| A.1个氢气分子与1个氟气分子反应生成2个氟化氢分子放出270kJ热量 |
| B.1mol氢气与1mol氟气反应生成2mol液态氟化氢放出的热量小于270kJ |
| C.2mol氟化氢气体分解成1mol的氢气和1mol的氟气放出270kJ热量 |
| D.1mol氢气1mol氟气的能量总和大于2mol氟化氢气体的能量 |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐2】下列有关能量变化的叙述正确的是
| A.碘升华属于吸热反应 |
| B.热化学方程式的计量数只表示物质的量 |
| C.“钻燧取火”过程中发生的是物理变化 |
D. 燃烧反应中仅存在放热过程 燃烧反应中仅存在放热过程 |
您最近一年使用:0次


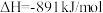 ”在298K和100 kPa时,表示的意义是
”在298K和100 kPa时,表示的意义是

