溶液中可能含有H+、K+、NH4+、Mg2+、Fe3+、Al3+、SO42-等离子,当向该溶液中加入某浓度的NaOH溶液时,发现生成沉淀的物质的量随NaOH溶液的体积变化如图所示,由此可知,
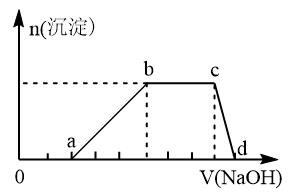
⑴该溶液中肯定含有的离子是_________________ ,且各离子的物质的量之比为____________ ;肯定不含的离子是_____________ 。
⑵还有一种离子可能存在,写出检验这种离子的实验方法及现象:_______________ 。

⑴该溶液中肯定含有的离子是
⑵还有一种离子可能存在,写出检验这种离子的实验方法及现象:
11-12高二上·江苏无锡·期中 查看更多[1]
(已下线)2011-2012学年江苏省无锡一中高二上学期期中考试化学试卷(必修)
更新时间:2016/12/09 02:21:17
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】回答下列问题
Ⅰ.处于下列状态的物质中:A.固态氯化钠 B.干冰 C.液氨 D.铜 E.硫酸钡晶体 F.甲烷 G.五氧化二磷 H.稀硫酸 I.熔融的硝酸钾 J.石墨 K.酒精 L.胆矾溶液 M.氢氧化铜 N.熟石灰 O.盐酸。
(1)上述物质中属于强电解质且能导电的是_______ (填字母,下同)。
(2)上述物质中属于电解质的是_______ 。
(3)上述物质中属于非电解质的是_______ 。
Ⅱ.在两份相同的 溶液中,分别滴入浓度相等的
溶液中,分别滴入浓度相等的 、
、 溶液,其导电能力随滴入溶液体积变化的曲线如图所示。
溶液,其导电能力随滴入溶液体积变化的曲线如图所示。
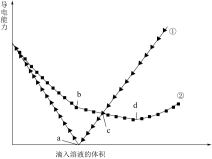
(4)图中①、②分别代表滴加哪种溶液的变化曲线①_______ ②_______
(5)d点,溶液中大量存在的离子是_______ 。
(6)a、b两点对应的溶液分别显_______ _______ (填“酸性”“中性”或“碱性”)
Ⅰ.处于下列状态的物质中:A.固态氯化钠 B.干冰 C.液氨 D.铜 E.硫酸钡晶体 F.甲烷 G.五氧化二磷 H.稀硫酸 I.熔融的硝酸钾 J.石墨 K.酒精 L.胆矾溶液 M.氢氧化铜 N.熟石灰 O.盐酸。
(1)上述物质中属于强电解质且能导电的是
(2)上述物质中属于电解质的是
(3)上述物质中属于非电解质的是
Ⅱ.在两份相同的
 溶液中,分别滴入浓度相等的
溶液中,分别滴入浓度相等的 、
、 溶液,其导电能力随滴入溶液体积变化的曲线如图所示。
溶液,其导电能力随滴入溶液体积变化的曲线如图所示。
(4)图中①、②分别代表滴加哪种溶液的变化曲线①
(5)d点,溶液中大量存在的离子是
(6)a、b两点对应的溶液分别显
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】(1)某同学发布了一份无色溶液检测报告,结果如下(水电离的H+、OH-忽略不计)
这份报告是否合理_______ ,理由是_____________________ 。
(2)甲乙两厂排放出两种含重金属离子废液,检验甲厂排出废液呈碱性且含Ba2+,若将甲乙两厂废液按一定比例混合后,毒性明显降低,回答下列问题
①乙厂废液可能含有( )
A. K+、SO42- B.Cu2+、SO42- C.Ag+、NO3- D.Cu2+、Cl-
②用离子方程式表示毒性降低的原因_____________________ 。
(3)X溶液含Ba2+、Ag+、Cu2+,请你设计一实验方案将这三种离子逐一沉淀分离______ 。(限用试剂硫酸钠溶液,盐酸,氢氧化钠溶液)
| 离子 | 浓度/mol·L-1 | 离子 | 浓度/mol·L-1 |
| Na+ | 0.1 | Cu2+ | 0.2 |
| Ba2+ | 0.5 |  | 1..5 |
| Mg2+ | 0.3 | Cl- | 0.6 |
这份报告是否合理
(2)甲乙两厂排放出两种含重金属离子废液,检验甲厂排出废液呈碱性且含Ba2+,若将甲乙两厂废液按一定比例混合后,毒性明显降低,回答下列问题
①乙厂废液可能含有
A. K+、SO42- B.Cu2+、SO42- C.Ag+、NO3- D.Cu2+、Cl-
②用离子方程式表示毒性降低的原因
(3)X溶液含Ba2+、Ag+、Cu2+,请你设计一实验方案将这三种离子逐一沉淀分离
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】某无色透明溶液中可能含有下列离子中的一种或几种:Na+、Mg2+、Cu2+、OH-、Cl-、CO 、NO
、NO 。现进行如下实验:
。现进行如下实验:
①用红色石蕊试纸检验,试纸变为蓝色。
②另取少量溶液逐滴滴加盐酸至过量,无气体放出,再加入BaCl2溶液后,没有沉淀生成。
③另取少量溶液用硝酸酸化后,加入AgNO3溶液有白色沉淀生成。
(1)根据上述实验推断:原溶液中肯定有___________ ,肯定没有___________ ,不能肯定存在___________ 。
(2)写出操作③中发生反应的离子方程式:___________ 。
 、NO
、NO 。现进行如下实验:
。现进行如下实验:①用红色石蕊试纸检验,试纸变为蓝色。
②另取少量溶液逐滴滴加盐酸至过量,无气体放出,再加入BaCl2溶液后,没有沉淀生成。
③另取少量溶液用硝酸酸化后,加入AgNO3溶液有白色沉淀生成。
(1)根据上述实验推断:原溶液中肯定有
(2)写出操作③中发生反应的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】“价-类”二维图是学习元素化合物的一种好方法。硫或氮及其化合物的部分“价-类”二维图如图所示。
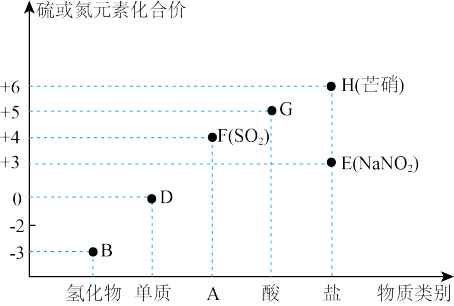
完成下列填空:
(1) 的物质类别是
的物质类别是_______ (填“碱”或“氧化物”)。芒硝的化学式为_______ ,用洁净的铂丝蘸取芒硝在酒精灯上灼烧,火焰呈现的颜色为_______ 。
(2)D可以为 或
或 ,已知同温同压下,同体积的
,已知同温同压下,同体积的 与
与 (蒸气)的质量比为7∶64,则
(蒸气)的质量比为7∶64,则
_______ 。
(3)下列物质能与 发生反应,其中
发生反应,其中 体现还原性的是
体现还原性的是_______ (填序号)。
a.氢氧化钠溶液 b.溴水 c.品红溶液
(4)常温下, 的浓溶液可以用干燥的铁或铝容器盛装,原因是
的浓溶液可以用干燥的铁或铝容器盛装,原因是_______ 。
(5)已知 溶液既有氧化性又有还原性,请设计实验证明之。(供选用的试剂是:硫化钠溶液 品红溶液酸性
溶液既有氧化性又有还原性,请设计实验证明之。(供选用的试剂是:硫化钠溶液 品红溶液酸性 溶液 澄清石灰水 稀硫酸)。
溶液 澄清石灰水 稀硫酸)。_______ 。

完成下列填空:
(1)
 的物质类别是
的物质类别是(2)D可以为
 或
或 ,已知同温同压下,同体积的
,已知同温同压下,同体积的 与
与 (蒸气)的质量比为7∶64,则
(蒸气)的质量比为7∶64,则
(3)下列物质能与
 发生反应,其中
发生反应,其中 体现还原性的是
体现还原性的是a.氢氧化钠溶液 b.溴水 c.品红溶液
(4)常温下,
 的浓溶液可以用干燥的铁或铝容器盛装,原因是
的浓溶液可以用干燥的铁或铝容器盛装,原因是(5)已知
 溶液既有氧化性又有还原性,请设计实验证明之。(供选用的试剂是:硫化钠溶液 品红溶液酸性
溶液既有氧化性又有还原性,请设计实验证明之。(供选用的试剂是:硫化钠溶液 品红溶液酸性 溶液 澄清石灰水 稀硫酸)。
溶液 澄清石灰水 稀硫酸)。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】尽管海洋中含有大量钠元素,但其都以化合态(Na+)的形态而存在。
(1)用离子方程式解释为什么海水中不存在金属钠单质:_______ 。
(2)用金属钠制取Na2O通常采用以下方法:2NaNO2+6Na=4Na2O+N2↑,而不采用钠在氧气中燃烧的原因是(用文字说明):_______ 。
(3)某溶液可能含有K+、Na+、 、
、 、Cl-。为了鉴别这些离子,分别取少量溶液进行以下实验:
、Cl-。为了鉴别这些离子,分别取少量溶液进行以下实验:
(I)加BaCl2溶液产生白色沉淀,分离;在沉淀中加入足量的盐酸,沉淀部分溶解。
(II)取(I)过滤后滤液,加HNO3酸化的AgNO3溶液,有白色沉淀析出。
①分析上述2个实验,原溶液中一定存在的离子是_______ 。
②若通过实验能检验到K+,则实验现象是_______ 。
(1)用离子方程式解释为什么海水中不存在金属钠单质:
(2)用金属钠制取Na2O通常采用以下方法:2NaNO2+6Na=4Na2O+N2↑,而不采用钠在氧气中燃烧的原因是(用文字说明):
(3)某溶液可能含有K+、Na+、
 、
、 、Cl-。为了鉴别这些离子,分别取少量溶液进行以下实验:
、Cl-。为了鉴别这些离子,分别取少量溶液进行以下实验:(I)加BaCl2溶液产生白色沉淀,分离;在沉淀中加入足量的盐酸,沉淀部分溶解。
(II)取(I)过滤后滤液,加HNO3酸化的AgNO3溶液,有白色沉淀析出。
①分析上述2个实验,原溶液中一定存在的离子是
②若通过实验能检验到K+,则实验现象是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】“生活无处不化学”,请你回答下列问题。
(1)厨房中的调味品有:①盐(主要成分为氯化钠)、②碱面(主要成分为碳酸钠)、③白醋(主要成分为乙酸)。
将上述物质分别溶于水,水溶液具有碱性的是_______ (填序号,下同),主要成分属于盐类的是_______ ,相互间能发生反应的是_______ 。
(2)食盐不慎洒落在天然气的火焰上,可观察到_______ 。
(3)沾有水的铁制器皿在高温的的火焰上会发黑,该反应的化学方程式是_______ 。
(4)使用“84”消毒液(含NaClO)时,按一定比例与水混合,并在空气中放置一段时间,使NaClO与H2O及空气中的CO2充分反应,目的是得到杀菌消毒效果更好的_______ (填物质名称),将该反应的离子方程式补充完整:
ClO- + CO2 + H2O =_______ + _____
(5)用KMnO4与浓盐酸反应制取氯气的化学方程式为_______ 。
(1)厨房中的调味品有:①盐(主要成分为氯化钠)、②碱面(主要成分为碳酸钠)、③白醋(主要成分为乙酸)。
将上述物质分别溶于水,水溶液具有碱性的是
(2)食盐不慎洒落在天然气的火焰上,可观察到
(3)沾有水的铁制器皿在高温的的火焰上会发黑,该反应的化学方程式是
(4)使用“84”消毒液(含NaClO)时,按一定比例与水混合,并在空气中放置一段时间,使NaClO与H2O及空气中的CO2充分反应,目的是得到杀菌消毒效果更好的
ClO- + CO2 + H2O =
(5)用KMnO4与浓盐酸反应制取氯气的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】如表是元素周期表的一部分,除标出的元素外,表中的每个编号代表一种元素。请根据要求回答问题:

(1)①的元素符号是___ ;②的元素名称为___ ;
(2)②和⑤的原子半径大小关系是②___ ⑤(填“>”“<”或“=”);
(3)③和⑤形成的化合物含有的化学键是__ (填“离子键”或“共价键”);
(4)③、④的最高价氧化物对应的水化物相互反应的化学方程式为__ 。

(1)①的元素符号是
(2)②和⑤的原子半径大小关系是②
(3)③和⑤形成的化合物含有的化学键是
(4)③、④的最高价氧化物对应的水化物相互反应的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】某无色溶液中,已知含有H+、Mg2+、 、Al3+各1mol,向该溶液中逐滴加入氢氧化钠溶液,则消耗氢氧化钠溶液体积(x轴)和生成沉淀量(y轴)之间的函数关系用图象表示
、Al3+各1mol,向该溶液中逐滴加入氢氧化钠溶液,则消耗氢氧化钠溶液体积(x轴)和生成沉淀量(y轴)之间的函数关系用图象表示_______ (用尺子作图,标出数量关系)。
 、Al3+各1mol,向该溶液中逐滴加入氢氧化钠溶液,则消耗氢氧化钠溶液体积(x轴)和生成沉淀量(y轴)之间的函数关系用图象表示
、Al3+各1mol,向该溶液中逐滴加入氢氧化钠溶液,则消耗氢氧化钠溶液体积(x轴)和生成沉淀量(y轴)之间的函数关系用图象表示
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】以含Fe2O3、FeO、SiO2、A12O3的混合物为原料,设计两种制备铁红(Fe2O3)的一种方案,部分产物已略去。

其中第③步试剂X体积(ml)与产生沉淀质量(g)的关系如图所示。
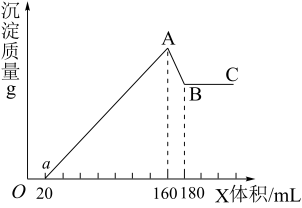
回答下列问题:
(1)溶液B中的溶质是_______ (填化学式)
(2)第②步的化学方程式为_______ 。
(3)试剂X的溶质可能是_______ (选填编号)
A.HNO3 B.NaHCO3 C. NH3.H2O D.NaOH
加入足量试剂X后,应进行的操作名称是_______ 。
(4)若试剂X的浓度为5mol/L,则固体中Al2O3的质量是_______ g。最终得到铁红的质量是_______ g(保留一位小数)

其中第③步试剂X体积(ml)与产生沉淀质量(g)的关系如图所示。

回答下列问题:
(1)溶液B中的溶质是
(2)第②步的化学方程式为
(3)试剂X的溶质可能是
A.HNO3 B.NaHCO3 C. NH3.H2O D.NaOH
加入足量试剂X后,应进行的操作名称是
(4)若试剂X的浓度为5mol/L,则固体中Al2O3的质量是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】完成下列问题。
(1)向CuCl2溶液中滴加NaOH溶液,现象:_______ ,离子方程式:_______ 。
(2)向Ba(OH)2溶液中加入稀硫酸,现象:_______ ,离子方程式:_______ 。
(3)某无色透明溶液可能存在大量Ag+、Mg2+、Fe3+、Cu2+、Cl-、NO 、CO
、CO 、K+中的一种或几种,请填写下列空白:
、K+中的一种或几种,请填写下列空白:
①取少量原溶液,加入过量稀盐酸,有白色沉淀生成,再加入过量稀硝酸,沉淀不消失,说明原溶液中肯定存在的离子是_______ 。
②取①的滤液加过量的NaOH溶液,出现白色沉淀,说明原溶液中肯定有_______ ,有关反应的离子方程式为_______ 。
③通过以上叙述可知溶液中肯定不存在的离子是_______ ,可能存在的离子是_______ 。
(1)向CuCl2溶液中滴加NaOH溶液,现象:
(2)向Ba(OH)2溶液中加入稀硫酸,现象:
(3)某无色透明溶液可能存在大量Ag+、Mg2+、Fe3+、Cu2+、Cl-、NO
 、CO
、CO 、K+中的一种或几种,请填写下列空白:
、K+中的一种或几种,请填写下列空白:①取少量原溶液,加入过量稀盐酸,有白色沉淀生成,再加入过量稀硝酸,沉淀不消失,说明原溶液中肯定存在的离子是
②取①的滤液加过量的NaOH溶液,出现白色沉淀,说明原溶液中肯定有
③通过以上叙述可知溶液中肯定不存在的离子是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】I.现有以下物质:①石墨;②乙醇;③氨水;④二氧化碳;⑤碳酸钠固体;⑥氢氧化钡溶液;⑦纯醋酸;⑧氯化氢气体。(填序号)
(1)其中能导电的是_______ ;属于非电解质的是_______ ;属于电解质的是_______ 。
II.某100mL溶液可能含有 、
、 、
、 、
、 、
、 、
、 中的若干种,取该溶液进行连续实验,实验过程如图所示(所加试剂均过量,已知
中的若干种,取该溶液进行连续实验,实验过程如图所示(所加试剂均过量,已知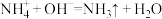 ,气体全部逸出)。
,气体全部逸出)。
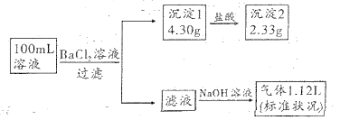
(2)原溶液中一定含有_______ 离子,可能含有_______ 离子。
(3)实验中生成硫酸钡的离子方程式为_______ 。
(4)原溶液中 的物质的量浓度范围是
的物质的量浓度范围是_______ 。
(5)对可能存在的离子用什么方法检验_______ 。
(1)其中能导电的是
II.某100mL溶液可能含有
 、
、 、
、 、
、 、
、 、
、 中的若干种,取该溶液进行连续实验,实验过程如图所示(所加试剂均过量,已知
中的若干种,取该溶液进行连续实验,实验过程如图所示(所加试剂均过量,已知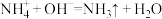 ,气体全部逸出)。
,气体全部逸出)。
(2)原溶液中一定含有
(3)实验中生成硫酸钡的离子方程式为
(4)原溶液中
 的物质的量浓度范围是
的物质的量浓度范围是(5)对可能存在的离子用什么方法检验
您最近一年使用:0次



