完成下列问题。
(1)向CuCl2溶液中滴加NaOH溶液,现象:_______ ,离子方程式:_______ 。
(2)向Ba(OH)2溶液中加入稀硫酸,现象:_______ ,离子方程式:_______ 。
(3)某无色透明溶液可能存在大量Ag+、Mg2+、Fe3+、Cu2+、Cl-、NO 、CO
、CO 、K+中的一种或几种,请填写下列空白:
、K+中的一种或几种,请填写下列空白:
①取少量原溶液,加入过量稀盐酸,有白色沉淀生成,再加入过量稀硝酸,沉淀不消失,说明原溶液中肯定存在的离子是_______ 。
②取①的滤液加过量的NaOH溶液,出现白色沉淀,说明原溶液中肯定有_______ ,有关反应的离子方程式为_______ 。
③通过以上叙述可知溶液中肯定不存在的离子是_______ ,可能存在的离子是_______ 。
(1)向CuCl2溶液中滴加NaOH溶液,现象:
(2)向Ba(OH)2溶液中加入稀硫酸,现象:
(3)某无色透明溶液可能存在大量Ag+、Mg2+、Fe3+、Cu2+、Cl-、NO
 、CO
、CO 、K+中的一种或几种,请填写下列空白:
、K+中的一种或几种,请填写下列空白:①取少量原溶液,加入过量稀盐酸,有白色沉淀生成,再加入过量稀硝酸,沉淀不消失,说明原溶液中肯定存在的离子是
②取①的滤液加过量的NaOH溶液,出现白色沉淀,说明原溶液中肯定有
③通过以上叙述可知溶液中肯定不存在的离子是
更新时间:2023-03-04 20:02:49
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】室温下部分弱酸的电离平衡常数如表所示。
弱酸 | HCOOH |
|
| HClO | HF |
电离平衡常数(25℃) |
|
|
|
|
|
回答下列问题:
(1)
 在水溶液中的第一步电离方程式为
在水溶液中的第一步电离方程式为 的HCOOH、
的HCOOH、 、
、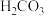 、HClO溶液中
、HClO溶液中 由大到小的顺序为
由大到小的顺序为(2)
 的HClO溶液中
的HClO溶液中 约为
约为 ,少量
,少量 通入NaClO溶液中发生反应的离子方程式为
通入NaClO溶液中发生反应的离子方程式为(3)KHS溶液呈
(4)25℃时,调节
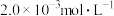 的氢氟酸水溶液的pH(忽略体积变化),得到
的氢氟酸水溶液的pH(忽略体积变化),得到 、
、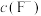 与溶液pH的变化关系如图所示。
与溶液pH的变化关系如图所示。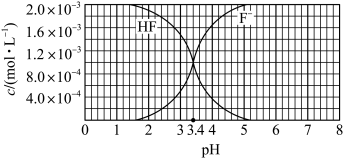
①
②向HF溶液中加入NaOH固体至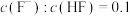 时,
时,
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】已知反应:
①SO3+H2O=H2SO4
②3NO2+H2O=2HNO3+NO
③2F2+2H2O=4HF+O2
④2Na+2H2O=2NaOH+H2↑
⑤Na2O+2HCl=2NaCl+H2O
⑥Al2O3+2NaOH=2NaAlO2+H2O
(1)上述反应不属于氧化还原反应的有___________ (填序号,下同)。H2O被氧化的是___________ ,H2O被还原的是___________ 。
(2)用双线桥法表示反应②的电子转移方向和数目:___________ 。
(3)用单线桥法表示反应③的电子转移方___________ 。
(4)写出反应④的离子方程式:___________ 。
①SO3+H2O=H2SO4
②3NO2+H2O=2HNO3+NO
③2F2+2H2O=4HF+O2
④2Na+2H2O=2NaOH+H2↑
⑤Na2O+2HCl=2NaCl+H2O
⑥Al2O3+2NaOH=2NaAlO2+H2O
(1)上述反应不属于氧化还原反应的有
(2)用双线桥法表示反应②的电子转移方向和数目:
(3)用单线桥法表示反应③的电子转移方
(4)写出反应④的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】根据提供的情境书写指定反应的方程式。
(1)通过如图转化可回收废旧锂电池电极材料 (难溶于水)中钴元素和锂元素。
(难溶于水)中钴元素和锂元素。
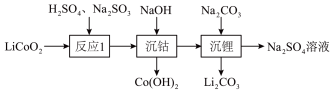
写出反应1的离子方程式:_______ 。
(2)活性自由基 可有效除去废水中的苯酚等有机污染物,原理如图所示。写出
可有效除去废水中的苯酚等有机污染物,原理如图所示。写出 除去苯酚(
除去苯酚( )反应的化学方程式:
)反应的化学方程式:_______ 。

(3)现代工业上用氧化锌烟灰(主要成分为 ,含少量
,含少量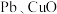 和
和 )制取高纯锌的部分工艺流程如图所示。
)制取高纯锌的部分工艺流程如图所示。
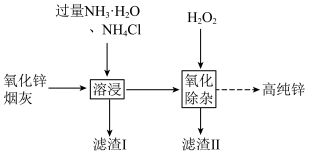
①已知:“溶浸”后浸出液中含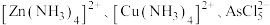 等。写出该过程中生成
等。写出该过程中生成 的相关离子方程式:
的相关离子方程式:_______ 。
②“氧化除杂”的目的是将“ ”转化为
”转化为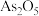 胶体,再经吸附聚沉除去。写出氧化反应的离子方程式:
胶体,再经吸附聚沉除去。写出氧化反应的离子方程式:_______ 。
(1)通过如图转化可回收废旧锂电池电极材料
 (难溶于水)中钴元素和锂元素。
(难溶于水)中钴元素和锂元素。
写出反应1的离子方程式:
(2)活性自由基
 可有效除去废水中的苯酚等有机污染物,原理如图所示。写出
可有效除去废水中的苯酚等有机污染物,原理如图所示。写出 除去苯酚(
除去苯酚( )反应的化学方程式:
)反应的化学方程式:
(3)现代工业上用氧化锌烟灰(主要成分为
 ,含少量
,含少量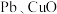 和
和 )制取高纯锌的部分工艺流程如图所示。
)制取高纯锌的部分工艺流程如图所示。
①已知:“溶浸”后浸出液中含
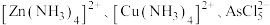 等。写出该过程中生成
等。写出该过程中生成 的相关离子方程式:
的相关离子方程式:②“氧化除杂”的目的是将“
 ”转化为
”转化为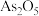 胶体,再经吸附聚沉除去。写出氧化反应的离子方程式:
胶体,再经吸附聚沉除去。写出氧化反应的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】化合物A、B是中学常见的物质,其阴、阳离子只能从下表中选择。
(1)若A、B的水溶液均为无色,且A的水溶液呈强酸性,B的水溶液呈强碱性。混合后产生不溶于稀硝酸的白色沉淀及能使红色石蕊试纸变蓝色的气体。
①B的化学式为________________ ,生成的气体电子式为___________
②A、B溶液混合加热反应的离子方程式___________________________________ 。
(2)若A的水溶液呈浅绿色,B的水溶液无色且其焰色反应为黄色。向A的水溶液中加入稀盐酸无明显现象,再加入B后溶液变黄,但A、B的水溶液混合亦无明显变化。
①A的化学式为________________ 。
②经分析上述过程中溶液变黄的原因可能有两种:I._________________________ 、Ⅱ.____________________________________________ 。(用离子方程式表示)
③请用一简易方法证明上述溶液变黄的原因__________________________________ 。
| 阳离子 | K+、Na+、Fe2+、Ba2+、NH4+ 、Ca2+ |
| 阴离子 | OH–、NO3–、I–、HCO3–、AlO2–、HSO4– |
(1)若A、B的水溶液均为无色,且A的水溶液呈强酸性,B的水溶液呈强碱性。混合后产生不溶于稀硝酸的白色沉淀及能使红色石蕊试纸变蓝色的气体。
①B的化学式为
②A、B溶液混合加热反应的离子方程式
(2)若A的水溶液呈浅绿色,B的水溶液无色且其焰色反应为黄色。向A的水溶液中加入稀盐酸无明显现象,再加入B后溶液变黄,但A、B的水溶液混合亦无明显变化。
①A的化学式为
②经分析上述过程中溶液变黄的原因可能有两种:I.
③请用一简易方法证明上述溶液变黄的原因
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】有一瓶澄清的溶液,其中可能含有NH4+、K+、Na+、Mg2+、Ba2+、Al3+、Fe3+、Cl-、I-、 NO3-、CO32-、SO42-中的几种,取该溶液进行以下实验:
(1)取pH试纸检验,溶液呈强酸性;
(2)取出部分溶液,加入少量CCl4及数滴新制氯水,经振荡后CCl4层呈紫红色;
(3)另取出部分溶液,逐渐加入NaOH溶液,使溶液从酸性逐渐变为碱性,在滴加过程中和滴加完毕后,溶液均无沉淀产生;
(4)取出部分上述碱性溶液加Na2CO3溶液后,有白色沉淀生成;
(5)根据以上实验事实确定①该溶液肯定存在的离子是__________________________ ;②肯定不存在的离子是_____________________________ ;③还不能确定的离子是________________________ ,要确定其中的阳离子可利用的方法原理是________________ 。
(1)取pH试纸检验,溶液呈强酸性;
(2)取出部分溶液,加入少量CCl4及数滴新制氯水,经振荡后CCl4层呈紫红色;
(3)另取出部分溶液,逐渐加入NaOH溶液,使溶液从酸性逐渐变为碱性,在滴加过程中和滴加完毕后,溶液均无沉淀产生;
(4)取出部分上述碱性溶液加Na2CO3溶液后,有白色沉淀生成;
(5)根据以上实验事实确定①该溶液肯定存在的离子是
您最近一年使用:0次
【推荐1】A、B、C、D 4种可溶性盐,它们的阳离子可能分别是 、
、 、
、 、
、 中的某一种,阴离子可能分别是
中的某一种,阴离子可能分别是 、
、 、
、 、
、 中的某一种。
中的某一种。
①若把4种盐分别溶解于盛有蒸馏水的4支试管中,均得澄清溶液,只有B盐的溶液呈蓝色。
②若向①的4支试管中分别加盐酸,C溶液中有沉淀产生,A溶液中有无色无味气体逸出。
(1)根据①②的事实推断B、C的化学式分别为_______ 、_______
(2)写出A与D反应的离子方程式:_______ ;
(3)若想从A与D反应后的混合物中分别提取两种固体产物,需要进行的实验操作是_______ 和_______
 、
、 、
、 、
、 中的某一种,阴离子可能分别是
中的某一种,阴离子可能分别是 、
、 、
、 、
、 中的某一种。
中的某一种。①若把4种盐分别溶解于盛有蒸馏水的4支试管中,均得澄清溶液,只有B盐的溶液呈蓝色。
②若向①的4支试管中分别加盐酸,C溶液中有沉淀产生,A溶液中有无色无味气体逸出。
(1)根据①②的事实推断B、C的化学式分别为
(2)写出A与D反应的离子方程式:
(3)若想从A与D反应后的混合物中分别提取两种固体产物,需要进行的实验操作是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】若四种溶液,分别含有: ①Al3+ ②Mg2+ ③Fe2+ ④Fe3+ 离子。请回答下列问题:
(1)遇KSCN溶液呈红色的是_________ 。
(2)加铁粉溶液质量增重的是__________ 。
(3)加入过量NaOH溶液中最终无沉淀的是______________ 。
(4)加入新制Cl2水溶液变黄色的是_____________ ,反应的离子方程式是_______________ 。
(1)遇KSCN溶液呈红色的是
(2)加铁粉溶液质量增重的是
(3)加入过量NaOH溶液中最终无沉淀的是
(4)加入新制Cl2水溶液变黄色的是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】某无色溶液只可能含有下列离子Na+、Ba2+、Cu2+、CO 、Cl﹣、Mg2+中的某些离子。①向此溶液中滴加稀盐酸无明显现象。②取少量①的溶液并加入少量的Na2SO4溶液,有白色沉淀产生。③取②的上层清液并加入过量的NaOH溶液,无明显现象。
、Cl﹣、Mg2+中的某些离子。①向此溶液中滴加稀盐酸无明显现象。②取少量①的溶液并加入少量的Na2SO4溶液,有白色沉淀产生。③取②的上层清液并加入过量的NaOH溶液,无明显现象。
(1)应最先判断出溶液中一定不含有哪种离子______ ,说明判断的理由____________ 。由步骤①可判断原溶液中一定不含有的离子是______ ,说明判断的理由____________ 。
(2)②中反应的离子方程式为________ 。不能确定是否含有的离子是______ 。
 、Cl﹣、Mg2+中的某些离子。①向此溶液中滴加稀盐酸无明显现象。②取少量①的溶液并加入少量的Na2SO4溶液,有白色沉淀产生。③取②的上层清液并加入过量的NaOH溶液,无明显现象。
、Cl﹣、Mg2+中的某些离子。①向此溶液中滴加稀盐酸无明显现象。②取少量①的溶液并加入少量的Na2SO4溶液,有白色沉淀产生。③取②的上层清液并加入过量的NaOH溶液,无明显现象。(1)应最先判断出溶液中一定不含有哪种离子
(2)②中反应的离子方程式为
您最近一年使用:0次





 的操作方法
的操作方法

