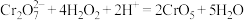硫化氢与浓硫酸的反应为3H2S+H2SO4=4S↓+4H2O,下列说法正确的是
| A.硫化氢气体被氧化成硫 | B.硫酸被氧化成硫 |
| C.硫酸被还原成水 | D.硫化氢气体被还原成水 |
18-19高一下·甘肃武威·期中 查看更多[3]
辽宁省建平县实验中学2023-2024学年高一上学期11月期中化学试题(已下线)专题05 化学反应与能量——备战2021年高考化学纠错笔记甘肃省武威第十八中学2018-2019学年高一下学期期中考试化学试题
更新时间:2019-06-11 14:58:37
|
相似题推荐
单选题
|
较难
(0.4)
名校
【推荐1】利用铜-铈氧化物( ,Ce是活泼金属)催化氧化除去
,Ce是活泼金属)催化氧化除去 中少量CO的可能机理如图所示。下列说法正确的是
中少量CO的可能机理如图所示。下列说法正确的是
 ,Ce是活泼金属)催化氧化除去
,Ce是活泼金属)催化氧化除去 中少量CO的可能机理如图所示。下列说法正确的是
中少量CO的可能机理如图所示。下列说法正确的是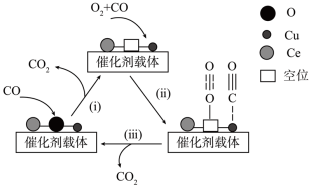
| A.反应(iii)中Cu、Ce化合价均未改变 |
| B.反应一段时间后催化剂活性下降,可能是CuO被还原成Cu所致 |
C.若用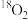 参与反应,一段时间后, 参与反应,一段时间后,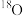 不可能出现在铜-铈氧化物中 不可能出现在铜-铈氧化物中 |
D.铜-铈氧化物减小了反应 的反应热 的反应热 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】酸性溶液中过氧化氢能使Cr2O72-转化成蓝色的过氧化铬(CrO5,分子结构为 ),该反应可用来检验Cr2O72-的存在,其反应的离子方程式为4H2O2+Cr2O72-+2H+===2CrO5+5H2O。下列说法正确的是
),该反应可用来检验Cr2O72-的存在,其反应的离子方程式为4H2O2+Cr2O72-+2H+===2CrO5+5H2O。下列说法正确的是
 ),该反应可用来检验Cr2O72-的存在,其反应的离子方程式为4H2O2+Cr2O72-+2H+===2CrO5+5H2O。下列说法正确的是
),该反应可用来检验Cr2O72-的存在,其反应的离子方程式为4H2O2+Cr2O72-+2H+===2CrO5+5H2O。下列说法正确的是| A.过氧化铬中铬元素的化合价为+5 | B.该反应为非氧化还原反应 |
| C.该反应中Cr2O72-发生还原反应 | D.该反应中H2O2表现了还原性 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐1】已知 (B为+3价)溶于水并和水发生反应
(B为+3价)溶于水并和水发生反应 ,下列说法中正确的是
,下列说法中正确的是
 (B为+3价)溶于水并和水发生反应
(B为+3价)溶于水并和水发生反应 ,下列说法中正确的是
,下列说法中正确的是A. 是氧化剂, 是氧化剂, 是还原剂。 是还原剂。 |
| B.被氧化的元素与被还原的元素质量比为1:1 |
| C.硼元素被氧化,氢元素被还原。 |
D. 既是氧化剂又是还原剂 既是氧化剂又是还原剂 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】高铁酸钾K2FeO4是一种新型、高效、氧化性比Cl2更强的水处理剂,工业上通常用下列反应先制得高铁酸钠:2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑,然后在某低温下,在高铁酸钠溶液中加KOH固体至饱和就可析出高铁酸钾。下列说法不正确的是
| A. Na2O2在反应中既作氧化剂,又作还原剂 |
| B.制取高铁酸钠时,每生成1mol Na2FeO4反应中共有4mol电子转移 |
| C.高铁酸钾在该温度下的溶解度比高铁酸钠的溶解度小 |
| D. K2FeO4能消毒杀菌,其还原产物水解生成的Fe(OH)3胶体能吸附水中的悬浮杂质 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】某离子反应涉及H2O、Cr2O72-、NO2-、H+、NO3-、Cr 六种微粒,氧化剂和还原剂的物质的量之比为1:3。下列判断错误的是:
六种微粒,氧化剂和还原剂的物质的量之比为1:3。下列判断错误的是:
 六种微粒,氧化剂和还原剂的物质的量之比为1:3。下列判断错误的是:
六种微粒,氧化剂和还原剂的物质的量之比为1:3。下列判断错误的是:| A.反应的氧化产物是NO3- |
B.反应过程中溶液pH变化如图所示 |
| C.消耗l mol氧化剂,转移电子6 mol |
D.反应中Cr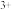 被氧化 被氧化 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】AlN广泛应用于电子、陶瓷等工业领域。在一定条件下,AlN可通过反应Al2O3+N2+3C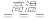 2AlN+3CO合成。下列叙述
2AlN+3CO合成。下列叙述正确 的是( )
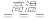 2AlN+3CO合成。下列叙述
2AlN+3CO合成。下列叙述| A.AlN为氧化产物 |
| B.AlN的摩尔质量为41g |
| C.上述反应中,每生成1molAlN需转移3mol电子 |
| D.上述反应中,N2是还原剂,Al2O3是氧化剂 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐3】氧化还原反应在日常生活中有着广泛的应用,下列有关说法正确的是
| 选项 | 化学反应方程式 | 相关说法 |
| A | H2S+4O2F2 SF6+2HF+4O2 SF6+2HF+4O2 | 氧气是氧化产物,O2F2是氧化剂又是还原剂 |
| B | Cl2+2Br-=2Cl-+Br2 Zn+Cu2+=Zn2++Cu | 均为单质被还原的置换反应 |
| C | 4Fe2++4Na2O2+6H2O=4Fe(OH)3↓+O2↑+8Na+ | 若Fe2+失去4mol电子,生成氧气的体积约为22.4L |
| D | HNCO+NOx N2+CO2+H2O N2+CO2+H2O | 若NOx中x=2,1mol NO2在反应中转移4NA个电子 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次

 )的结构为
)的结构为 。
。