氯元素原子结构示意图为______ ,其与钠元素组成的化合物的电子式为_____ 。
更新时间:2019-06-23 01:04:12
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】请回答下列问题:
(1)某元素原子M层电子数是K、L层电子数之和的一半,该原子的结构示意图是___________ 。
(2)某种粒子有1个原子核,核中有17个质子,20个中子,核外有18个电子,该粒子的化学符号是___________ 。
(3)某分子中有5个原子核,共有10个电子,这种分子的结构式是___________ 。
(4)CaC2是离子化合物,含有Ca2+和C 两种离子,其中C
两种离子,其中C 的电子式
的电子式___________ 。
(1)某元素原子M层电子数是K、L层电子数之和的一半,该原子的结构示意图是
(2)某种粒子有1个原子核,核中有17个质子,20个中子,核外有18个电子,该粒子的化学符号是
(3)某分子中有5个原子核,共有10个电子,这种分子的结构式是
(4)CaC2是离子化合物,含有Ca2+和C
 两种离子,其中C
两种离子,其中C 的电子式
的电子式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】为纪念元素周期表诞生150周年,IUPAC等向世界介绍118位优秀青年化学家,并形成一张“青年化学家元素周期表”。中国学者雷晓光、姜雪峰、刘庄分别成为“N、S、Hg”元素的代言人。回答下列问题:
(1)请补全汞的原子结构示意图___________ 。

(2)自然界的水银内含7种核素: 、
、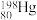 、
、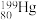 、
、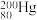 、
、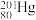 、
、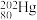 和
和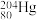 ,其中,
,其中,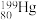 和
和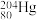 的中子数之比为
的中子数之比为___________ 。
(3)硫磺可用于制作黑火药,爆炸时的反应为: 。
。
①用电子式表示 的形成过程
的形成过程___________ ;
②烟花爆竹的成分中除了加火药,常加入一些金属元素,若燃放烟花的火焰呈现黄色,则烟花中可能含有___________ 元素(填名称)。
(4)氮、磷、砷都是第VA族元素,下列说法正确的是___________ (填字母)。
a.非金属性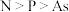 ,所以氮气最活泼
,所以氮气最活泼
b. 与
与 性质相似,
性质相似, 能与
能与 溶液反应
溶液反应
c.As的最高价氧化物对应的水化物是强酸
d.形成的简单氢化物的还原性随着原子序数递增而增强
(1)请补全汞的原子结构示意图

(2)自然界的水银内含7种核素:
 、
、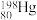 、
、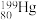 、
、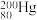 、
、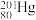 、
、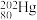 和
和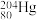 ,其中,
,其中,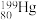 和
和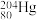 的中子数之比为
的中子数之比为(3)硫磺可用于制作黑火药,爆炸时的反应为:
 。
。①用电子式表示
 的形成过程
的形成过程②烟花爆竹的成分中除了加火药,常加入一些金属元素,若燃放烟花的火焰呈现黄色,则烟花中可能含有
(4)氮、磷、砷都是第VA族元素,下列说法正确的是
a.非金属性
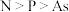 ,所以氮气最活泼
,所以氮气最活泼b.
 与
与 性质相似,
性质相似, 能与
能与 溶液反应
溶液反应c.As的最高价氧化物对应的水化物是强酸
d.形成的简单氢化物的还原性随着原子序数递增而增强
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】新型陶瓷材料氮化硅(Si3N4)可用于制作火箭发动机中燃料的喷嘴。氮化硅可由石英、焦炭在高温氮气流中制取。完成下列填空:
SiO2 +______C +_____N2 ______Si3N4 + ________CO
______Si3N4 + ________CO
(1)试配平该化学反应方程式,在方程式上标出电子转移的方向和数目_____ 。
(2)反应中___________ 被还原,当氧化产物比还原产物多1mol时,反应中电子转移数为___________ 。
(3)在该反应体系中:所涉及物质属于单质的电子式为___________ ;所涉及元素中原子半径最大的原子的结构示意图为___________ 。
SiO2 +______C +_____N2
 ______Si3N4 + ________CO
______Si3N4 + ________CO(1)试配平该化学反应方程式,在方程式上标出电子转移的方向和数目
(2)反应中
(3)在该反应体系中:所涉及物质属于单质的电子式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】PtRu@Pd纳米核壳材料是氢能源燃料电池的重要催化剂。某研究团队提出一种可重复制备该催化剂的方案,步骤如下:
步骤一、在95℃下,将 溶液加入一定量十六烷基三甲基溴化铵(
溶液加入一定量十六烷基三甲基溴化铵(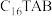 )水溶液中。
)水溶液中。
步骤二、向混合溶液中逐渐加入一定量 的碱性水溶液,持续搅拌30分钟,离心分离,多次洗涤,得到Pd纳米颗粒。
的碱性水溶液,持续搅拌30分钟,离心分离,多次洗涤,得到Pd纳米颗粒。
步骤三、将所得Pd纳米颗粒分散在超纯水中,添加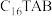 后搅拌。加入特定组成的PtRu前体,再加入
后搅拌。加入特定组成的PtRu前体,再加入 的碱性水溶液,80℃下搅拌3小时,离心洗涤后得到PtRu@Pd纳米核壳材料(如图a)。
的碱性水溶液,80℃下搅拌3小时,离心洗涤后得到PtRu@Pd纳米核壳材料(如图a)。
已知:十六烷基三甲基溴化铵(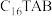 )是一种表面活性剂,其工作原理如图b所示:
)是一种表面活性剂,其工作原理如图b所示:
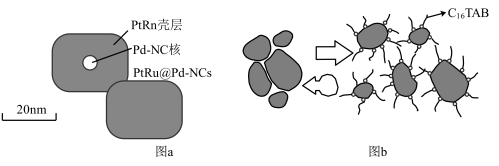
回答下列问题:
(1)配制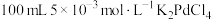 溶液所需的玻璃仪器有量筒、烧杯、玻璃棒、
溶液所需的玻璃仪器有量筒、烧杯、玻璃棒、_______ 。
(2) 的电子式为
的电子式为_______ ;配平并完成 与
与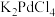 反应制备纳米Pd的离子方程式:
反应制备纳米Pd的离子方程式:_______ 。 其中
其中 可用以下
可用以下_______ 代替(填标号)。
A.亚硫酸钾 B.氯水 C.硝酸 D.维生素C
(3)步骤二中多次洗涤的目的是为了得到纯净的Pd纳米颗粒,检验其洗净的方法是_______ 。
(4)步骤三中保持温度为80℃的方法是_______ 。
(5)在整个过程中,十六烷基三甲基溴化铵(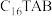 )的作用是
)的作用是_______ 。
步骤一、在95℃下,将
 溶液加入一定量十六烷基三甲基溴化铵(
溶液加入一定量十六烷基三甲基溴化铵(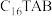 )水溶液中。
)水溶液中。步骤二、向混合溶液中逐渐加入一定量
 的碱性水溶液,持续搅拌30分钟,离心分离,多次洗涤,得到Pd纳米颗粒。
的碱性水溶液,持续搅拌30分钟,离心分离,多次洗涤,得到Pd纳米颗粒。步骤三、将所得Pd纳米颗粒分散在超纯水中,添加
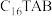 后搅拌。加入特定组成的PtRu前体,再加入
后搅拌。加入特定组成的PtRu前体,再加入 的碱性水溶液,80℃下搅拌3小时,离心洗涤后得到PtRu@Pd纳米核壳材料(如图a)。
的碱性水溶液,80℃下搅拌3小时,离心洗涤后得到PtRu@Pd纳米核壳材料(如图a)。已知:十六烷基三甲基溴化铵(
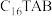 )是一种表面活性剂,其工作原理如图b所示:
)是一种表面活性剂,其工作原理如图b所示:
回答下列问题:
(1)配制
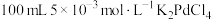 溶液所需的玻璃仪器有量筒、烧杯、玻璃棒、
溶液所需的玻璃仪器有量筒、烧杯、玻璃棒、(2)
 的电子式为
的电子式为 与
与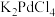 反应制备纳米Pd的离子方程式:
反应制备纳米Pd的离子方程式: 其中
其中 可用以下
可用以下A.亚硫酸钾 B.氯水 C.硝酸 D.维生素C
(3)步骤二中多次洗涤的目的是为了得到纯净的Pd纳米颗粒,检验其洗净的方法是
(4)步骤三中保持温度为80℃的方法是
(5)在整个过程中,十六烷基三甲基溴化铵(
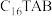 )的作用是
)的作用是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】利用如图所示的“价-类”二维图,可以从物质类别、化合价角度认识含氯元素的物质的性质及其转化关系,图中甲~辛均为含氯元素的物质。回答下列问题:
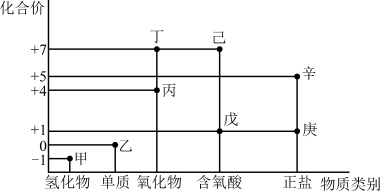
(1)将新制乙的水溶液滴加几滴到干燥的有色纸条上观察到的现象是_____ 。
(2)戊的结构式为______ ;甲、乙、丙、戊中,属于非电解质的是______ (填化学式)。
(3)丙是目前国际上公认的新一代的高效、广谱、安全的杀菌、保鲜剂,丙在杀菌消毒过程中会产生副产物亚氯酸盐(ClO ),需将其转化为Cl-除去。下列试剂中,可将ClO
),需将其转化为Cl-除去。下列试剂中,可将ClO 转化为Cl-的是
转化为Cl-的是_____ (填字母序号)。
a.Fe2(SO4)3 b.HClO4 c.SO2 d.KMnO4
(4)庚是“84”消毒液的有效成分,能有效灭菌,某化学社团模拟生产厂家配制了500mL“84消毒液”,并在瓶体贴上标签,如图所示,回答下列问题:
①写出氯气和NaOH溶液生产此消毒液的离子方程式______ ;该“84消毒液”有效成分的物质的量浓度为_____ (结果保留1位小数)。
②“84消毒液”与稀硫酸混合使用可增强消毒能力,该社团成员用18.0mol/L的浓硫酸配制90mL 0.90mol/L的稀硫酸用于增强“84消毒液”的消毒能力,需要量取上述浓硫酸的体积为_____ mL(结果保留1位小数).若所配制的稀硫酸浓度大于0.90mol/L,则可能的原因是_____ 。
A.配制前,容量瓶未干燥
B.用量筒量取浓硫酸时,仰视刻度线取浓硫酸
C.浓硫酸溶解后未恢复到室温,立即转移至容量瓶定容
D.转移硫酸溶液至容量瓶时,有少量溶液溅出
E.定容时,仰视容量瓶刻度线进行定容

(1)将新制乙的水溶液滴加几滴到干燥的有色纸条上观察到的现象是
(2)戊的结构式为
(3)丙是目前国际上公认的新一代的高效、广谱、安全的杀菌、保鲜剂,丙在杀菌消毒过程中会产生副产物亚氯酸盐(ClO
 ),需将其转化为Cl-除去。下列试剂中,可将ClO
),需将其转化为Cl-除去。下列试剂中,可将ClO 转化为Cl-的是
转化为Cl-的是a.Fe2(SO4)3 b.HClO4 c.SO2 d.KMnO4
(4)庚是“84”消毒液的有效成分,能有效灭菌,某化学社团模拟生产厂家配制了500mL“84消毒液”,并在瓶体贴上标签,如图所示,回答下列问题:
| 84消毒液 有效成分 NaClO 规格 500mL 质量分数 25% 密度 1.19g•cm-3 |
②“84消毒液”与稀硫酸混合使用可增强消毒能力,该社团成员用18.0mol/L的浓硫酸配制90mL 0.90mol/L的稀硫酸用于增强“84消毒液”的消毒能力,需要量取上述浓硫酸的体积为
A.配制前,容量瓶未干燥
B.用量筒量取浓硫酸时,仰视刻度线取浓硫酸
C.浓硫酸溶解后未恢复到室温,立即转移至容量瓶定容
D.转移硫酸溶液至容量瓶时,有少量溶液溅出
E.定容时,仰视容量瓶刻度线进行定容
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】用化学用语回答下列问题
(1)写出二氧化碳分子的电子式___________ ;写出氮气分子的结构式___________ 。
(2)A+、B-、C、D四种粒子(分子或离子),它们都分别含10个电子,已知它们有如下转化关系:A++B- C+D,则A的电子式
C+D,则A的电子式___________ 。比较C和D的稳定性的强弱∶___________ (用化学式表示)。
(3)用电子式表示MgCl2的形成过程___________
(4)①CaBr2;②H2O;③NH4Cl;④H2O2;⑤Na2O2;⑥Ca(OH)2;⑦HClO;⑧I2;⑨He;只含有离子键的是(用序号回答)___________ ,含有共价键的离子化合物是(用序号回答)___________ ,含有非极性共价键的共价化合物是(用序号回答)___________ ,常温时为固体,当其熔化时,不破坏化学键的是(用序号回答)___________ 。
(1)写出二氧化碳分子的电子式
(2)A+、B-、C、D四种粒子(分子或离子),它们都分别含10个电子,已知它们有如下转化关系:A++B-
 C+D,则A的电子式
C+D,则A的电子式(3)用电子式表示MgCl2的形成过程
(4)①CaBr2;②H2O;③NH4Cl;④H2O2;⑤Na2O2;⑥Ca(OH)2;⑦HClO;⑧I2;⑨He;只含有离子键的是(用序号回答)
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】(1)写出下列物质的电子式: HClO_____________ ;
(2)用电子式表示下列物质的形成过程:MgCl2___________________ 。
(2)用电子式表示下列物质的形成过程:MgCl2
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】按要求回答下列问题:
(1)某种粒子有1个原子核,核中有17个质子,20个中子,核外有18个电子,该粒子的化学符号是______________ 。
(2)现有下列物质:①H2 ②Na2O2 ③NaOH ④H2O2 ⑤CaCl2 ⑥NH4NO3 ⑦H2S。只由离子键构成的物质是_________ ;只由极性共价键构成的物质是_____ ;由极性键和非极性键构成的物质是_______ ;由离子键和极性键构成的物质是_______ 。(填序号)。
(3)写出下列物质的电子式:CaF2:______________ CO2:______________ NH4Cl:________________ 。
(4) 用电子式表示下列化合物的形成过程:H2S:__________________________________ ;MgCl2:_____________________________ 。
(1)某种粒子有1个原子核,核中有17个质子,20个中子,核外有18个电子,该粒子的化学符号是
(2)现有下列物质:①H2 ②Na2O2 ③NaOH ④H2O2 ⑤CaCl2 ⑥NH4NO3 ⑦H2S。只由离子键构成的物质是
(3)写出下列物质的电子式:CaF2:
(4) 用电子式表示下列化合物的形成过程:H2S:
您最近一年使用:0次



