按要求回答下列问题:
(1)某种粒子有1个原子核,核中有17个质子,20个中子,核外有18个电子,该粒子的化学符号是______________ 。
(2)现有下列物质:①H2 ②Na2O2 ③NaOH ④H2O2 ⑤CaCl2 ⑥NH4NO3 ⑦H2S。只由离子键构成的物质是_________ ;只由极性共价键构成的物质是_____ ;由极性键和非极性键构成的物质是_______ ;由离子键和极性键构成的物质是_______ 。(填序号)。
(3)写出下列物质的电子式:CaF2:______________ CO2:______________ NH4Cl:________________ 。
(4) 用电子式表示下列化合物的形成过程:H2S:__________________________________ ;MgCl2:_____________________________ 。
(1)某种粒子有1个原子核,核中有17个质子,20个中子,核外有18个电子,该粒子的化学符号是
(2)现有下列物质:①H2 ②Na2O2 ③NaOH ④H2O2 ⑤CaCl2 ⑥NH4NO3 ⑦H2S。只由离子键构成的物质是
(3)写出下列物质的电子式:CaF2:
(4) 用电子式表示下列化合物的形成过程:H2S:
更新时间:2020-01-02 17:19:18
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】I.碘(Ⅰ)在元素周期表中位于ⅦA族,是人体必需的微量元素之一。
(1)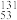 I可用于治疗甲亢。
I可用于治疗甲亢。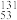 I的原子核内中子数为
I的原子核内中子数为_____ 。
(2)①碘元素的非金属性比氯元素的非金属性弱,其原因是同主族元素从上到下原子核外电子层数依次增多,_____ 逐渐增大,______ 能力逐渐减弱。
②下列事实能够用“碘的非金属性比氯的弱”来解释的是_____ (填序号)。
a.碘单质的熔点高于氯单质
b.高氯酸的酸性强于高碘酸
c.Cl2比I2更容易与H2化合
Ⅱ.已知某短周期元素的氧化物为RO2。根据下列信息,回答相关问题:
(3)实现“碳达峰和碳中和”的一种有效措施是开发高效催化剂电还原RO2制备高附加值的产品,RO2的结构式为_____ 。
(4)若RO2常用于制造光导纤维。工业上,常用焦炭作还原剂以RO2为原料制备R单质,则该反应的氧化产物是_____ (填化学式)。
Ⅲ.回答下列问题:
(5)察尔汗盐湖是世界上最著名的内陆盐湖之一。通常通过煮盐湖水得到的是粗盐,粗盐除含NaCl外,还含有少量MgCl2、CaCl2、Na2SO4以及泥沙等杂质,工业上需要进一步提纯,若要除去粗盐中杂质Na2SO4选择加入的试剂是:_____ (填化学式),所涉及的离子反应为:______ 。
(1)
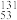 I可用于治疗甲亢。
I可用于治疗甲亢。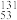 I的原子核内中子数为
I的原子核内中子数为(2)①碘元素的非金属性比氯元素的非金属性弱,其原因是同主族元素从上到下原子核外电子层数依次增多,
②下列事实能够用“碘的非金属性比氯的弱”来解释的是
a.碘单质的熔点高于氯单质
b.高氯酸的酸性强于高碘酸
c.Cl2比I2更容易与H2化合
Ⅱ.已知某短周期元素的氧化物为RO2。根据下列信息,回答相关问题:
(3)实现“碳达峰和碳中和”的一种有效措施是开发高效催化剂电还原RO2制备高附加值的产品,RO2的结构式为
(4)若RO2常用于制造光导纤维。工业上,常用焦炭作还原剂以RO2为原料制备R单质,则该反应的氧化产物是
Ⅲ.回答下列问题:
(5)察尔汗盐湖是世界上最著名的内陆盐湖之一。通常通过煮盐湖水得到的是粗盐,粗盐除含NaCl外,还含有少量MgCl2、CaCl2、Na2SO4以及泥沙等杂质,工业上需要进一步提纯,若要除去粗盐中杂质Na2SO4选择加入的试剂是:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】已知氮元素及其化合物的转化关系如下图所示,回答下列问题。
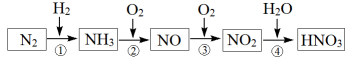
(1)氮气用于工业合成氨,写出氮气的电子式_______ ;
(2)①~④各步转化中,属于氮的固定的是_______ (填序号)。
(3)实验室常用加热氯化铵和氢氧化钙固体混合物的方法制取氨气。
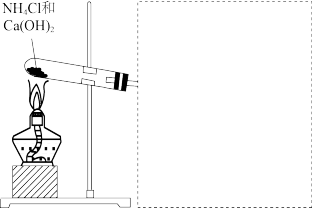
①化学方程式是_______ 。
②在图中方框内绘制用小试管 收集氨气的装置图__________ 。
(4)工业上用氨气制备NO的化学方程式是_______ 。
(5)工业制硝酸时尾气中含有NO、 ,可用NaOH溶液吸收,发生的反应有:
,可用NaOH溶液吸收,发生的反应有:
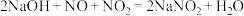
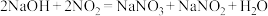
用不同浓度的NaOH溶液吸收 含量不同的尾气,关系如下图:(
含量不同的尾气,关系如下图:( 表示尾气里NO、
表示尾气里NO、 中
中 的含量)
的含量)

i.根据上图得知_______ (填字母)。
a.NaOH溶液浓度越大,氮氧化物的吸收率越大
b. 含量越大,氮氧化物的吸收率越大
含量越大,氮氧化物的吸收率越大
ii.当α小于50%时,加入 能提升氮氧化物的吸收率,原因是
能提升氮氧化物的吸收率,原因是_______ 。
(6)在微生物作用下,蛋白质在水中分解产生的氨能够被氧气氧化生成亚硝酸( ),反应的化学方程式为
),反应的化学方程式为_______ 。若反应中有0.3mol电子发生转移时,生成亚硝酸的质量为_______ g(小数点后保留两位有效数字)。

(1)氮气用于工业合成氨,写出氮气的电子式
(2)①~④各步转化中,属于氮的固定的是
(3)实验室常用加热氯化铵和氢氧化钙固体混合物的方法制取氨气。

①化学方程式是
②在图中方框内绘制用
(4)工业上用氨气制备NO的化学方程式是
(5)工业制硝酸时尾气中含有NO、
 ,可用NaOH溶液吸收,发生的反应有:
,可用NaOH溶液吸收,发生的反应有: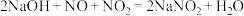
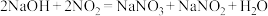
用不同浓度的NaOH溶液吸收
 含量不同的尾气,关系如下图:(
含量不同的尾气,关系如下图:( 表示尾气里NO、
表示尾气里NO、 中
中 的含量)
的含量)
i.根据上图得知
a.NaOH溶液浓度越大,氮氧化物的吸收率越大
b.
 含量越大,氮氧化物的吸收率越大
含量越大,氮氧化物的吸收率越大ii.当α小于50%时,加入
 能提升氮氧化物的吸收率,原因是
能提升氮氧化物的吸收率,原因是(6)在微生物作用下,蛋白质在水中分解产生的氨能够被氧气氧化生成亚硝酸(
 ),反应的化学方程式为
),反应的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】现有①BaCl2、②金刚石、③KOH、④Na2SO4、⑤干冰、⑥碘片六种物质,按下列要求回答:
(1)熔化时不需要破坏化学键的是__ (填写物质的序号,下同),熔化时需要破坏共价键的是___ 。
(2)属于离子化合物的是____ ,只有离子键的物质是___ 。
(1)熔化时不需要破坏化学键的是
(2)属于离子化合物的是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】元素周期律
基于元素之间具有内在联系的思想,通过对元素性质及其关系的探寻,元素周期律已成为将物质组成元素性质以及原子结构建立联系的连接点。
(1)下列不属于主族元素的是________
(2) 的电子式正确的是________
的电子式正确的是________
(3)有关N、O两种元素,下列排序错误的是________
(4)甲~戊均为短周期元素,在元素周期表中的相对位置如图所示。戊的最高价氧化物对应的水化物为强酸。下列说法不正确的是________
基于元素之间具有内在联系的思想,通过对元素性质及其关系的探寻,元素周期律已成为将物质组成元素性质以及原子结构建立联系的连接点。
(1)下列不属于主族元素的是________
A. | B. | C. | D. |
 的电子式正确的是________
的电子式正确的是________A.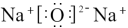 | B. |
C.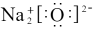 | D. |
| A.元素的最高化合价:O>N | B.简单氢化物的稳定性: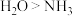 |
| C.元素的电负性:O>N | D.离子半径: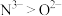 |
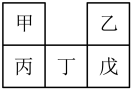
| A.原子半径:丁>戊>乙 |
| B.非金属性:戊>丁>丙 |
| C.甲的氢化物遇氯化氢一定有白烟产生 |
| D.丙的最高价氧化物对应的水化物一定能与强碱反应 |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】下列物质中:①MgCl2 ②HD ③Na2O2 ④H2O ⑤NaCl ⑥Ne ⑦H2SO4 ⑧NH4Cl ⑨CO2 ⑩O2(用序号填空)
(1)只含离子键的是____ ,既含离子键又含共价键的是____ ,不存在化学键的是_____ 。
(2)属于离子化合物的是____ ,属于共价化合物的是______ 。
(1)只含离子键的是
(2)属于离子化合物的是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】I.下图是碳和水蒸气发生反应生成CO、H2的途径和三个状态的能量,该反应为吸热反应,试问:
(1)步骤1、2分别是吸热过程还是放热过程?步骤1:________ ,步骤2:________ 。
(2)比较E1、E2、E3的大小:____________________ 。
II. 下列变化 ①碘的升华 ②烧碱熔化 ③氯化钠溶于水 ④氯化氢溶于水 ⑤氧气溶于水 ⑥氯化铵受热分解。
(1)未发生化学键破坏的是__________ ;(填序号,下同)仅发生离子键破坏的是______________ ;
(2)若上述物质都为纯净物时,属于共价化合物的是_______ ;属于离子化合物的是__________ ;
III. 写出下列物质的电子式:
S_______ CsOH_______ CO2_________
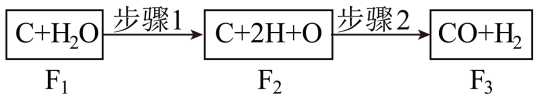
(1)步骤1、2分别是吸热过程还是放热过程?步骤1:
(2)比较E1、E2、E3的大小:
II. 下列变化 ①碘的升华 ②烧碱熔化 ③氯化钠溶于水 ④氯化氢溶于水 ⑤氧气溶于水 ⑥氯化铵受热分解。
(1)未发生化学键破坏的是
(2)若上述物质都为纯净物时,属于共价化合物的是
III. 写出下列物质的电子式:
S
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】填空。
(1)有下列物质:He、N2、CaO、H2SO4、Na2S、KOH、NaHCO3。
①其中只含共价键的是___________ ;
②只含离子键的是___________ ;
③既含有共价键又含有离子键的是___________ ;
④属于共价化合物的是___________ ;
⑤属于离子化合物的是___________ 。
(2)下列变化中,不需要破坏化学键的是___________(填字母)。
(1)有下列物质:He、N2、CaO、H2SO4、Na2S、KOH、NaHCO3。
①其中只含共价键的是
②只含离子键的是
③既含有共价键又含有离子键的是
④属于共价化合物的是
⑤属于离子化合物的是
(2)下列变化中,不需要破坏化学键的是___________(填字母)。
| A.硫酸与氢氧化钠反应 | B.加热氯酸钾使其分解 |
| C.冰融化 | D.氯化钠溶于水 |
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】从结构上看,大部分酸是___________ 化合物,而大部分碱是___________ 化合物,大部分盐是___________ 化合物,而氧化物___________ 。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】无机物可根据其组成和性质进行分类。现有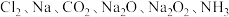 六种物质,完成下列填空:
六种物质,完成下列填空:
(1)由分子构成的单质是
(2)既有离子键又有共价键的物质的电子式为
(3)上述化合物中组成元素的原子半径由大到小的顺序是
(4)
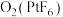 是离子化合物,其中
是离子化合物,其中 为
为 价。正确判断是___________。
价。正确判断是___________。| A.常温下为固体 | B.不存在共价键 | C.属于极性分子 | D.由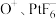 构成 构成 |
您最近一年使用:0次

 的电子式是
的电子式是 分子的空间结构为
分子的空间结构为 粉末中混有的少量
粉末中混有的少量 ,所涉及的反应的化学方程式为
,所涉及的反应的化学方程式为 溶液中加入
溶液中加入 溶液时观察到的现象是
溶液时观察到的现象是

