Ⅰ书写下列物质的电子式:
O2:______________ N2:____________ .Cl2:______________ H2O:____________ . NaOH:___________ Na2O2:___________ .
Ⅱ 写出下列电极反应式:
(1)碱性锌锰电池负极反应式:____________________________________ .
(2)铅蓄电池的负极反应式:___________________________________________ .
(3)氢氧燃料电池酸性介质的负极反应式:_______________________________ .正极反应式:_______________________________ .
O2:
Ⅱ 写出下列电极反应式:
(1)碱性锌锰电池负极反应式:
(2)铅蓄电池的负极反应式:
(3)氢氧燃料电池酸性介质的负极反应式:
更新时间:2019-06-24 15:03:44
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】按照组成元素可将有机物分为烃和烃的衍生物。
I.某些烃分子的模型如图所示
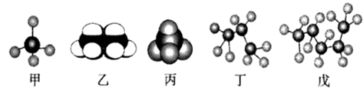
回答下列问题:
(1)等质量的上述烃,完全燃烧时耗氧量最多的是___________ (填分子式)。
(2)25℃时,10mL某气态烃和50mL氧气混合,完全燃烧后恢复到原来的温度和压强,体积变为35mL,则该烚可能为___________。
II.烃可以通过化学反应制得烃的衍生物,例如由丙烯可以制得丙烯酸(CH2=CHCOOH)、乳酸[CH3CH(OH)COOH]等。
(3)2分子乳酸分子间酯化能生成一个六元环的酯,写出该酯的键线式___________ 。
(4)3.6g乳酸与足量钠反应,能生成标准状况下 的体积为
的体积为___________ L。
III.异戊二烯是重要的有机化工原料,其结构简式为 。
。
(5)化合物X与异戊二烯具有相同的分子式,与 反应后得到3−甲基−1,1,2,2−四溴丁烷。X的结构简式为
反应后得到3−甲基−1,1,2,2−四溴丁烷。X的结构简式为___________ 。
I.某些烃分子的模型如图所示

回答下列问题:
(1)等质量的上述烃,完全燃烧时耗氧量最多的是
(2)25℃时,10mL某气态烃和50mL氧气混合,完全燃烧后恢复到原来的温度和压强,体积变为35mL,则该烚可能为___________。
A. | B. | C. | D.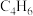 |
II.烃可以通过化学反应制得烃的衍生物,例如由丙烯可以制得丙烯酸(CH2=CHCOOH)、乳酸[CH3CH(OH)COOH]等。
(3)2分子乳酸分子间酯化能生成一个六元环的酯,写出该酯的键线式
(4)3.6g乳酸与足量钠反应,能生成标准状况下
 的体积为
的体积为III.异戊二烯是重要的有机化工原料,其结构简式为
 。
。(5)化合物X与异戊二烯具有相同的分子式,与
 反应后得到3−甲基−1,1,2,2−四溴丁烷。X的结构简式为
反应后得到3−甲基−1,1,2,2−四溴丁烷。X的结构简式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】黑火药的爆炸反应为2KNO3+3C+S A+N2↑+3CO2↑(已配平)
A+N2↑+3CO2↑(已配平)
(1)除S外,上列元素的电负性从大到小依次为______________________ 。
(2)在生成物中,A的晶体类型为____________ 、其电子式为___________ 。
(3)含极性共价键的分子的中心原子轨道杂化类型为____________________ 。
(4)已知CN-与N2结构相似,推算HCN分子中σ键与π键数目之比为________ 。
 A+N2↑+3CO2↑(已配平)
A+N2↑+3CO2↑(已配平)(1)除S外,上列元素的电负性从大到小依次为
(2)在生成物中,A的晶体类型为
(3)含极性共价键的分子的中心原子轨道杂化类型为
(4)已知CN-与N2结构相似,推算HCN分子中σ键与π键数目之比为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
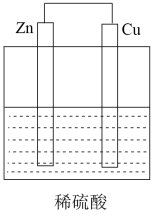
【推荐1】Ⅰ如图所示是Zn和Cu形成的原电池,某实验兴趣小组做完实验后,在读书卡上的记录如下,则卡片上的描述合理的是____________ (填序号)。
Ⅱ锌锰电池(俗称干电池)在生活中的用量很大.两种锌锰电池的构造如图(甲)所示.回答下列问题:
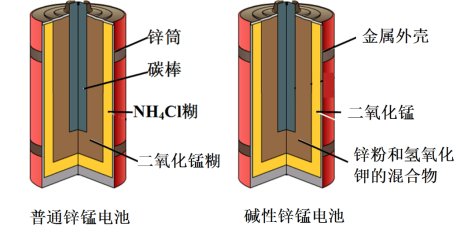
(1)普通锌锰电池放电时发生的主要反应为:Zn+2NH4Cl+2MnO2=Zn(NH3)2Cl2+2MnOOH
①该电池中,负极材料主要是_________ ,电解质的主要成分是__________ ;
②与普通锌锰电池相比,碱性锌锰电池的优点及其理由是______________________ 。
(2)下图表示回收利用废旧普通锌锰电池工艺(不考虑废旧电池中实际存在的少量其他金属).
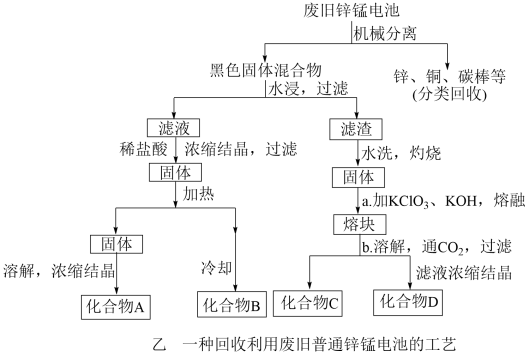
①图(乙)中产物的化学式分别为A________ ,B________ ;
②操作a中得到熔块的主要成分是K2MnO4.操作b中,绿色的K2MnO4溶液反应生成紫色溶液和一种黑色固体,该反应的离子方程式为_____________________________ 。
| 实验后的记录: ①Cu为负极,Zn为正极 ②Cu极上有气泡产生,发生还原反应 ③SO42-向Cu极移动 ④若有0.5mol电子流经导线,则可产生0.25mol气体 ⑤电子的流向是:Cu→Zn ⑥正极反应式:Cu-2e-=Cu2+,发生氧化反应 |

Ⅱ锌锰电池(俗称干电池)在生活中的用量很大.两种锌锰电池的构造如图(甲)所示.回答下列问题:

(1)普通锌锰电池放电时发生的主要反应为:Zn+2NH4Cl+2MnO2=Zn(NH3)2Cl2+2MnOOH
①该电池中,负极材料主要是
②与普通锌锰电池相比,碱性锌锰电池的优点及其理由是
(2)下图表示回收利用废旧普通锌锰电池工艺(不考虑废旧电池中实际存在的少量其他金属).

①图(乙)中产物的化学式分别为A
②操作a中得到熔块的主要成分是K2MnO4.操作b中,绿色的K2MnO4溶液反应生成紫色溶液和一种黑色固体,该反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】原电池原理的发现是储能和供能技术的巨大进步,是化学对人类的一项重大贡献。某课外实验小组欲探究铝和铜的金属性(原子失电子能力)强弱,同学们提出了如下实验方案:
A.比较铝和铜的硬度和熔点
B.比较二者在稀硫酸中的反应现象
C.将铝片放入硫酸铜溶液,观察铝片上是否有红色物质
D.将铝片、铜片用导线连接后共同投入氢氧化钠溶液中接入电流计,观察电流方向
(1)上述方案中能达到实验目的的是_______ (填字母)。
(2)上述方案D中负极为_______ ,电极反应为_______ 。
(3)将纯锌片和纯铜片按如图所示方式插入500mL相同浓度的稀硫酸一段时间,两烧杯中均产生气泡,有同学认为产生气泡的位置相同,你赞同吗?请写出理由_______ 。

(4)当甲中产生2.24L(标准状况)气体时,将锌、铜片取出(设反应前后溶液体积不变),再将烧杯中的溶液稀释至1L,测得溶液中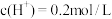 。试确定原稀硫酸的物质的量浓度为
。试确定原稀硫酸的物质的量浓度为_______ mol/L。
(5)镍铁电池放电时也可产生FeO(OH),其工作原理如图所示。
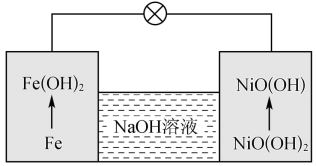
Fe放电生成 后,继续放电时,电极上的
后,继续放电时,电极上的 可转化为
可转化为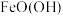 ,写出该过程的电极反应式:
,写出该过程的电极反应式:_______ 。
A.比较铝和铜的硬度和熔点
B.比较二者在稀硫酸中的反应现象
C.将铝片放入硫酸铜溶液,观察铝片上是否有红色物质
D.将铝片、铜片用导线连接后共同投入氢氧化钠溶液中接入电流计,观察电流方向
(1)上述方案中能达到实验目的的是
(2)上述方案D中负极为
(3)将纯锌片和纯铜片按如图所示方式插入500mL相同浓度的稀硫酸一段时间,两烧杯中均产生气泡,有同学认为产生气泡的位置相同,你赞同吗?请写出理由

(4)当甲中产生2.24L(标准状况)气体时,将锌、铜片取出(设反应前后溶液体积不变),再将烧杯中的溶液稀释至1L,测得溶液中
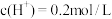 。试确定原稀硫酸的物质的量浓度为
。试确定原稀硫酸的物质的量浓度为(5)镍铁电池放电时也可产生FeO(OH),其工作原理如图所示。

Fe放电生成
 后,继续放电时,电极上的
后,继续放电时,电极上的 可转化为
可转化为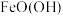 ,写出该过程的电极反应式:
,写出该过程的电极反应式:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】氢能是一种极具发展潜力的清洁能源。3月29日,长城汽车氢能战略全球发布会推出氢能技术,并计划今年推出全球首款C级氢燃料电池SUV。关于氢能,根据要求回答问题:
I.制备氢气
制备氢气常采用以下方法:
①电解水法:2H2O 2H2↑+O2↑
2H2↑+O2↑
②水煤气法:C+H2O(g) CO+H2,CO+H2O
CO+H2,CO+H2O CO2+H2↑
CO2+H2↑
③太阳能光催化分解水法:2H2O 2H2↑+O2↑
2H2↑+O2↑
(1)三种方法中最节能的是___________ (填标号)。
(2)已知拆开1 mol H -H、1 mol O=O和 1 mol H-О分别需要的能量依次为436kJ、498kJ和463kJ,则理论上每3.6 gH2O(g)完全分解,需___________ (填“放出”或“吸收")能量___________ kJ。下列能正确表示该过程的能量变化示意图的是___________ (填标号)。
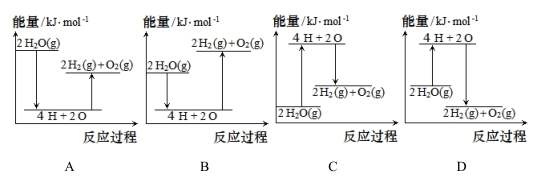
II.氢燃料电池
(3)氢燃料电池具有清洁高效等优点,其简易装置如下图所示。
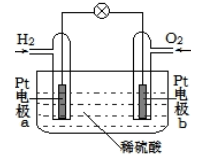
该电池正极反应式为___________ ;反应过程中将___________ 能转化为___________ 能。
I.制备氢气
制备氢气常采用以下方法:
①电解水法:2H2O
 2H2↑+O2↑
2H2↑+O2↑②水煤气法:C+H2O(g)
 CO+H2,CO+H2O
CO+H2,CO+H2O CO2+H2↑
CO2+H2↑③太阳能光催化分解水法:2H2O
 2H2↑+O2↑
2H2↑+O2↑(1)三种方法中最节能的是
(2)已知拆开1 mol H -H、1 mol O=O和 1 mol H-О分别需要的能量依次为436kJ、498kJ和463kJ,则理论上每3.6 gH2O(g)完全分解,需

II.氢燃料电池
(3)氢燃料电池具有清洁高效等优点,其简易装置如下图所示。

该电池正极反应式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】某同学用下图装置电解硫酸钾溶液来获得氧气、氢气、硫酸和氢氧化钾。
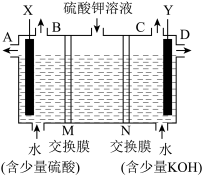
(1)X极与电源的________ (填“正”或“负”)极相连,氢气从________ (填“A”“B”“C”或“D”)口导出。
(2)离子交换膜只允许一类离子通过,则M为________ (填“阴离子”或“阳离子”,下同)交换膜,N为________ 交换膜,图中少量硫酸和少量氢氧化钾的作用是________________________________________ 。
(3)若将制得的氢气、氧气和氢氧化钾溶液组合为氢氧燃料电池(石墨为电极),则电池负极的电极反应式为______________________________________________ 。
(4)若使用铅蓄电池作电源完成上述电解,当制得11.2 L标准状况下的氢气时,理论上铅蓄电池消耗硫酸________ mol,正极板质量增加______ g,负极板质量增加________ g。

(1)X极与电源的
(2)离子交换膜只允许一类离子通过,则M为
(3)若将制得的氢气、氧气和氢氧化钾溶液组合为氢氧燃料电池(石墨为电极),则电池负极的电极反应式为
(4)若使用铅蓄电池作电源完成上述电解,当制得11.2 L标准状况下的氢气时,理论上铅蓄电池消耗硫酸
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】按要求完成下列问题。
⑴写出铅蓄电池放电时的总反应和两个电极反应及反应类型
放电总反应:____________________________________________
负极:____________________________ ( ) 反应;
正极:____________________________ ( ) 反应;
⑵写出氯碱工业中电解饱和食盐水的总反应和两个电极反应及反应类型
电解总反应:_____________________________________________
阳极:_____________________________ ( ) 反应;
阴极:_____________________________ ( ) 反应;
⑶氢氧燃料电池中用KOH做电解质溶液,H2是还原剂,O2是助燃剂,写出正、负两极的电极反应
负极:_______________________ 正极:_____________________
⑴写出铅蓄电池放电时的总反应和两个电极反应及反应类型
放电总反应:
负极:
正极:
⑵写出氯碱工业中电解饱和食盐水的总反应和两个电极反应及反应类型
电解总反应:
阳极:
阴极:
⑶氢氧燃料电池中用KOH做电解质溶液,H2是还原剂,O2是助燃剂,写出正、负两极的电极反应
负极:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】回答下列问题
(1)将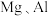 用导线相连浸入
用导线相连浸入 溶液中,形成原电池,负极的电极反应为
溶液中,形成原电池,负极的电极反应为___________
(2)铅蓄电池放电时的正极反应为___________ 。
(3)以硫酸溶液为电解质时,甲烷燃料电池的正极反应为___________ 。
(4)某研究性学习小组根据反应 设计如下原电池,其中甲、乙两烧杯中各物质的物质的量浓度均为
设计如下原电池,其中甲、乙两烧杯中各物质的物质的量浓度均为 ,溶液的体积均为
,溶液的体积均为 ,盐桥中装有饱和
,盐桥中装有饱和 溶液。
溶液。
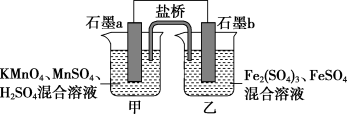
回答下列问题:
①此原电池的负极是石墨___________ (填“a”或“b”)。
②电池工作时,盐桥中的 移向
移向___________ (填“甲”或“乙”)烧杯。
③甲烧杯中的电极反应式为___________ 。
④若不考虑溶液的体积变化, ,则反应中转移的电子为
,则反应中转移的电子为___________  。
。
(1)将
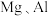 用导线相连浸入
用导线相连浸入 溶液中,形成原电池,负极的电极反应为
溶液中,形成原电池,负极的电极反应为(2)铅蓄电池放电时的正极反应为
(3)以硫酸溶液为电解质时,甲烷燃料电池的正极反应为
(4)某研究性学习小组根据反应
 设计如下原电池,其中甲、乙两烧杯中各物质的物质的量浓度均为
设计如下原电池,其中甲、乙两烧杯中各物质的物质的量浓度均为 ,溶液的体积均为
,溶液的体积均为 ,盐桥中装有饱和
,盐桥中装有饱和 溶液。
溶液。
回答下列问题:
①此原电池的负极是石墨
②电池工作时,盐桥中的
 移向
移向③甲烧杯中的电极反应式为
④若不考虑溶液的体积变化,
 ,则反应中转移的电子为
,则反应中转移的电子为 。
。
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】北京冬奥会赛区内将使用氢燃料清洁能源车辆,就是利用原电池原理提供清洁电能,回答下面问题:
(1)某氢氧燃料电池工作示意图如图1。

①电极a是_______ (填“正极”“负极”“阳极”或“阴极”),电极a发生的电极反应是_______ 。
②电解质KOH溶液中K+向_______ 电极移动(填“a”或“b”)。
(2)利用图1中的原电池电解饱和食盐水,可以有效的利用海水资源,原理如图:
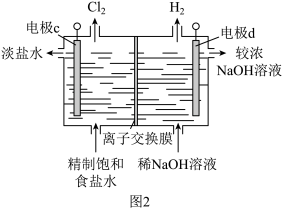
①电极d应连接图1装置的_______ 电极(填“a”或“b”),离子交换膜是_______ (填“阴离子交换膜”或“阳离子交换膜”)。
②写出电极c的电极反应_______ 。
③写出电解饱和食盐水的离子方程式_______ 。
(3)将铁钉的下半部分分别镀上铜和锌,放入培养皿中,加入饱和食盐水溶液,再各滴入几滴酚酞溶液和K3[Fe(CN)6]溶液。装置如图3:
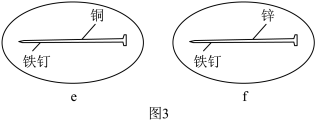
①在铁钉下半部分镀上铜的装置中,阳极材料是_______ (填化学式)。
②e装置中出现蓝色沉淀,铜电极发生的电极反应是_______ 。
③f装置中可能出现的现象是_______ 。
(1)某氢氧燃料电池工作示意图如图1。

①电极a是
②电解质KOH溶液中K+向
(2)利用图1中的原电池电解饱和食盐水,可以有效的利用海水资源,原理如图:

①电极d应连接图1装置的
②写出电极c的电极反应
③写出电解饱和食盐水的离子方程式
(3)将铁钉的下半部分分别镀上铜和锌,放入培养皿中,加入饱和食盐水溶液,再各滴入几滴酚酞溶液和K3[Fe(CN)6]溶液。装置如图3:

①在铁钉下半部分镀上铜的装置中,阳极材料是
②e装置中出现蓝色沉淀,铜电极发生的电极反应是
③f装置中可能出现的现象是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】人们应用原电池原理制作了多种电池以满足不同的需要。在现代生活、生产和科学技术发展中,电池发挥着越来越重要的作用。请根据题中提供的信息,回答下列问题:
(1)将纯铁片和纯铜片按图甲、乙方式插入100mL相同浓度的稀硫酸中一段时间,回答下列问题:
①下列说法正确的是___________ 。
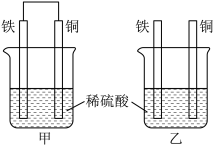
A.甲、乙均为化学能转变为电能的装置
B.甲、乙中铜片上均没有明显现象
C.甲、乙中铁片质量均减少
D.甲、乙两烧杯中 均减小
均减小
②在相同时间内,两烧杯中产生气泡的速度:甲___________ 乙(填“>”、“<”或“=”、“无法判断”)。
③请写出甲、乙中构成原电池的正极电极反应式:___________ 。电池工作时,溶液中 向
向___________ 极(填“铜极”或“铁极”)移动。当构成原电池的溶液质量增重27g时,电极上转移电子数目为___________ 。
④若将甲中的稀硫酸换为浓硝酸,则电池总反应的离子方程式为___________ 。
(2)燃料电池是目前电池研究的热点之一,某课外小组自制的氢氧燃料电池如图所示,a、b均为惰性电极。

①正极是___________ (填“a”或“b”),a极发生的电极反应式是___________ 。
②将上图 改成甲烷,电解质溶液改成
改成甲烷,电解质溶液改成 溶液。通甲烷电极反应式为
溶液。通甲烷电极反应式为___________ 。
(3)用燃料电池做电源,用惰性电极电解饱和食盐水,电解总反应方程式为___________ 。
(1)将纯铁片和纯铜片按图甲、乙方式插入100mL相同浓度的稀硫酸中一段时间,回答下列问题:
①下列说法正确的是

A.甲、乙均为化学能转变为电能的装置
B.甲、乙中铜片上均没有明显现象
C.甲、乙中铁片质量均减少
D.甲、乙两烧杯中
 均减小
均减小②在相同时间内,两烧杯中产生气泡的速度:甲
③请写出甲、乙中构成原电池的正极电极反应式:
 向
向④若将甲中的稀硫酸换为浓硝酸,则电池总反应的离子方程式为
(2)燃料电池是目前电池研究的热点之一,某课外小组自制的氢氧燃料电池如图所示,a、b均为惰性电极。

①正极是
②将上图
 改成甲烷,电解质溶液改成
改成甲烷,电解质溶液改成 溶液。通甲烷电极反应式为
溶液。通甲烷电极反应式为(3)用燃料电池做电源,用惰性电极电解饱和食盐水,电解总反应方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】下图是某氢氧燃料电池的结构示意图,电解质为硫酸溶液。氢气在催化剂作用下提供质子(H+)和电子,电子经外电路、质子经内电路到达另一极与氧气反应,电池总反应为2H2+O2=2H2O,完成下列问题:
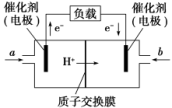
(1)通H2的一极为电池的_______ 极(填“正”或“负”)。
(2)b极上的电极反应式为:_______ 。
(3)每转移0.2mol电子,消耗H2的体积为_______ L(标准状况下)。
(4)若将氢气换成甲烷(CH4),电解质溶液更换为NaOH溶液,去掉质子交换膜。
①则a极的电极反应式为_______ 。
②电池工作一段时间后电解质溶液的pH_______ (填“增大”“减小”或“不变”)。
(5)若将氢气换成一氧化碳(CO),电解质溶液更换为固体电解质(传导O2-),去掉质子交换膜。则a极的电极反应式为_______ 。

(1)通H2的一极为电池的
(2)b极上的电极反应式为:
(3)每转移0.2mol电子,消耗H2的体积为
(4)若将氢气换成甲烷(CH4),电解质溶液更换为NaOH溶液,去掉质子交换膜。
①则a极的电极反应式为
②电池工作一段时间后电解质溶液的pH
(5)若将氢气换成一氧化碳(CO),电解质溶液更换为固体电解质(传导O2-),去掉质子交换膜。则a极的电极反应式为
您最近一年使用:0次

 )还原为Cr3+的离子方程式
)还原为Cr3+的离子方程式

