一定温度下,反应N2(g)+3H2(g)  2NH3(g)达到化学平衡状态的标志是
2NH3(g)达到化学平衡状态的标志是
 2NH3(g)达到化学平衡状态的标志是
2NH3(g)达到化学平衡状态的标志是| A.N2、H2和NH3的质量分数不再改变 |
| B.c(N2)∶c(H2)∶c(NH3)=1∶3∶2 |
| C.断裂1 mol N≡N键的同时,形成6 mol N—H键 |
| D.N2与H2的物质的量之和是NH3的物质的量的2倍 |
更新时间:2019-07-08 10:20:42
|
【知识点】 化学平衡状态的判断方法解读
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】某温度下,在容积为1L的密闭容器中充入1 mol CO2和3.25mol H2,发生反应: ,测得CH3OH(g)的物质的量随时间的变化如图所示。已知:此温度下该反应的平衡常数K=2.25。下列说法正确的是
,测得CH3OH(g)的物质的量随时间的变化如图所示。已知:此温度下该反应的平衡常数K=2.25。下列说法正确的是
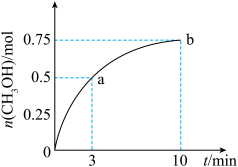
 ,测得CH3OH(g)的物质的量随时间的变化如图所示。已知:此温度下该反应的平衡常数K=2.25。下列说法正确的是
,测得CH3OH(g)的物质的量随时间的变化如图所示。已知:此温度下该反应的平衡常数K=2.25。下列说法正确的是
| A.点b所对应的状态为化学平衡状态 |
| B.0~10min,v(H2)=0.075mol·L-1·min-1 |
| C.点a时c(CO2)=0.25mol·L-1 |
D.欲增大平衡状态时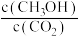 的值,可保持其他条件不变,升高温度 的值,可保持其他条件不变,升高温度 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】T℃时,向恒温恒容密闭容器中充入一定浓度的N2O4(无色),测得各气体的浓度随时间变化的关系如图所示。下列说法错误的是
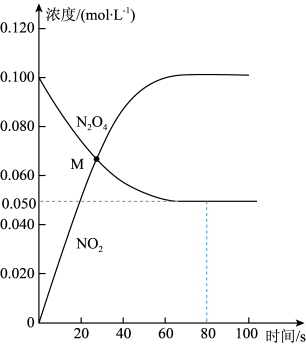

| A.0~20s内N2O4的分解速率比20~40s内的快 |
| B.由M点可计算出该温度时N2O4的平衡转化率为33.3% |
| C.混合气体的颜色不再变化时反应达到平衡状态 |
| D.0~80s内生成NO2的平均反应速率为1.25×10-3mol·L-1·s-1 |
您最近半年使用:0次

 2NH3(g)的反应,达到化学平衡状态的标志为
2NH3(g)的反应,达到化学平衡状态的标志为

