下表是元素周期表的一部分,①~⑫分别代表12种元素,请回答:
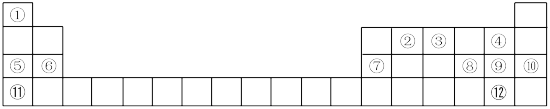
(1)写出12种元素中化学性质最不活泼的元素的原子结构示意图______________ 。
(2)⑪在元素周期表中的位置是____________________________ 。
(3)12种元素形成的单质中硬度最大的是________________ (填名称)。
(4)用电子式表示①与⑪形成化合物的过程_______________________ 。
(5)可以用来验证⑥⑦两种元素金属性强弱的实验是__________ (填字母序号)。
a 将在空气中放置已久的这两种元素的块状单质分别放入水中
b 将形状、大小相同的无氧化膜的这两种元素的单质分别和同浓度同体积的盐酸反应
c 将形状、大小相同的无氧化膜的这两种元素的单质分别和温度相同的热水作用,并滴入酚酞
d 比较这两种元素的氢化物的热稳定性
(6)⑧⑨两种元素的简单阴离子中还原性较强的是________ (填离子名称);用一个置换反应证明这一结论__________________________ (写化学方程式)。

(1)写出12种元素中化学性质最不活泼的元素的原子结构示意图
(2)⑪在元素周期表中的位置是
(3)12种元素形成的单质中硬度最大的是
(4)用电子式表示①与⑪形成化合物的过程
(5)可以用来验证⑥⑦两种元素金属性强弱的实验是
a 将在空气中放置已久的这两种元素的块状单质分别放入水中
b 将形状、大小相同的无氧化膜的这两种元素的单质分别和同浓度同体积的盐酸反应
c 将形状、大小相同的无氧化膜的这两种元素的单质分别和温度相同的热水作用,并滴入酚酞
d 比较这两种元素的氢化物的热稳定性
(6)⑧⑨两种元素的简单阴离子中还原性较强的是
更新时间:2019-07-20 22:40:34
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】已知非金属单质硫(S)是淡黄色固体粉末,难溶于水。为了验证氯元素的非金属性比硫元素的非金属性强(提示:Na2S +2HCl = 2NaCl+ H2S↑),某化学实验小组设计了如下实验,请回答下列问题:

(1)画出虚线框内的实验装置图____ ,所加试剂为___________ ,该装置的作用是__________ 。
(2)装置B中盛放的试剂是____ (填序号),
A.Na2S溶液 B.Na2SO3溶液 C.Na2SO4溶液
B装置中发生反应的离子方程式为___________________________ 。
(3)已知:①硫原子与氯原子的电子层数相同,氯的原子半径小于硫原子。②高氯酸的酸性比硫酸强;③铁与氯气在加热条件下反应生成三氯化铁,铁与硫在加热条件下反应生成硫化亚铁;④HCl比H2S稳定;⑤硫酸比次氯酸稳定;能说明氯的非金属性比硫强的是____ (填序号)。
A.全部 B. ①②③④ C.①②④⑤ D. ①③④⑤
(4)装置C中盛放烧碱溶液,目的是吸收反应后剩余的气体,防止污染空气,写出该装置中所发生反应的离子方程式:_____________________ 。

(1)画出虚线框内的实验装置图
(2)装置B中盛放的试剂是
A.Na2S溶液 B.Na2SO3溶液 C.Na2SO4溶液
B装置中发生反应的离子方程式为
(3)已知:①硫原子与氯原子的电子层数相同,氯的原子半径小于硫原子。②高氯酸的酸性比硫酸强;③铁与氯气在加热条件下反应生成三氯化铁,铁与硫在加热条件下反应生成硫化亚铁;④HCl比H2S稳定;⑤硫酸比次氯酸稳定;能说明氯的非金属性比硫强的是
A.全部 B. ①②③④ C.①②④⑤ D. ①③④⑤
(4)装置C中盛放烧碱溶液,目的是吸收反应后剩余的气体,防止污染空气,写出该装置中所发生反应的离子方程式:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】某研究性学习小组的甲,乙同学分别设计了以下实验来验证元素周期律。
(1)甲同学将NaOH溶液滴加在 溶液中,可观察到的现象为
溶液中,可观察到的现象为_______ 。由此得出碱性的强弱关系为_______ (用化学式表示)。
(2)乙同学设计了如图装置来验证元素非金属性的变化规律,根据要求完成下列各小题。

①实验装置:仪器A名称为_______ 。
②实验步骤:连接仪器、_______ 、加药品后,打开活塞,然后滴入试剂。
③已知常温下,高锰酸钾和浓盐酸反应能生成氯气。实验室中现有药品 溶液、
溶液、 、浓盐酸、
、浓盐酸、 ,请选择合适药品设计实验验证氯的非金属性大于硫的,装置C中所装药品为
,请选择合适药品设计实验验证氯的非金属性大于硫的,装置C中所装药品为_______ ,装置C中发生反应的离子方程式为_______ 。
④已知 为难溶于水的白色胶状沉淀。若要证明非金属性:S>C>Si,则A中加
为难溶于水的白色胶状沉淀。若要证明非金属性:S>C>Si,则A中加_______ 、B中加 、C中加
、C中加 ,能说明碳元素的非金属性比硅元素的非金属性强的实验现象是
,能说明碳元素的非金属性比硅元素的非金属性强的实验现象是_______ 。试管C中发生反应的离子方程式是_______ 。
(1)甲同学将NaOH溶液滴加在
 溶液中,可观察到的现象为
溶液中,可观察到的现象为(2)乙同学设计了如图装置来验证元素非金属性的变化规律,根据要求完成下列各小题。

①实验装置:仪器A名称为
②实验步骤:连接仪器、
③已知常温下,高锰酸钾和浓盐酸反应能生成氯气。实验室中现有药品
 溶液、
溶液、 、浓盐酸、
、浓盐酸、 ,请选择合适药品设计实验验证氯的非金属性大于硫的,装置C中所装药品为
,请选择合适药品设计实验验证氯的非金属性大于硫的,装置C中所装药品为④已知
 为难溶于水的白色胶状沉淀。若要证明非金属性:S>C>Si,则A中加
为难溶于水的白色胶状沉淀。若要证明非金属性:S>C>Si,则A中加 、C中加
、C中加 ,能说明碳元素的非金属性比硅元素的非金属性强的实验现象是
,能说明碳元素的非金属性比硅元素的非金属性强的实验现象是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】某同学为探究元素周期表中元素性质的递变规律,设计了如下系列实验。
Ⅰ.(1)将钠、钾、镁、铝各1 mol分别投入到足量的同浓度的盐酸中,试预测实验结果:________ 与盐酸反应最剧烈,______ 与盐酸反应的速度最慢;________ 与盐酸反应产生的气体最多。
(2)向Na2S溶液中通入氯气出现黄色浑浊,可证明Cl的非金属性比S强,反应的离子方程式为______________ 。
(3)将NaOH溶液与NH4Cl溶液混合生成NH3·H2O,从而验证NaOH碱性强于NH3·H2O,继而可以验证Na的金属性强于氮,你认为此设计是否合理?并说明理由。__________ 。
Ⅱ.利用如图装置可验证同主族元素非金属性的变化规律

(4)仪器B的名称为________ ,干燥管D的作用为____________ 。
(5)若要证明非金属性:Cl>I,则A中加浓盐酸,B中加KMnO4(KMnO4与浓盐酸常温下反应生成氯气),C中加淀粉碘化钾混合溶液,观察到C中溶液______________ (填现象),即可证明。从环境保护的观点考虑,此装置缺少尾气处理装置,可用______________ 溶液吸收尾气。
Ⅰ.(1)将钠、钾、镁、铝各1 mol分别投入到足量的同浓度的盐酸中,试预测实验结果:
(2)向Na2S溶液中通入氯气出现黄色浑浊,可证明Cl的非金属性比S强,反应的离子方程式为
(3)将NaOH溶液与NH4Cl溶液混合生成NH3·H2O,从而验证NaOH碱性强于NH3·H2O,继而可以验证Na的金属性强于氮,你认为此设计是否合理?并说明理由。
Ⅱ.利用如图装置可验证同主族元素非金属性的变化规律

(4)仪器B的名称为
(5)若要证明非金属性:Cl>I,则A中加浓盐酸,B中加KMnO4(KMnO4与浓盐酸常温下反应生成氯气),C中加淀粉碘化钾混合溶液,观察到C中溶液
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】某研究性学习小组设计了一组实验来探究元素周期律。
甲同学根据元素非金属性与对应最高价含氧酸之间的关系,设计了如图1装置来一次性完成N、C、Si三种非金属元素的非金属性强弱比较的实验研究;
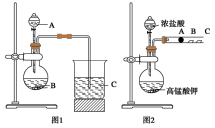
(1)写出选用物质的名称:A_________ ,B________ ,C________ ;上述反应的离子方程式____________ ;___________ 。
乙同学设计了如图2装置来验证卤族元素性质的递变规律。A、B、C三处分别是沾有NaBr溶液的棉花、湿润的淀粉KI试纸、湿润红纸。
已知常温下浓盐酸与高锰酸钾能反应生成氯气。
(2)乙同学的实验原理是_______________ ,写出B处的离子方程式: _______________ 。
甲同学根据元素非金属性与对应最高价含氧酸之间的关系,设计了如图1装置来一次性完成N、C、Si三种非金属元素的非金属性强弱比较的实验研究;

(1)写出选用物质的名称:A
乙同学设计了如图2装置来验证卤族元素性质的递变规律。A、B、C三处分别是沾有NaBr溶液的棉花、湿润的淀粉KI试纸、湿润红纸。
已知常温下浓盐酸与高锰酸钾能反应生成氯气。
(2)乙同学的实验原理是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】如图是实验室制备氯气并进行一系列相关实验的装置(夹持设备已略)。

(1)装置A是氯气的发生装置,请写出相应反应的化学方程式:_____ ;
(2)装置B中饱和食盐水的作用是_____ ;同时装置B也是安全瓶,监测实验进行时C中是否发生堵塞,请写出发生堵塞时B中的现象:______ ;
(3)装置C的实验目的是验证氯气是否具有漂白性,为此C中I、II、III处依次放入物质的组合应是______ (填字母编号)
(4)设计装置D,E的目的是比较氯、溴、碘单质的氧化性。反应一段时间后,打开活塞,将装置D中少量溶液加入装置E中,振荡,观察到的现象是____ ,该现象_____ (填“能”或“不能”)说明溴单质的氧化性强于碘,原因是_____ ;
(5)装置F的作用是______ ,其烧杯中的溶液不能选用下列中的(填字母编号)_____ 。
a.饱和NaOH溶液 b.饱和Ca(OH)2溶液
c.饱和Na2SO3溶液 d.饱和Na2CO3溶液

(1)装置A是氯气的发生装置,请写出相应反应的化学方程式:
(2)装置B中饱和食盐水的作用是
(3)装置C的实验目的是验证氯气是否具有漂白性,为此C中I、II、III处依次放入物质的组合应是
| 编号 | Ⅰ | Ⅱ | Ⅲ |
| a | 干燥的有色布条 | 碱石灰 | 湿润的有色布条 |
| b | 干燥的有色布条 | 无水硫酸铜 | 湿润的有色布条 |
| c | 湿润的有色布条 | 浓硫酸 | 干燥的有色布条 |
| d | 湿润的有色布条 | 无水氯化钙 | 干燥的有色布条 |
(5)装置F的作用是
a.饱和NaOH溶液 b.饱和Ca(OH)2溶液
c.饱和Na2SO3溶液 d.饱和Na2CO3溶液
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】某同学利用如图装置探究元素周期表中元素性质的递变规律。

(1) 仪器B的名称为________ ,干燥管D的作用为_________ 。
(2)若要证明非金属性:Cl > I,则A中加浓盐酸,B中加KMnO4(已知KMnO4与浓盐酸常温下反应生成氯气),C中加淀粉碘化钾混合溶液,观察到C中溶液________ 的现象,即可证明。此装置缺少尾气处理装置,可用________ 溶液吸收尾气,反应的离子方程式为:__________________________________ 。
(3)现有盐酸、CaCO3和Na2SiO3溶液,若要证明非金属性:C>Si,则C中装试剂______ 。观察到C中溶液________ 的现象,即可证明。但有同学认为盐酸具有挥发性,可进入C中干扰试验,也会产生相同的实验现象,为了避免干扰,应在两装置间添加装有________ 溶液的洗气瓶除去。

(1) 仪器B的名称为
(2)若要证明非金属性:Cl > I,则A中加浓盐酸,B中加KMnO4(已知KMnO4与浓盐酸常温下反应生成氯气),C中加淀粉碘化钾混合溶液,观察到C中溶液
(3)现有盐酸、CaCO3和Na2SiO3溶液,若要证明非金属性:C>Si,则C中装试剂
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】A、B、C、D都是短周期元素,原子半径:D>C>A>B。已知:A、B同周期,A、C处于同一主族;C原子核内的质子数等于A、B原子核内的质子数之和;C原子最外层电子数是D原子最外层电子数的3倍。试回答:
(1)写出元素的名称:A__________ 。
(2)写出由B、D组成的两种化合物的电子式分别为:___________ 、__________ 。
(3)A、C的最高价氧化物对应水化物中酸性较强的是__________ (写水化物的分子式)。
(4)写出C的氧化物与D的最高价氧化物对应水化物反应的离子方程式_______________________ 。
(1)写出元素的名称:A
(2)写出由B、D组成的两种化合物的电子式分别为:
(3)A、C的最高价氧化物对应水化物中酸性较强的是
(4)写出C的氧化物与D的最高价氧化物对应水化物反应的离子方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】下表是现行中学化学教科书中元素周期表的一部分,表中的每个编号表示一种元素,请根据要求回答问题。
(1)② 表示的元素是______ (填元素符号);
(2)①、⑤两种元素的原子半径大小为①______ ⑤(填“< ”或“>”);
(3)③、④两种元素的金属性强弱顺序为:③______ ④(填“< ”或“>”);
(4)写出④与⑥两种元素所形成化合物的化学式_________ 。
(5)①最简单氢化物的结构式为_________ 。
(6)③与⑥的最高价氧化物的水化物反应的离子方程式为__________________ 。
族 周期 | IA | 0 | ||||||
1 | H | IIA | IIIA | IVA | VA | VIA | VIIA | |
2 | ① | ② | ||||||
3 | ③ | ④ | ⑤ | ⑥ |
(2)①、⑤两种元素的原子半径大小为①
(3)③、④两种元素的金属性强弱顺序为:③
(4)写出④与⑥两种元素所形成化合物的化学式
(5)①最简单氢化物的结构式为
(6)③与⑥的最高价氧化物的水化物反应的离子方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】下表是元素周期表的一部分,表中所列的每个字母分别代表某一元素。
(1)表中所列短周期元素中,原子半径最大的是___________ (填元素符号)。
(2)元素b、d、f的最高价氧化物对应水化物的碱性较强的为___________ (填化学式)。
(3)元素j、l的氢化物的稳定性从强到弱的顺序为___________ (填化学式)。
(4)由a、g、i三种元素组成的离子化合物是___________ ,在实验室检验该化合物中阳离子的方法是___________ 。
| a | |||||||||||||||||
| g | i | ||||||||||||||||
| b | d | f | h | j | l | m | |||||||||||
| c | k |
(2)元素b、d、f的最高价氧化物对应水化物的碱性较强的为
(3)元素j、l的氢化物的稳定性从强到弱的顺序为
(4)由a、g、i三种元素组成的离子化合物是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】下表列出了①~⑨九种元素在周期表中的位置:
请按要求回答下列问题。
(1)元素③在周期表中所处位置_______ 。
(2)元素⑧的原子结构示意图是_______ 。
(3)②③④的简单气态氢化物的稳定性由强到弱的顺序为:_______ (用氢化物的化学式表示)。
(4)写出元素⑥形成的单质在氧气中燃烧的化学方程式:_______ 。
(5)⑥与⑨组成化合物甲,用电子式表示甲的形成过程:_______ 。
IA | 0族 | |||||||
1 | ① | IIA | IIIA | IVA | VA | VIA | VIIA | |
2 | ② | ③ | ④ | ⑤ | ||||
3 | ⑥ | ⑦ | ⑧ | ⑨ |
(1)元素③在周期表中所处位置
(2)元素⑧的原子结构示意图是
(3)②③④的简单气态氢化物的稳定性由强到弱的顺序为:
(4)写出元素⑥形成的单质在氧气中燃烧的化学方程式:
(5)⑥与⑨组成化合物甲,用电子式表示甲的形成过程:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】如图是元素周期表的前四周期,请回答下列问题:
(1)元素③在元素周期表位置___________ ;④⑦⑧的简单氢化物稳定性由强到弱的顺序是___________ (用化学式表示);
(2)元素⑤⑦⑧的简单离子半径由大到小顺序___________ (用化学式表示);
(3)⑥与⑧的最高价氧化物的水化物与铜反应的化学方程式为___________ ;
(4)⑤⑥⑨的金属性由强到弱的顺序是___________ (用化学式表示);
(5)用电子式表示⑤元素和⑦元素形成化合物的形成过程___________ 。
| 1 | ① | |||||||
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ||||
| 4 | ⑨ | |||||||
(2)元素⑤⑦⑧的简单离子半径由大到小顺序
(3)⑥与⑧的最高价氧化物的水化物与铜反应的化学方程式为
(4)⑤⑥⑨的金属性由强到弱的顺序是
(5)用电子式表示⑤元素和⑦元素形成化合物的形成过程
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】原子序数由小到大排列的四种短周期元素X、Y、Z、W,其中X、Z、W与氢元素可组成XH3、H2Z和HW型共价化合物;Y与氧元素可组成Y2O和Y2O2型离子化合物。
(1)写出Y2O2的电子式:________ ,其中含有的化学键是________ 。
(2)用电子式表示Y2O的形成过程:____________________________ 。
(3)X、Z、W三种元素的最高价氧化物对应的水化物中,酸性最强的是________ (填化学式)。
(4)由X、W组成的化合物分子中,X、W原子的最外层均达到8电子稳定结构,该化合物的化学式为_________________________________________
(1)写出Y2O2的电子式:
(2)用电子式表示Y2O的形成过程:
(3)X、Z、W三种元素的最高价氧化物对应的水化物中,酸性最强的是
(4)由X、W组成的化合物分子中,X、W原子的最外层均达到8电子稳定结构,该化合物的化学式为
您最近一年使用:0次



