丙烷是液化石油气主要成分之一,是一种优良的燃料。试回答下列问题:

(1)如图是一定量丙烷完全燃烧生成CO2和1mol H2O(l)过程中的能量变化图,(图中的括号内填入“+”或“﹣”)_____ 。写出表示丙烷燃烧热的热化学方程式:_________________________
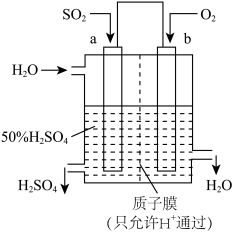
(2)科研人员设想用如图所示装置生产硫酸。
①上述生产硫酸的总反应方程式为_____________ ,b 是___________ 极(填“正”或“负”),b 电极反应式为______________________________ ,a 电极发生______________ (填“氧化反应”或“还原反应”)。②生产过程中H+向_____ (填 a 或 b)电极区域运动。
(3)将两个铂电极插入氢氧化钾溶液中,向两极分别通入甲烷和氧气,可构成甲烷燃料电池,已知通入甲烷的一极为负极,其电极反应式为:_______________________ 。电池在放电过程中,溶液的pH值将______________ 。(填“下降”“上升”或“不变”)

(1)如图是一定量丙烷完全燃烧生成CO2和1mol H2O(l)过程中的能量变化图,(图中的括号内填入“+”或“﹣”)

(2)科研人员设想用如图所示装置生产硫酸。
①上述生产硫酸的总反应方程式为
(3)将两个铂电极插入氢氧化钾溶液中,向两极分别通入甲烷和氧气,可构成甲烷燃料电池,已知通入甲烷的一极为负极,其电极反应式为:
更新时间:2019-07-20 20:00:11
|
相似题推荐
【推荐1】汽车发动机代用燃料包括乙醇、氢气和甲烷等。回答下列问题:
(1)在25℃、 下,一定质量的无水乙醇完全燃烧,转移6mol电子,放出热量
下,一定质量的无水乙醇完全燃烧,转移6mol电子,放出热量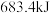 ,则乙醇燃烧热的热化学方程式为
,则乙醇燃烧热的热化学方程式为_______ 。
(2)根据图甲中的能量关系,可求得 键的键能为
键的键能为_______  。
。
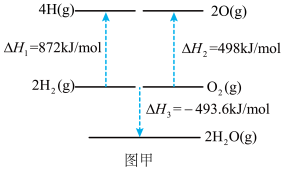
(3)甲烷完全燃烧反应的能量关系如图乙所示。

①

_______ (用含 和
和 的关系式表示)
的关系式表示)
②为提高燃料利用率,加入甲烷燃烧的催化剂,则
_______ (填“变大”、“变小”或“不变”,下同),该反应的 =
=_______ 。
(4)已知氢气的燃烧热为 ,甲烷的燃烧热为
,甲烷的燃烧热为 ,根据乙醇、氢气和甲烷的燃烧热,说明氢气作为能源的优点
,根据乙醇、氢气和甲烷的燃烧热,说明氢气作为能源的优点_______ ,_______ 。
(1)在25℃、
 下,一定质量的无水乙醇完全燃烧,转移6mol电子,放出热量
下,一定质量的无水乙醇完全燃烧,转移6mol电子,放出热量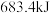 ,则乙醇燃烧热的热化学方程式为
,则乙醇燃烧热的热化学方程式为(2)根据图甲中的能量关系,可求得
 键的键能为
键的键能为 。
。
(3)甲烷完全燃烧反应的能量关系如图乙所示。

①


 和
和 的关系式表示)
的关系式表示)②为提高燃料利用率,加入甲烷燃烧的催化剂,则

 =
=(4)已知氢气的燃烧热为
 ,甲烷的燃烧热为
,甲烷的燃烧热为 ,根据乙醇、氢气和甲烷的燃烧热,说明氢气作为能源的优点
,根据乙醇、氢气和甲烷的燃烧热,说明氢气作为能源的优点
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】按要求完成下列填空:
(1)在101kPa时,4.0g硫粉在氧气中完全燃烧生成二氧化硫,放出27kJ的热量,硫的燃烧热为_______ 。
(2)在101kPa时,氢气在1.00mol氧气中完全燃烧,生成2.00mol液态水,放出571.6kJ的热量,表示氢气燃烧热的热化学方程式为_______ 。
(3)天然气中含有的微量H2S会腐蚀管道和设备,在1200℃下进行脱硫处理,H2S会被氧气氧化为SO2,并产生水蒸气。
请写出该反应的热化学方程式:_______ 。
(4)使Cl2和H2O(g)通过灼热的炭层,生成HCl(g)和CO2,当有1molCl2参与反应时释放出145kJ热量,写出该反应的热化学方程式_______ 。
(5)已知:H2O(g)=H2O(l) ∆H=-44 kJ/mol;
C2H5OH(l)+3O2(g)=2CO2(g)+3H2O(g) ∆H=-1228 kJ/mol。
写出液态酒精完全燃烧后温度恢复到室温时反应的热化学方程式:_______ 。
(1)在101kPa时,4.0g硫粉在氧气中完全燃烧生成二氧化硫,放出27kJ的热量,硫的燃烧热为
(2)在101kPa时,氢气在1.00mol氧气中完全燃烧,生成2.00mol液态水,放出571.6kJ的热量,表示氢气燃烧热的热化学方程式为
(3)天然气中含有的微量H2S会腐蚀管道和设备,在1200℃下进行脱硫处理,H2S会被氧气氧化为SO2,并产生水蒸气。
| 化学键 | H-S | O=O | H-O | SO2中共价键 |
| 键能/(kJ▪mol-1) | 339 | 498 | 464 | 1083 |
请写出该反应的热化学方程式:
(4)使Cl2和H2O(g)通过灼热的炭层,生成HCl(g)和CO2,当有1molCl2参与反应时释放出145kJ热量,写出该反应的热化学方程式
(5)已知:H2O(g)=H2O(l) ∆H=-44 kJ/mol;
C2H5OH(l)+3O2(g)=2CO2(g)+3H2O(g) ∆H=-1228 kJ/mol。
写出液态酒精完全燃烧后温度恢复到室温时反应的热化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】完成下列填空
(1) 的电子式是
的电子式是______ .
(2) 的系统命名是
的系统命名是______ .
(3)锌片、铜片连接后浸入稀硫酸形成原电池,正极反应式是______ .
(4)写出苯和液溴在催化剂作用下生成溴苯的化学方程式______ .
(5)已知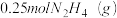 完全燃烧生成氮气和气态水时,放出
完全燃烧生成氮气和气态水时,放出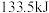 热量.写出该反应的热化学方程式
热量.写出该反应的热化学方程式______ .
(1)
 的电子式是
的电子式是(2)
 的系统命名是
的系统命名是(3)锌片、铜片连接后浸入稀硫酸形成原电池,正极反应式是
(4)写出苯和液溴在催化剂作用下生成溴苯的化学方程式
(5)已知
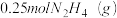 完全燃烧生成氮气和气态水时,放出
完全燃烧生成氮气和气态水时,放出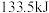 热量.写出该反应的热化学方程式
热量.写出该反应的热化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】原电池是化学对人类的一项重大贡献。
(1)依反应2Ag+ (aq)+Cu(s)=Cu2+ (aq)+2Ag(s)设计的原电池如图1所示。请回答下列问题:

①电极X的材料是______ (填化学式);电解质溶液Y是______ 溶液。
②银电极为电池的极,发生的电极反应式为______ ;
③导线上转移0.2mol电子时,Cu片质量减轻______ g。
(2)铅蓄电池在放电时发生的电池反应式为:Pb+PbO2+2H2SO4=2PbSO4+2H2O,负极电极反应式为______ 。
(3)Li-SOCl2电池可用于心脏起搏器。该电池的电极材料分别为锂和碳,电解液是LiAlCl4、SOCl2。电池的总反应可表示为4Li+2SOCl2=4LiCl+S+SO2↑。则该电池正极的电极反应式为______ 。
(4)甲醇是一种重要的化工原料和新型燃料。写出用Li2CO3和Na2CO3的熔融盐混合物作电解质的甲醇燃料电池的正极电极反应式:______ 。
(1)依反应2Ag+ (aq)+Cu(s)=Cu2+ (aq)+2Ag(s)设计的原电池如图1所示。请回答下列问题:

①电极X的材料是
②银电极为电池的极,发生的电极反应式为
③导线上转移0.2mol电子时,Cu片质量减轻
(2)铅蓄电池在放电时发生的电池反应式为:Pb+PbO2+2H2SO4=2PbSO4+2H2O,负极电极反应式为
(3)Li-SOCl2电池可用于心脏起搏器。该电池的电极材料分别为锂和碳,电解液是LiAlCl4、SOCl2。电池的总反应可表示为4Li+2SOCl2=4LiCl+S+SO2↑。则该电池正极的电极反应式为
(4)甲醇是一种重要的化工原料和新型燃料。写出用Li2CO3和Na2CO3的熔融盐混合物作电解质的甲醇燃料电池的正极电极反应式:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】电池的发明和应用是化学家们对人类社会的重要贡献之一。每一次化学电池技术的突破,都带来了电子设备革命性的发展。最近,我国在甲烷燃料电池的相关技术上获得了新突破,原理如下图所示:
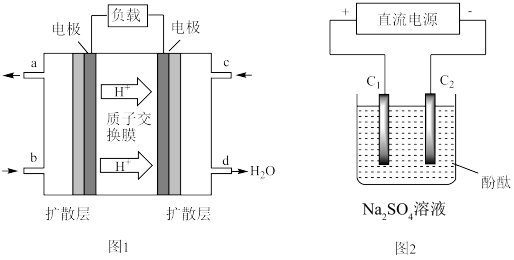
(1)甲烷燃料应从___________ 口通入(图1),发生的电极反应式___________ 。
(2)以石墨做电极电解Na2SO4溶液,如图2所示,电解开始后在___________ 的周围(填“阴极”或“阳极”)先出现红色,该极的电极反应式为___________ 。。
(3)以CuSO4溶液为电解质溶液进行粗铜(含Al、Zn、Ag、Pt、Au等杂质)的电解精炼,下列说法正确的是___________。
(4)人工肾脏可采用间接电化学方法除去代谢产物中的尿素[CO(NH2)2],原理如图。
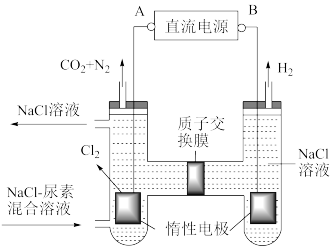
①电源的正极为___________ (填“A”或“B”)。
②电解结束后,阴极室溶液的pH与电解前相比将___________ (填“增大”、“减小”、“不变”);若收集到H22.24L(标准状况),则通过质子交换膜的H+数目为___________ (忽略气体的溶解)。

(1)甲烷燃料应从
(2)以石墨做电极电解Na2SO4溶液,如图2所示,电解开始后在
(3)以CuSO4溶液为电解质溶液进行粗铜(含Al、Zn、Ag、Pt、Au等杂质)的电解精炼,下列说法正确的是___________。
| A.利用阳极泥可回收Ag、Pt、Au等金属 |
| B.粗铜接电源正极,发生氧化反应 |
| C.溶液中Cu2+向阳极移动 |
| D.电能全部转化为化学能 |
(4)人工肾脏可采用间接电化学方法除去代谢产物中的尿素[CO(NH2)2],原理如图。

①电源的正极为
②电解结束后,阴极室溶液的pH与电解前相比将
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】一个完整的氧化还原反应方程式可以拆写成两个“半反应式”,如2Fe3++Cu=2Fe2++Cu2+,可拆写为氧化反应式:Cu-2e=Cu2+,还原反应式:2Fe3++2e-=2Fe2+。并由此实现了化学能与电能的相互转化。据此,回答下列问题。
(1)将反应Zn+2H+=Zn2++H2↑拆写为两个“半反应式”,氧化反应式为:______ ,还原反应式为:______ 。
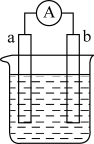
(2)由题(1)反应,设计成原电池如图所示:若电极a为Zn,电极b可选择材料:______ (只填一种);电解质溶液是______ 。
(3)由反应2H2+O2 2H2O,设计出以稀硫酸为电解质溶液的原电池电极反应式:负极
2H2O,设计出以稀硫酸为电解质溶液的原电池电极反应式:负极____ ,正极:_____ 。

(1)将反应Zn+2H+=Zn2++H2↑拆写为两个“半反应式”,氧化反应式为:
(2)由题(1)反应,设计成原电池如图所示:若电极a为Zn,电极b可选择材料:
(3)由反应2H2+O2
 2H2O,设计出以稀硫酸为电解质溶液的原电池电极反应式:负极
2H2O,设计出以稀硫酸为电解质溶液的原电池电极反应式:负极
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】电化学应用广泛。请回答下列问题:
(1)自发进行的氧化还原反应可以设计成原电池。若电池放电时的反应式为:2Cu+2H2SO4+O2= 2CuSO4+2H2O,该电池的负极材料为_______ ;正极的电极反应式为____________ 。
(2)燃料电池和二次电池的应用非常广泛。
①如图为甲烷燃料电池的示意图,则负极的电极反应式为_____________________ ;

②铅蓄电池为生活中常用的二次电池。放电时的反应为:PbO2 +Pb+2H2SO4=2PbSO4 + 2H2O,铅蓄电池负极的电极反应式为_____ ;充电时,铅蓄电池的PbO2极应与外加直流电源的____ 极相连。
(3)以铅蓄电池为电源精炼粗铜(含Fe、Pb、Ag、Au及其他不反应物质)时,以硫酸铜溶液为电解质溶液,粗铜做____ 极;精炼一段时间后,当阴极增重128 g时,铅蓄电池参加反应的硫酸的物质的量为____ mol。
(1)自发进行的氧化还原反应可以设计成原电池。若电池放电时的反应式为:2Cu+2H2SO4+O2= 2CuSO4+2H2O,该电池的负极材料为
(2)燃料电池和二次电池的应用非常广泛。
①如图为甲烷燃料电池的示意图,则负极的电极反应式为

②铅蓄电池为生活中常用的二次电池。放电时的反应为:PbO2 +Pb+2H2SO4=2PbSO4 + 2H2O,铅蓄电池负极的电极反应式为
(3)以铅蓄电池为电源精炼粗铜(含Fe、Pb、Ag、Au及其他不反应物质)时,以硫酸铜溶液为电解质溶液,粗铜做
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】用CH4和O2组合形成的质子交换膜燃料电池的结构如图丙:
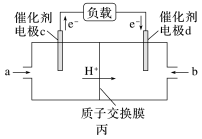
(1)电极c为电子_______ (填流入或流出)的一极,H+移向_______ (填正极或负极)。
(2)气体a为_______ (CH4或O2),若线路中转移2 mol电子,则该燃料电池理论上消耗的O2在标准状况下的体积为_______ L。

(1)电极c为电子
(2)气体a为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】CuSO4溶液是一种较重要的铜盐试剂,在电镀、印染、颜料、农药等方面有广泛应用。某同学利用CuSO4溶液进行以下实验探究。
i. 下图是根据反应Zn+CuSO4=Cu+ZnSO4设计成的锌铜原电池。

①该原电池的正极为____ ,其外电路中的电子是从____ 极(填“Zn”或“Cu”)流出。
②电解质溶液乙是______ 溶液,Zn极的电极反应式是_______ 。
③如果盐桥中的成分是K2SO4溶液,则盐桥中向左侧烧杯中移动的离子主要是_____ 。
ii. 下图中,Ⅰ是甲烷燃料电池(电解质溶液为KOH溶液)的结构示意图。
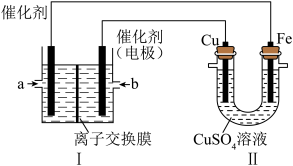
①同学想在Ⅱ中实现铁上镀铜,则Cu作____ 极,电极反应式为______ ,当线路中有0.1mol电子通过时,阴极增重_____ g。Ⅰ中消耗氧气体积是_____ L(标况下)。
②a处通入的是____ (填“CH4”或“O2”),b处电极上发生的电极反应式是___ 。Ⅰ中的总反应方程式为___ 。
③该同学若将Ⅱ中的两个电极都换成铂电极,当线路中有0.1mol电子通过时,测得溶液pH=______ (100mL的CuSO4溶液),则Ⅱ中的总反应方程式为 _______ 。
i. 下图是根据反应Zn+CuSO4=Cu+ZnSO4设计成的锌铜原电池。

①该原电池的正极为
②电解质溶液乙是
③如果盐桥中的成分是K2SO4溶液,则盐桥中向左侧烧杯中移动的离子主要是
ii. 下图中,Ⅰ是甲烷燃料电池(电解质溶液为KOH溶液)的结构示意图。

①同学想在Ⅱ中实现铁上镀铜,则Cu作
②a处通入的是
③该同学若将Ⅱ中的两个电极都换成铂电极,当线路中有0.1mol电子通过时,测得溶液pH=
您最近一年使用:0次



