关于如图所示装置的叙述,错误的是
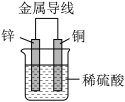

| A.锌是负极,其质量逐渐减小 | B.氢离子在铜表面被还原,产生气泡 |
| C.电子从锌片经硫酸溶液流向铜片 | D.电子从锌片经导线流向铜片 |
更新时间:2019-08-06 14:11:22
|
相似题推荐
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】某小组为研究电化学原理,设计如图装置。下列叙述不正确的是
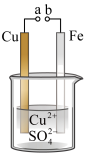
| A.a和b不连接时,铁片上会有金属铜析出 |
B.a和b用导线连接时,铜片上发生的反应为: |
| C.无论a和b是否连接,铁片均会溶解,溶液蓝色逐渐变浅 |
| D.将表面附着铜的铁片放入稀硫酸中,不能构成原电池 |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐2】一个容器被多孔隔板分隔成a、b两部分,a中盛放的是质量相等的两种金属氯化物混合物溶液、底部放一薄石墨片,b中盛放ZnCl2溶液、底部放一薄Zn片,这两个薄片可以与其上析出的沉淀一起称量。将溶液进行搅拌,用导线连接两薄片,两电极片质量变化与时间的关系如下表(按称量序号增大的次序,锌和水的反应可忽略不计):
下列说法中,不正确的是
| 称量编号 | 电极片质量的变化Δm/g | |
| 石墨 | Zn片 | |
| 实验前 | 0.00 | 0.00 |
| 1 | 0.00 | -0.20 |
| 2 | 0.00 | -0.40 |
| 3 | +0.49 | -0.56 |
| 4 | +0.74 | -0.64 |
| 5 | +1.47 | -0.88 |
| 6 | +1.30 | -1.04 |
| 7 | +1.15 | -1.18 |
| 8 | +0.95 | -1.37 |
| 9 | +0.95 | -1.37 |
| A.实验开始前,a中盛放的两种金属氯化物的质量均为18.2g |
| B.初期,石墨增量为0的原因是,两种金属氯化物中的一种被还原,且产物溶于水 |
| C.编号3~5的实验过程中发生了反应:Cu2++Cl-+e-=CuCl↓ |
| D.Cl-浓度在整个实验过程中的变化情况是:不变→减小→增加→不变 |
您最近一年使用:0次




